Таблица совместимости металлов
| Металлы, в отноше- нии которых представ- лены данные в таблице по подвержен- ности их коррозии |
Соот-ноше-ние пло-щади метал-ла к дру-гим метал-лам табли-цы |
Маг-ний |
Цинк | Алю-ми-ний | Кад- мий |
Угле-ро-дис-тая сталь | Низ-ко- леги-ро-ван-ная сталь |
Ли-тей- ная сталь |
Хро-ми- ро-ван- ная сталь |
Сви-нец | Оло-во | Медь | Нер-жа- вею-щая сталь |
| Магний | Низкое | С | С | С | С | С | С | С | С | С | С | С | |
| Высокое | У | У | С | С | С | С | С | С | С | ||||
| Цинк | Низкое | У | У | У | С | С | С | С | С | С | С | С | |
| Высокое | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ||
| Алюминий | Низкое | У | Н | Н | У | С | С | С | С | ||||
| Высокое | Н | У | Н | Н | Н | У | У | С | С | С | У | ||
| Кадмий | Низкое | Н | Н | Н | С | С | С | С | С | С | С | С | |
| Высокое | У | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ||
| Углеродистая сталь |
Низкое | Н | Н | Н | Н | У | С | С | С | С | С | С | |
| Высокое | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ||
| Низколеги- рованная сталь |
Низкое | Н | Н | Н | Н | Н | Н | С | С | С | С | С | |
| Высокое | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ||
| Литейная сталь |
Низкое | Н | Н | Н | Н | Н | У | С | С | С | С | С | |
| Высокое | Н | Н | Н | Н | Н | Н | Н | Н | Н | ||||
| Хромирован ная сталь |
Низкое | Н | Н | Н | Н | Н | Н | Н | У | У | С | С | |
| Высокое | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | |||
| Свинец | Низкое | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ||
| Высокое | Н | Н | Н | Н | Н | Н | У | Н | Н | ||||
| Олово | Низкое | Н | Н | Н | Н | Н | Н | Н | Н | ||||
| Высокое | Н | Н | Н | Н | Н | Н | Н | У | Н | ||||
| Медь | Низкое | Н | Н | Н | Н | Н | Н | У | У | С | |||
| Высокое | Н | Н | Н | Н | Н | Н | Н | Н | У | Н | |||
| Нержавеющая сталь |
Низкое | Н | Н | Н | Н | Н | Н | Н | Н | ||||
| Высокое | Н | Н | Н | Н | Н | Н | Н | У | У | У | Н |
В 1 столбце таблицы представлены металлы, которые подвергаются или не подвергаются коррозии с металлами указанными в остальных столбцах таблицы и пропорция соотношения площадей металла, указанного в 1 столбце, к металлам в остальных столбцах таблицы.
Краткое обозначение С, У, Н в таблице означает:
- С – сильная и быстрая коррозия металла;
- У – умеренная коррозия металла;
- Н – Несущественная или ничтожная коррозия металла
Таблица совместимости металлов и сплавов
Опубликовано 2023-01-13
- Таблица электрохимической совместимости металлов
- Способы защиты от контактной коррозии
Гальваническая пара, которую погружают в кислотный или щелочной раствор, будет разрушаться под воздействием кислорода (корродировать). Такой процесс называется гальванической коррозией.
Соединения разных металлов под действием атмосферы подвержены коррозии, однако некоторые пары металлов окисляются намного сильнее и быстрее.
Несовместимые гальванические пары следующие:
- Алюминии и его сплавы.
- Медь, все сплавы на ее основе, золото, платина, олово, никель, хром, нелегированная сталь.

- Магниево-алюминиевые сплавы.
- Цинк и сплавы.
- Никель, хром, серебро, золото, родий, палладий.
- Титан и его сплавы.
- Алюминий и его сплавы.
Нельзя механически соединять детали, у которых разный электрохимический потенциал. Например, латунные детали алюминиевыми заклепками соединять недопустимо. Чтобы выбрать подходящий материал, используйте таблицу совместимости металлов и сплавов.
Таблица электрохимической совместимости металлов
| Материал | Алюминий | Бронза | Дюраль | Латунь | Медь | Никель | Олово | Оловянно-свинцовый сплав (припой ПОС) | Сталь нелегированная (углеродистая) / чугун | Хром | Цинк |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Алюминий | Совм | Не совм | Совм | Не совм | Не совм | Не совм | Не совм | Не совм | Совм | Совм | |
| Бронза | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Дюралюминий | Совм | Не совм | Совм | Не совм | Не совм | Не совм | Не совм | Не совм | Совм | Не совм | Совм |
| Латунь | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Медь | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Никель | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Совм | нет данных | Совм |
| Олово | Не совм | Пайка | Не совм | Пайка | Пайка | Пайка | Совм | Совм | Совм | нет данных | Совм |
| Оловянно-свинцовый сплав (припой ПОС) | Не совм | Пайка | Не совм | Пайка | Пайка | Пайка | Совм | Совм | Совм | нет данных | Совм |
| Сталь нелегированная (углеродистая)/ чугун | Совм | Не совм | Совм | Не совм | Не совм | Совм | Совм | Совм | Совм | Совм | Совм |
| Хром | Не совм | Совм | Не совм | Совм | Совм | нет данных | нет данных | нет данных | Совм | Совм | Совм |
| Цинк | Совм | Не совм | Совм | Не совм | Не совм | Совм | Совм | Совм | Совм | Совм | Совм |
- Совм – совместимые
- Не совм – несовместимые
- П – совместимые при пайке, но несовместимые при непосредственном соприкосновении, так как образуют гальваническую пару
Способы защиты от контактной коррозии
Электрическая совместимость металлов – это возможность создать соединение без гальванической пары (анода и катода). Остановить разрушение металла на 100% нельзя, однако способы защиты от контактной коррозии есть:
Остановить разрушение металла на 100% нельзя, однако способы защиты от контактной коррозии есть:
- Покрасить поверхность металлов в районе стыка.
- Нанесение совместимых покрытий из металла.
- Изоляция соединения от атмосферы.
- Электрическая изоляция места соединения.
- Установка неметаллических прокладок, шайб в болтовых соединениях.
Важно!
На скорость гальванической коррозии влияет площадь поверхности анода и катода. Если большой анод соединить с маленьким анодом, то он будет ржаветь медленнее. У зависимости есть и обратный эффект. Например, болты из нержавейки используйте для крепления алюминия, а не наоборот.
Неправильная компоновка контактных пар – это путь к выходу из строя узлов креплений в трубопроводах или металлоконструкциях.
Оцените нашу статью
[Всего голосов: 3 Рейтинг статьи: 5]
гальваническая и коррозионная совместимость разнообразной коррозии металлов
Гальваническая коррозионная Руководство по коррозии по коррозии / гальваническая совместимость таблицы содержимого
.
 Corrosion Guide
Corrosion Guide Качественная разработка и проектирование требуют понимания совместимости материалов. Гальваническая коррозия (иногда называемая коррозией разнородных металлов) представляет собой процесс, при котором материалы, находящиеся в контакте друг с другом, окисляются или разъедают. Есть три условия, которые должны существовать для возникновения гальванической коррозии. Во-первых, должны присутствовать два электрохимически разнородных металла. Во-вторых, между двумя металлами должен быть электропроводящий путь. И в-третьих, должен существовать проводящий путь для перемещения ионов металла от более анодного металла к более катодному металлу. Если хотя бы одно из этих трех условий не выполняется, гальваническая коррозия не возникает. Часто, когда дизайн требует, чтобы разнородные металлы соприкасались, гальваническая совместимость достигается за счет отделки и покрытия. Выбранная отделка и покрытие облегчают контакт разнородных материалов и защищают основные материалы от коррозии.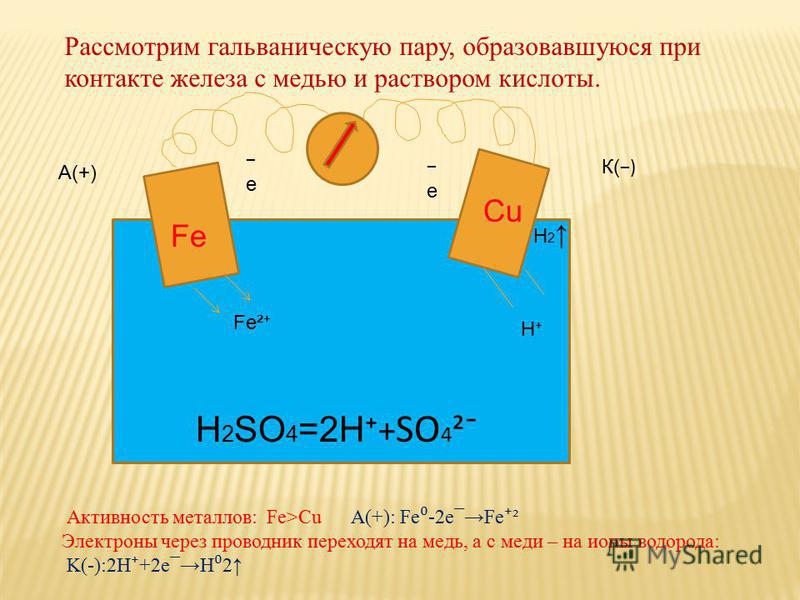
Для суровых условий , например, на открытом воздухе, с высокой влажностью и соленой средой, подпадает под эту категорию. Обычно разница в «анодном индексе» не должна превышать 0,15 В. Например; золото серебро будет иметь допустимую разницу в 0,15 В.
Для нормальных условий , таких как хранение на складах или в условиях без контроля температуры и влажности. Обычно разница в «анодном индексе» не должна превышать 0,25 В.
Для контролируемых сред , таких как температура и влажность, допускается напряжение 0,50 В. Следует соблюдать осторожность при выборе этого применения, так как влажность и температура могут различаться в зависимости от региона.
АНОДНЫЙ ИНДЕКС (V)
Золото, сплошное и с покрытием, золото-платиновый сплав
0,00
Покрытие родием на посеребренной меди
0,05
Серебро, сплошное или с покрытием; монель металл. Сплавы с высоким содержанием никеля и меди
Сплавы с высоким содержанием никеля и меди
0,15
Никель, сплошной или с покрытием, титан и сплавы, монель
0,30
Медь сплошная или с покрытием; низкие латуни или бронзы; серебряный припой; немецкие серебристые сплавы с высоким содержанием меди и никеля; никель-хромовые сплавы
0,35
Латунь и бронза
0,40
Высококачественные латуни и бронзы
0,45
Коррозионностойкие стали с содержанием 18 % хрома
0,50
Хромированный; луженые; Коррозионностойкие стали с содержанием 12 % хрома
0,60
Белая жесть; оловянно-свинцовый припой
0,65
Свинец, сплошной или с покрытием; сплавы с высоким содержанием свинца
0,70
Алюминий, деформируемые сплавы серии 2000
0,75
Железо кованое, серое или ковкое, углеродистая и низколегированная сталь
0,85
Алюминий, деформируемые сплавы, кроме алюминия серии 2000, литые сплавы типа кремния
0,90
Алюминий, литые сплавы, кроме кремния, кадмий, с покрытием и хромат
0,95
Горячеоцинкованная пластина; оцинкованная сталь
1,20
Цинк, кованый; литейные сплавы на основе цинка; оцинкованный
1,25
Магний и сплавы на его основе, литые или кованые
1,75
Бериллий
1,85
Другие документы, представляющие интерес:
- Покрытия, устойчивые к коррозии
- Гальваническая коррозия
Знакомство с гальванической серией: Galvanic Compatibili
Гальваническая серия играет жизненно важную роль в определении и предотвращении коррозии.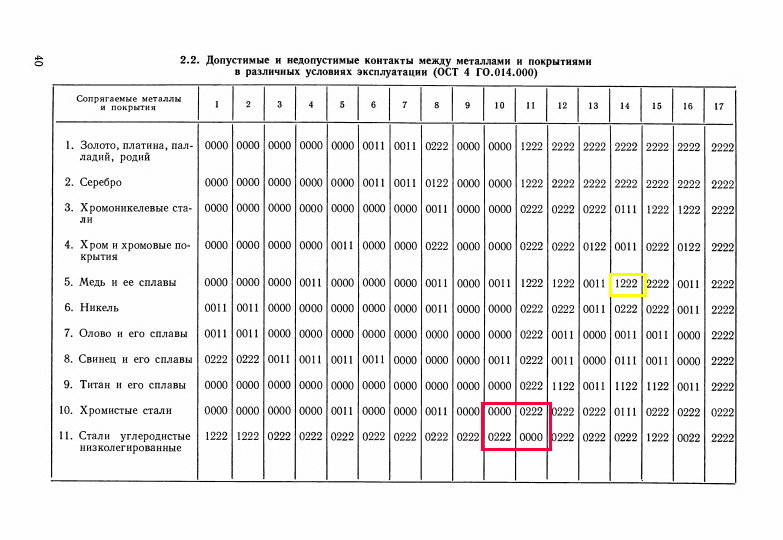 Эта серия, также известная как «серия электропотенциалов», идентифицирует полуметаллическое и металлическое благородство. По сути, гальваническая коррозия возникает, когда два разных металла, погруженные в электролит, соединяются вместе. В этом случае основание или металл с меньшим благородством будут подвергаться коррозии. Таким образом, скорость коррозии можно определить на основе благородства металлов и электролита, воздействию которого они подвергаются.
Эта серия, также известная как «серия электропотенциалов», идентифицирует полуметаллическое и металлическое благородство. По сути, гальваническая коррозия возникает, когда два разных металла, погруженные в электролит, соединяются вместе. В этом случае основание или металл с меньшим благородством будут подвергаться коррозии. Таким образом, скорость коррозии можно определить на основе благородства металлов и электролита, воздействию которого они подвергаются.
Реклама
Различные материалы могут реагировать друг с другом благодаря наличию катализатора или электролита. Почти во всех случаях реакция не столь значительна. Однако, когда неподходящие материалы комбинируются и подвергаются воздействию воды и других типов электролитов, последствия могут быть очень вредными. В условиях низкой влажности гальваническая коррозия не представляет серьезной проблемы. С другой стороны, в приложениях, подверженных влажным или влажным условиям, гальваническая коррозия может представлять серьезную угрозу. (Подробнее читайте в статье «10 главных угроз коррозии».)
(Подробнее читайте в статье «10 главных угроз коррозии».)
Соотношения в серии для гальваники могут быть очень полезным руководством для выбора металлов для соединения. В этой серии можно эффективно выбирать материалы, чтобы можно было выбрать металлы с наименьшей склонностью к гальванической реакции. В тех случаях, когда гальваническое взаимодействие наиболее вероятно, потребуется определенный уровень защиты, чтобы уменьшить возможные потенциальные реакции.
Реклама
Как правило, металлы, расположенные дальше друг от друга в ряду, с наибольшей вероятностью подвергаются гальванической коррозии, которую следует остановить путем правильного выбора и конструкции. Металлы, которые находятся дальше друг от друга, имеют самую высокую скорость коррозии при объединении. Зная соотношения металлов в ряду, можно определить гальваническую совместимость, предотвратив возможное вредное воздействие гальванической коррозии.
Диаграмма 1. Гальваническая серия / гальваническая таблица.
Диаграмма 1. Гальваническая серия / гальваническая таблица. ( Источник: Tugsatydin, CC BY-SA 4.0, через Wikimedia Commons)
Реклама
На приведенной выше диаграмме показаны потенциалы коррозии в проточной морской воде при температуре окружающей среды. Незаштрихованные символы показывают диапазоны, демонстрируемые нержавеющими сталями в кислой воде, которая может существовать в щелях или в стоячей, низкоскоростной или плохо аэрированной воде. Более благородные материалы слева имеют тенденцию быть катодными и, следовательно, защищенными; те, что справа, менее благородны и склонны к анодизму. Следовательно, они будут подвергаться коррозии в гальванической паре.
Таблица гальванических данных Чтобы лучше понять гальванический ряд, очень важно ознакомиться с таблицей гальванических данных.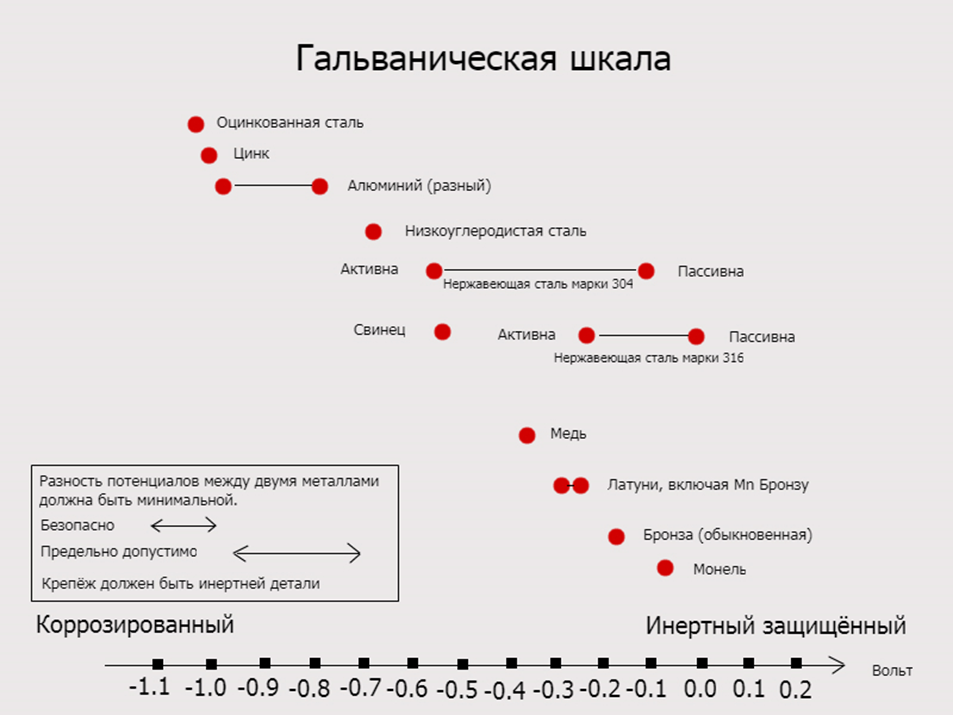 Что такое гальванический стол?
Что такое гальванический стол?
В этой таблице активные металлы перечислены в порядке их относительной активности в среде электролита. Таблица начинается с наиболее активного или анодного металла в ряду и перечисляет металлы до катодного или наименее активного металла. Список начинается с наиболее активных металлов, которые наиболее подвержены коррозии, таких как магний, сплавы магния, алюминия и цинка. Металлы, которые находятся последними в списке, считаются катодными и менее всего подвержены коррозии.
Гальванический ряд применяется к определенному раствору. В паре металлы, находящиеся в верхней части списка, считаются анодами и будут подвергаться коррозии в большей степени, чем окружающая среда. Ключом к предотвращению возможных разрушительных реакций, вызванных комбинацией металлов, является использование материалов, которые находятся рядом друг с другом в гальванической таблице. Таким образом можно предотвратить гальваническую коррозию. Чтобы добиться идеального сочетания материалов, необходимо очень тщательно изучить гальваническую совместимость.
Бывают случаи, когда конкретная конструкция требует сочетания различных металлов. В таких случаях гальваническая совместимость обеспечивается за счет покрытия и отделки. Выбранные методы нанесения покрытия и отделки облегчают контакт разнородных металлов, обеспечивая при этом защиту основного металла от коррозии. (Подробнее о гальваническом покрытии см. в разделе «Как металлические покрытия защищают металлы от коррозии».)
Например, в суровых условиях, таких как соленая среда, зоны с высокой влажностью и на открытом воздухе, требуется не более 0,15 В в зависимости от анодного индекса. Например, такие металлы, как никель и серебро, дают разницу в 0,15 В, что вполне приемлемо. Двигаясь вперед, в стандартных условиях, таких как склады, хранилища и другие среды с регулируемой температурой и влажностью, требуемая разница анодного показателя между металлами не должна превышать 0,25 В, а в условиях, где влажность и температура могут жестко контролироваться, разница составляет 0,50. вольт можно терпеть. Но тогда следует соблюдать крайнюю осторожность для различных применений, поскольку температура, влажность и другие факторы различаются в каждой области. (Подробное обсуждение см. в статье Временная защита от коррозии при хранении, транспортировке и обращении.)
вольт можно терпеть. Но тогда следует соблюдать крайнюю осторожность для различных применений, поскольку температура, влажность и другие факторы различаются в каждой области. (Подробное обсуждение см. в статье Временная защита от коррозии при хранении, транспортировке и обращении.)
Чтобы предотвратить возникновение гальванической коррозии в различных местах соединения металлов и материалов, следует учитывать гальваническую совместимость путем определения допустимой разницы анодного показателя материалов.
Соблюдая гальваническую совместимость, два металла, которые не имеют необходимого анодного индекса, могут быть надлежащим образом защищены. Металлы, которые перечислены дальше друг от друга в гальванической таблице, должны быть защищены, если они будут использоваться вместе. Следует применять определенные меры для предотвращения контакта двух разных металлов. Этот вид защиты может быть обеспечен с помощью различных средств, таких как:
- Герметизация: Этот метод распространяется на все водонепроницаемые зоны.

- Защитный анод: Нанесение защитного покрытия на катодный элемент, потенциал которого аналогичен потенциалу анодной области, предотвратит гальваническую коррозию.
- Сопротивление: Повышение сопротивления с помощью покрытия, металлизации и других методов может помочь повысить защиту от электрических цепей.
Правило во избежание гальванической коррозии заключается в том, чтобы держать анодные области вдали от сравнительно катодных областей.
Гальваническая коррозия Как обсуждалось ранее, гальваническая коррозия возникает, когда два разных металла вступают в контакт в электролите, обладающем электропроводностью, таком как земля или дождевая вода. При этом типе коррозии атомы металла окисляются и оставляют после себя объемный металл после обмена или передачи одного или нескольких электронов. Область, где атомы металла сбрасывают электроны, называется анодом; область, где транспортируются электроны, является катодом.
Рис. 1. Гальваническая коррозия из-за разного анодного индекса между болтами и пластиной. (Источник D3j4vu в английской Википедии, CC BY-SA 3.0, через Wikimedia Commons)
В гальваническом ряду металлы перечислены в соответствии с их электрическим потенциалом в электролите, таком как морская вода. Как уже упоминалось, анодные металлы будут подвергаться коррозии с большей скоростью, чем пассивные или катодные металлы.
Чрезвычайно важно учитывать потенциал гальванической коррозии при выборе металлов для различных применений, таких как отделка, обшивка, крепеж и многое другое. (Тема нанесения покрытий на крепеж подробно обсуждается в статье «Практика нанесения покрытий на крепеж высокого давления в условиях пожара: выступление Иэна МакМой».)
Рис. 2. Различные металлические детали с различной гальванической совместимостью.
Чтобы свести к минимуму гальваническую коррозию, очень важно использовать аналогичные металлы. В тех случаях, когда это невозможно, следует предусмотреть достаточную защиту, чтобы не допустить, чтобы металлы, которые не совпадают, образовывали электрическое соединение с водой или электролитом. (Конкретный пример морской коррозии обсуждается в статье «Как остановить морскую коррозию за 3 шага».) Кроме того, предотвращение контакта крошечных анодов с большими катодами может помочь снизить вероятность гальванической коррозии.
В тех случаях, когда это невозможно, следует предусмотреть достаточную защиту, чтобы не допустить, чтобы металлы, которые не совпадают, образовывали электрическое соединение с водой или электролитом. (Конкретный пример морской коррозии обсуждается в статье «Как остановить морскую коррозию за 3 шага».) Кроме того, предотвращение контакта крошечных анодов с большими катодами может помочь снизить вероятность гальванической коррозии.
Скорость коррозии зависит от отношения анода к поверхности катода. Если площадь катода больше площади анода, концентрация электронов выше; результатом будет гальваническая коррозия с более высокой скоростью. В обратном случае, например, когда площадь катода меньше по сравнению с поверхностью анода, коррозия будет происходить медленнее.
Защитные покрытия для предотвращения гальванической коррозии
Для обеспечения гальванической защиты обычно используется защитное покрытие. Это дает пассивному металлу или основе эффективное покрытие, которое является более анодным по сравнению с основой.