виды, схемы монтажа и соединения батарей
Главная функция системы центрального отопления – эффективный обогрев помещения. Элементы этой системы, в частности, радиаторы, должны быть подключены и расположены таким образом, чтобы их теплоотдача была максимальной. В схеме присоединения батарей должны учитыватсяь такие нюансы, как их общее количество, длина теплотрассы, особенности расположения труб и т.д. Рассмотрим, какие варианты чаще применяются в частных домах. В первую очередь, это однотрубный и двухтрубный способы подключения радиаторов отопления.
Содержание
1 Однотрубная система
2 Двухтрубная система
3 Схемы подключения батарей
3.1 Боковое одностороннее подключение радиаторов
3.2 Диагональное подключение
3.3 Нижнее подключение
3.4 Подключение Тихельмана
4 Рекомендации по выбору места для установки радиаторов
Однотрубная система
Схема однотрубной системы отопления. Нажмите на фото для увеличения.
Нажмите на фото для увеличения.
Такая схема подключения предполагает соединение всех батарей отопления последовательно при помощи одной трубы. Она подводится от котла к первому нагревательному элементу, затем от него идет ко второму, от второго – к третьему и т.д. Усовершенствованный вариант однотрубной схемы – цельная труба для подведения горячей воды, батареи к которой присоединяются при помощи стояков подачи и «обратки». Этот вариант делает возможной установку термовентиля непосредственно перед радиатором. Основная функция термовентилей – прекращение подведения горячей воды к батарее, когда будет достигнут установленный уровень температуры воздуха в помещении. В первом варианте однотрубной схемы невозможно «заблокировать» один из нагревательных элементов без прекращения подачи теплоносителя и в другие, следующие за ним.
Явное преимущество такого способа организации обогрева помещения – его простота и экономия материалов, так как соединительных труб много не понадобится. Отрицательный момент – существенная разница в нагреве ближнего к котлу и самого удаленного от него радиатора.
Если циркуляция теплоносителя в системе естественная, общая протяженность последней не может быть большой. Решить проблему поможет установка насоса с высокой производительностью.
Если в здании несколько этажей, то однотрубный метод работает следующим образом: по одной трубе – прямому стояку – горячая вода подается на верхний этаж, а затем опускается вниз, проходя через каждую из последовательно подключенных батарей. Здесь также есть свой минус: нагревательный элемент на первом этаже будет намного холоднее, чем на верхнем, и уменьшить эту разницу не представляется возможным.
Двухтрубная система
Данная схема подключения представляет собой несколько радиаторов отопления, соединенных параллельно. При этом подведение теплоносителя происходит по одной трубе, а отвод – по другой. Таким способом чаще всего организуется обогрев комнат в частных домах и загородных коттеджах. Степень прогрева всех батарей примерно одинаков, и изменять ее можно при помощи терморегулятора, установленного на прямом стояке.
[nggallery id=8]
Схемы подключения батарей
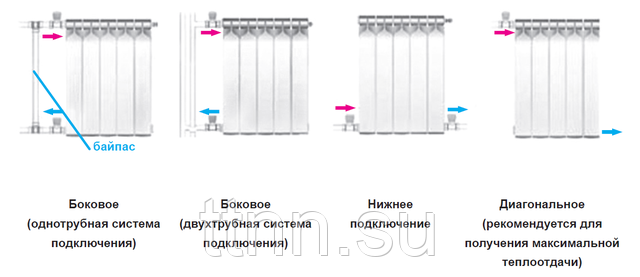
Существуют следующие виды подключения радиаторов к центральной системе отопления:
- боковое одностороннее;
- диагональное;
- нижнее;
- попутно перехлестывающее, или подключение Тихельмана.
Прежде чем мы перейдем к подробному рассмотрению каждого вида, опишем, как в общем виде выглядит и какие элементы включает радиатор, присоединенный к прямому и обратному стоякам. На рисунке ниже это представлено довольно наглядно. Необходимо пояснить лишь то, что такое байпас. Байпас – это отрезок трубы, меньшей по диаметру, чем остальные. Он соединяет подачу и «обратку» и устанавливается в том случае, когда в однотрубной системе присутствует терморегулятор.
Боковое одностороннее подключение радиаторов
Такая система подключения предполагает боковое одностороннее присоединение радиаторов отопления к прямому и обратному стояку, то есть обе трубы подключаются к одной и той же секции (сверху и снизу). Рекомендуется присоединять подачу к верхней части батареи, а «обратку» – к нижней. Двухтрубная схема, в которой подача горячей воды в систему радиаторного отопления происходит снизу, характеризуется более низкой (примерно на 7%) мощностью.
Рекомендуется присоединять подачу к верхней части батареи, а «обратку» – к нижней. Двухтрубная схема, в которой подача горячей воды в систему радиаторного отопления происходит снизу, характеризуется более низкой (примерно на 7%) мощностью.
Боковое одностороннее подключение обеспечивает максимальный прогрев батарей с большим количеством секций или равномерный прогрев всех радиаторов в высотных зданиях, где эти элементы соединяются параллельно.
Диагональное подключение
Диагональная схема подключения радиатора к системе отопления предполагает присоединение стояков подачи и «обратки» с разных сторон: прямую трубу подводят к верхней части нагревательного элемента, а обратную – к нижней. Рекомендуется именно такой порядок, иначе эффективность обогрева помещения снизится по меньшей мере на 10%.
Диагональная схема соединения батарей – это оптимальный подход к организации системы отопления, состоящей из большого количества радиаторов. Горячая вода равномерно распределяется по всему пространству внутри батареи. Теплопотери при этом составляют не более 2%.
Горячая вода равномерно распределяется по всему пространству внутри батареи. Теплопотери при этом составляют не более 2%.
[nggallery id=9]
Нижнее подключение
Такая схема подключения используется, когда все трубы системы отопления спрятаны под пол. Стояки подвода и отвода теплоносителя присоединяются к нижней части крайних секций нагревательного элемента. Теплопотери при таком способе подключения могут достигать 15%, так как верхняя часть батареи прогревается неравномерно.
Подключение Тихельмана
Система Тихельмана. Нажмите на фото для увеличения.
Схема соединения Тихельмана, или попутно перехлестывающее подключение радиаторов отопления – это та же двухтрубная система, только с установкой сужающих устройств на участках подачи и «обратки». Рассмотрим конкретный пример. Труба подачи от котла имеет диаметр 50 мм. В нее врезается подача на первый радиатор, диаметром 20 мм. После перехода следует отрезок трубы диаметром 40 мм. Далее – 20-милиметровый отвод на вторую батарею.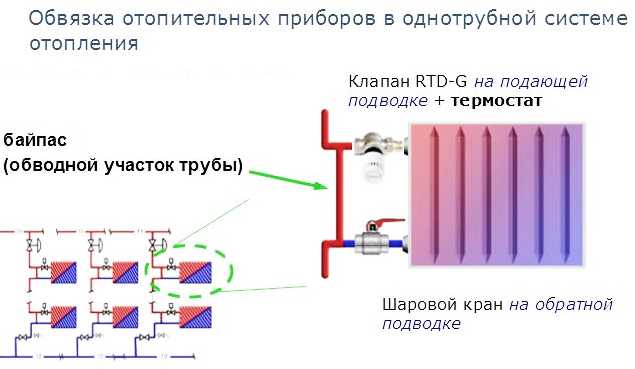 После второго радиатора диаметр стояка меняется на 32 мм. Далее – еще один отвод 20 мм на нагревательный элемент. Диаметр стояка после третьего радиатора – 25 мм. Далее – последний отвод 20 мм и последняя батарея.
После второго радиатора диаметр стояка меняется на 32 мм. Далее – еще один отвод 20 мм на нагревательный элемент. Диаметр стояка после третьего радиатора – 25 мм. Далее – последний отвод 20 мм и последняя батарея.
«Обратка» собирается по зеркальной схеме: первым подключается к стояку отвода при помощи трубы самого маленького диаметра первый радиатор, последним – последний элемент с диаметром стояка 50 мм.
Таким образом, даже в теплотрассах большой протяженности (большие особняки, гаражи, склады, ангары и т.д.) обеспечивается равномерный прогрев всех радиаторов с минимальными теплопотерями.
Рекомендации по выбору места для установки радиаторов
Правильная и неправильная установка радиатора. Нажмите на фото для увеличения.
Основная функция батарей – не только обогревать помещение, но и препятствовать распространению в нем холодного воздуха. В связи с этим они чаще всего устанавливаются под подоконником. Следует выдержать определенное расстояние между батареей и стеной, а также батареей и полом: 3-5 см и 10 см соответственно.
Батарея не должна находиться полностью под подоконником, то есть если он очень широкий, нагревательный элемент следует выдвинуть. Если жар от него слишком сильный, целесообразно использовать экран, который будет распределять теплый воздух более равномерно.
Очень важно учитывать и то, как в целом спроектировано отопление. Если в нем предусмотрена установка электрического насоса, сложностей обычно не возникает. Другое дело – трассы с естественной циркуляцией теплоносителя, когда горячая вода поднимается вверх, выталкивая холодную. Существенное преимущество таких систем в том, что они энергонезависимы, то есть работают стабильно даже при перебоях с подачей электроэнергии. Однако проектировать такую схему должен исключительно специалист, так как нужно проанализировать и общую протяженность теплотрассы, и специфику ее прокладки, и число отопительных элементов, и количество секций в них. Если вы желаете обеспечить максимально эффективный обогрев своего дома, следует учитывать все нюансы.
- Автор: admin
- Распечатать
Оцените статью:
(0 голосов, среднее: 0 из 5)
Поделитесь с друзьями!
схема подключения радиаторов, как подсоединить правильно, как подключать
Содержание:
Виды отопительных систем
Однотрубное отопление
Двухтрубное отопление
Расположение радиаторов
Диагональное подключение
Одностороннее подключение
Нижнее подключение
Заключение
Видео
Эффективность работы отопительной системы зависит от множества факторов, одним из которых является схема подключения батарей. Конечно, характеристики самих батарей тоже оказывают серьезное влияние на работу отопления, но правильная установка позволит им полностью реализоваться. О том, как правильно подключать радиаторы отопления в квартире, и пойдет речь в данной статье.
О том, как правильно подключать радиаторы отопления в квартире, и пойдет речь в данной статье.
Виды отопительных систем
Перед тем, как подсоединить батарею отопления, нужно разобраться с конфигурацией отопительной системы – этот фактор очень сильно влияет на теплоотдачу всех батарей. Существует два основных вида отопительных систем – двухтрубные и однотрубные. О каждом из них стоит поговорить подробнее.
Однотрубное отопление
Ключевым недостатком однотрубной схемы является неравномерный прогрев установленных радиаторов и невозможность контроля их теплоотдачи. Установка регулятора на одну батарею приводит к регулировке дальнейшего участка контура. Расположенные далеко от котла батареи получают гораздо меньше тепла – оно попросту остается на предыдущих приборах. Даже если точно знать, как правильно подключить батарею, равномерной теплоотдачи в однотрубной системе достичь не выйдет.
Установка регулятора на одну батарею приводит к регулировке дальнейшего участка контура. Расположенные далеко от котла батареи получают гораздо меньше тепла – оно попросту остается на предыдущих приборах. Даже если точно знать, как правильно подключить батарею, равномерной теплоотдачи в однотрубной системе достичь не выйдет.
Двухтрубное отопление
Отличительная особенность двухтрубной разводки – наличие двух контуров, один из которых предназначен для подачи разогретого теплоносителя к радиаторам, а второй необходимо для возврата остывшего теплоносителя в котел. Двухтрубная конструкция дает возможность подключать радиаторы параллельно, в результате чего каждый из них получает теплоноситель одинаковой температуры.
Благодаря параллельному подключению удается достичь независимости каждого радиатора, потому на них можно устанавливать отдельные терморегуляторы для настройки теплоотдачи. Единственным недостатком такой разводки является высокая себестоимость – для обустройства отопления требуется в два раза больше материалов. Впрочем, эти затраты в дальнейшем с лихвой окупаются.
Впрочем, эти затраты в дальнейшем с лихвой окупаются.
Расположение радиаторов
В подавляющем большинстве случаев радиаторы устанавливаются под окнами, и такое расположение вполне оправдано. Дело в том, что от окон всегда идет поток холодного воздуха – а поднимающиеся от батареи разогретые воздушные массы препятствуют их попаданию в помещение. Кроме того, нагретый воздух предотвращает появление конденсата на стеклах.
Чтобы точно знать, как правильно подключить батарею отопления в квартире, нужно учесть следующие правила и следовать им при проектировании и монтаже отопительной системы:
- Нормальное предотвращение попадания холода от окон и образования конденсата на них возможно только в том случае, если размеры радиатора занимают хотя бы 70% ширины оконного проема. Этот фактор нужно учесть еще на этапе выбора радиаторов.
- Отопительные батареи рекомендуется устанавливать на высоте около 10 см от уровня пола.
 Большое отклонение от этого показателя приведет к недостаточному прогреву нижнего уровня помещения или же спровоцирует сложности при уборке. Расстояние до подоконника должно составлять около 10-12 см – такое значение позволяет воздух свободно огибать препятствие и полноценно прогревать окно.
Большое отклонение от этого показателя приведет к недостаточному прогреву нижнего уровня помещения или же спровоцирует сложности при уборке. Расстояние до подоконника должно составлять около 10-12 см – такое значение позволяет воздух свободно огибать препятствие и полноценно прогревать окно. - Расстояние между батареей и стеной должно составлять около 3-5 см. При таком размещении в пространстве за батареей свободно проходят разогретые воздушные массы, в результате чего эффективность обогрева помещения улучшается.
Способы подключения радиаторов
Существует несколько вариантов подключения радиаторов, но все они делятся на две больших категории – боковые и нижние. Нижнее подключение может выполняться единственным способом, который выглядит очень просто: есть два патрубка, один из которых подводится ко входу радиатора, а второй – к выходу. Схема подключения радиатора отопления в квартире всегда описывается в приложенной к нему документации.
Боковая схема подключения батарей в квартире имеет большее количество вариантов, среди которых:
- Диагональное подключение;
- Одностороннее подключение;
- Нижнее (седельное) подключение.

Каждому варианту стоит уделить особое внимание.
Диагональное подключение
Диагональная схема подключения батарей отопления в квартире считается самой эффективной, поэтому по возможности стоит отдать предпочтение именно ей. Большинство производителей отопительных приборов проверяют свою продукцию именно при диагональном подключении, и в соответствии с полученной информацией вносят данные в технический паспорт радиаторов.
При диагональном подключении разогретый теплоноситель запускается через верхний вход на одной стороне батареи. Полностью пройдя через радиатор, остывший теплоноситель направляется к выходному патрубку, который расположен с другой стороны батареи в нижней ее части. В результате диагональное подключение радиатора в квартире обеспечивает максимальное прохождение теплоносителя через внутренние полости отопительного прибора.
Одностороннее подключение
Данная схема подключения радиаторов полностью оправдывает свое название – трубы подачи и обратки подводятся к прибору с одной стороны, но на разных уровнях. Такой вариант наиболее актуален в квартирах, где стояк находится сбоку от радиатора. В остальных ситуациях одностороннее подключение будет не очень удобным в обустройстве.
Такой вариант наиболее актуален в квартирах, где стояк находится сбоку от радиатора. В остальных ситуациях одностороннее подключение будет не очень удобным в обустройстве.
Эффективность одностороннего подключения достаточно высока и лишь немного уступает диагональному. Это утверждение верно в том случае, если количество секций не превышает 10 – слишком длинная батарея не будет прогреваться полностью, поэтому теплоотдача снизится. В панельных, алюминиевых и биметаллических радиаторах эту проблему можно решить при помощи удлинителей потока, которые позволяют теплоносителю пройти через большую часть радиатора.
Нижнее подключение
Данный вариант подключения отличается минимальной эффективностью – теплоотдача радиаторов при его использовании снижается в среднем на 12%. Впрочем, в некоторых ситуациях эти потери будут оправданными, поскольку нижнее подключение позволяет установить трубы максимально незаметно, тем самым улучшая интерьер помещения.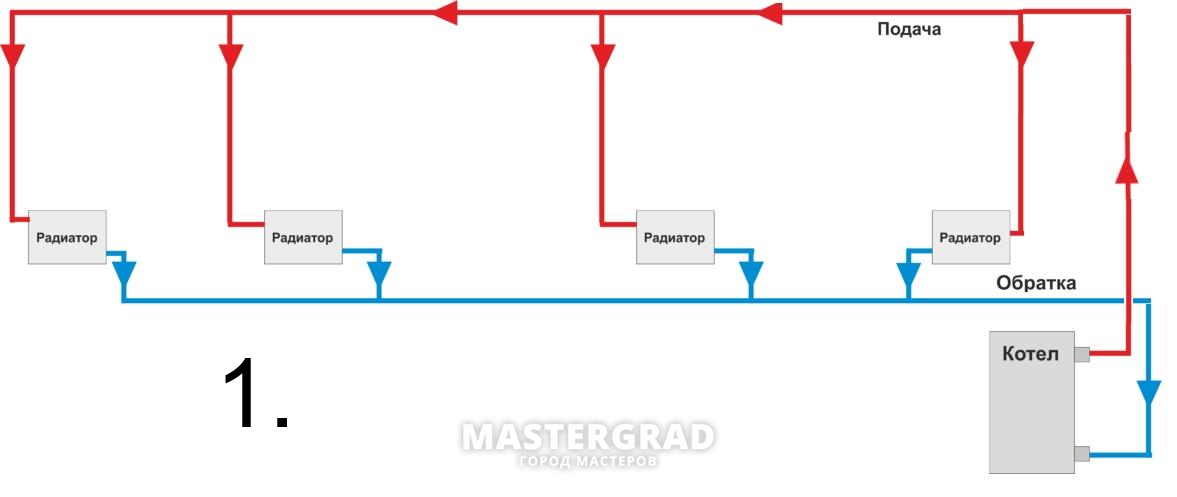 А теплопотери можно компенсировать более мощным радиатором.
А теплопотери можно компенсировать более мощным радиатором.
В гравитационных отопительных системах подключение седельного типа использовать не рекомендуется в силу его недостаточной эффективности. Если же в отоплении имеется насос, то система будет работать достаточно хорошо, и теплоотдача отопительных приборов повысится. Отчасти это связано с малоизученным вихревым характером потока теплоносителя, при котором теплоотдача характеризуется как наиболее интенсивная.
Заключение
Данная статья подробно отвечает на вопрос о том, как правильно подсоединить батареи отопления в квартире. Есть несколько распространенных схем подключения, каждая из которых имеет свои особенности и подходит для конкретной ситуации.
Как работает батарея – Любопытно
Представьте себе мир без батареек. Все те портативные устройства, от которых мы так зависим, были бы такими ограниченными! Мы смогли бы донести наши ноутбуки и телефоны только до предела досягаемости их кабелей, что сделало бы это новое работающее приложение, которое вы только что загрузили на свой телефон, довольно бесполезным.
Все те портативные устройства, от которых мы так зависим, были бы такими ограниченными! Мы смогли бы донести наши ноутбуки и телефоны только до предела досягаемости их кабелей, что сделало бы это новое работающее приложение, которое вы только что загрузили на свой телефон, довольно бесполезным.
К счастью, у нас есть батарейки. Еще в 150 г. до н.э. в Месопотамии парфянская культура использовала устройство, известное как багдадская батарея, сделанное из медных и железных электродов с уксусом или лимонной кислотой. Археологи считают, что на самом деле это не были батареи, а использовались в основном для религиозных церемоний.
Изобретение батареи в том виде, в каком мы ее знаем, приписывают итальянскому ученому Алессандро Вольта, который собрал первую батарею, чтобы доказать точку зрения другого итальянского ученого, Луиджи Гальвани. В 1780 году Гальвани показал, что лапки лягушек, подвешенных на железных или латунных крючках, будут дергаться при прикосновении к ним зондом из какого-либо другого металла.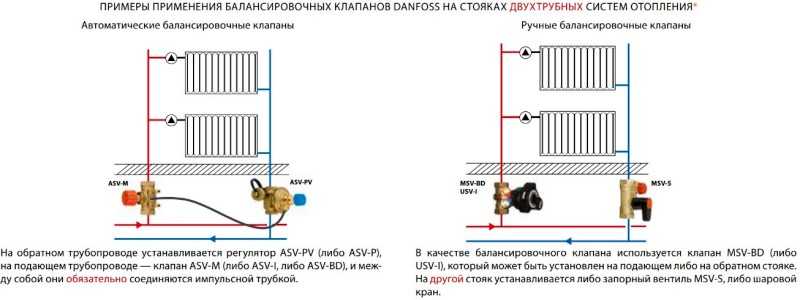 Он считал, что это было вызвано электричеством из тканей лягушек, и называл это «животным электричеством».
Он считал, что это было вызвано электричеством из тканей лягушек, и называл это «животным электричеством».
Вольта, поначалу впечатленный открытиями Гальвани, пришел к выводу, что электрический ток исходит из двух разных типов металла (крючков, на которых висят лягушки, и другого металла зонда) и просто передается через них, а не через них. из тканей лягушек. Он экспериментировал со стопками слоев серебра и цинка, перемежаемых слоями ткани или бумаги, пропитанными соленой водой, и обнаружил, что электрический ток действительно протекал по проводу, прикрепленному к обоим концам стопки.
Батарея Алессандро Вольта: груда цинковых и серебряных листов с вкраплениями ткани или бумаги, пропитанной соленой водой. Представьте, что вы используете это для питания вашего телефона. Источник изображения: Луиджи Кьеза / Wikimedia Commons.
Представьте, что вы используете это для питания вашего телефона. Источник изображения: Луиджи Кьеза / Wikimedia Commons.Вольта также обнаружил, что, используя различные металлы в куче, можно увеличить величину напряжения. Он описал свои открытия в письме Джозефу Бэнксу, тогдашнему президенту Лондонского королевского общества, в 1800 году. ‘ (мера электрического потенциала) названа в его честь.
Я сам, если не считать шуток, поражаюсь тому, как мои старые и новые открытия… чистого и простого электричества, вызываемого контактом металлов, могли вызвать такой ажиотаж.Алессандро Вольта
Так что же именно происходило с этими слоями цинка и серебра и с дергающимися лягушачьими лапками?
Химия батареи
Батарея представляет собой устройство, которое накапливает химическую энергию и преобразует ее в электричество. Это известно как электрохимия, а система, которая лежит в основе батареи, называется электрохимической ячейкой. Батарея может состоять из одного или нескольких (как в исходной куче Вольты) электрохимических элементов. Каждая электрохимическая ячейка состоит из двух электродов, разделенных электролитом.
Батарея может состоять из одного или нескольких (как в исходной куче Вольты) электрохимических элементов. Каждая электрохимическая ячейка состоит из двух электродов, разделенных электролитом.
Так откуда электрохимический элемент получает электричество? Чтобы ответить на этот вопрос, нам нужно знать, что такое электричество. Проще говоря, электричество — это тип энергии, производимый потоком электронов. В электрохимической ячейке электроны образуются в результате химической реакции, которая происходит на одном электроде (подробнее об электродах ниже!), а затем перетекают на другой электрод, где они расходуются. Чтобы понять это правильно, нам нужно поближе взглянуть на компоненты клетки и на то, как они собираются вместе.
Электроды
Чтобы создать поток электронов, вам нужно где-то, чтобы электроны текли из , и куда-то, чтобы электроны текли в . Это электроды клетки. Электроны текут от одного электрода, называемого анодом (или отрицательным электродом), к другому электроду, называемому катодом (положительный электрод). Как правило, это различные типы металлов или других химических соединений.
Как правило, это различные типы металлов или других химических соединений.
В батарее Вольта анодом был цинк, от которого электроны текли по проводу (при подключении) к серебру, которое было катодом батареи. Он сложил множество этих элементов вместе, чтобы сделать общую кучу и поднять напряжение.
Но откуда анод получает все эти электроны? И почему они так счастливы, что их весело отправляют на катод? Все сводится к химии, которая происходит внутри клетки.
Происходит несколько химических реакций, которые нам нужно понять. На аноде электрод вступает в реакцию с электролитом, в результате которой образуются электроны. Эти электроны накапливаются на аноде. Тем временем на катоде одновременно происходит другая химическая реакция, которая позволяет этому электроду принимать электроны.
Технический химический термин для реакции, включающей обмен электронами, представляет собой реакцию восстановления-окисления, чаще называемую окислительно-восстановительной реакцией. Всю реакцию можно разделить на две полуреакции, а в случае электрохимической ячейки одна полуреакция происходит на аноде, другая на катоде. Восстановление — это присоединение электронов, и это то, что происходит на катоде; мы говорим, что катод восстанавливается в ходе реакции. Окисление — это потеря электронов, поэтому мы говорим, что анод окисляется.
Всю реакцию можно разделить на две полуреакции, а в случае электрохимической ячейки одна полуреакция происходит на аноде, другая на катоде. Восстановление — это присоединение электронов, и это то, что происходит на катоде; мы говорим, что катод восстанавливается в ходе реакции. Окисление — это потеря электронов, поэтому мы говорим, что анод окисляется.
Каждая из этих реакций имеет определенный стандартный потенциал. Думайте об этой характеристике как о способности/эффективности реакции либо производить, либо поглощать электроны — ее сила в перетягивании каната электронами.
- Стандартные потенциалы для полуреакций
Ниже приведен список полуреакций, которые включают высвобождение электронов либо из чистого элемента, либо из химического соединения. Рядом с реакцией указано число (E 0 ), которое сравнивает силу электрохимического потенциала реакции с силой готовности водорода расстаться со своим электроном (если вы посмотрите вниз по списку, вы увидите, что водородная полуреакция имеет Е 0 нуля).
 E 0 измеряется в вольтах.
E 0 измеряется в вольтах.Причина, по которой этот список настолько интересен, заключается в том, что если вы выберете две реакции из списка и объедините их для создания электрохимической ячейки, значения E 0 подскажут вам, каким образом будет протекать общая реакция: реакция с более отрицательное значение E 0 пожертвует свои электроны другой реакции, и это определяет анод и катод вашей ячейки. Разница между двумя значениями E 0 говорит вам об электрохимическом потенциале вашей ячейки, который в основном является напряжением ячейки.
Итак, если вы возьмете литий и фтор и сумеете соединить их, чтобы сделать элемент батареи, вы получите максимальное напряжение, теоретически достижимое для гальванического элемента. Этот список также объясняет, почему в куче Вольта цинк был анодом, а серебро катодом: полуреакция цинка имеет более низкое (более отрицательное) значение E 0 (-0,7618), чем полуреакция серебра (0,7996).
 .
.Стандартные потенциалы полуреакций восстановления
(по отношению к стандартному водородному электроду при 25°C)
В° (В) Li + (водный) + e − Li(s) –3,040 Be 2+ (водн.) + 2e − Be(s) –1,99 Al 3+ (водн.) + 3e − Al(s) –1,676 Zn 2+ (водный) + 2e − Zn(s) –0,7618 Ag 2 S(s) + 2e − 2Ag(s) + S 2− (водн.) –0,71 Fe 2+ (водн.) + 2e − Fe(s) –0,44 Cr 3+ (водн.) + e − Cr 2+ (водн.) –0,424 Cd 2+ (водн.) + 2e − Cd(s) –0,4030 PbSO 4 (т) + 2e − Pb(т) + SO 4 2− (водн.  )
)–0,356 Ni 2+ (водн.) + 2e − Ni(s) –0,257 2SO 4 2− (водн.) + 4H + (водн.) + 2e − S 2 O 6 − 290940048 (водн.) + 2H 2 O(л) –0,25 Sn 2+ (водн.) + 2e − Sn(s) −0,14 2H + (водн.) + 2e − H 2 (г) 0 Sn 4+ (водн.) + 2e − Sn 2+ (водн.) 0,154 Cu 2+ (водн.) + e − Cu + (водный) 0,159 AgCl(s) + e − Ag(s) + Cl − (водн.) 0,2223 Cu 2+ (водн.) + 2e − Cu(s) 0,3419 O 2 (г) + 2H 2 O(ж) + 4e − 4OH − (водн.  )
)0,401 H 2 SO 3 (водн.) + 4H + (водн.) + 4e − S(т) + 3H 2 O(л) 0,45 I 2 (s) + 2e − 2I − (aq) 0,5355 MnO 4 2− (водн.) + 2H 2 O(ж) + 2e − MnO 2 (тв) + 4OH − 906 0,6 O 2 (г) + 2H + (водн.) + 2e − H 2 O 2 (водный) 0,695 H 2 SeO 3 (водн.) + 4H + + 4e − Se(s) + 3H 2 O(ж) 0,74 Fe 3+ (водн.) + e − Fe 2+ (водн.) 0,771 Ag + (водный) + e − Ag(s) 0,7996 NO 3 − (водн.  ) + 3H + (водн.) + 2e − HNO 2 (водн.) + H 2 O(l)
) + 3H + (водн.) + 2e − HNO 2 (водн.) + H 2 O(l)0,94 Br 2 (водн.) + 2e − 2Br − (водн.) 1,087 MnO 2 (т) + 4H + (водн.) + 2e − Mn 2+ (водн.) + 2H 2 O(л) 1,23 О 2 (г) + 4H + (водн.) + 4e − 2H 2 O(л) 1,229 CR 2 O 7 2- (AQ) + 14H + (AQ) + 6E – 2CR 3+ (AQ) + 7H 22 2 3333333333333333 (AQ) + 7H 2 2 333333333333333333333333 3+ (AQ) + 7H
22 2 33333333. 3+ (AQ) + – 2 3+ (AQ).
1,36 Cl 2 (г) + 2e − 2Cl − (водн.) 1,396 Се 4+ (водн.  )+е − Се 3+ (водный)
)+е − Се 3+ (водный)1,44 PBO 2 (S) + HSO 4 – (AQ) + 3H + (AQ) + 2E – PBSO 4 (S) + 2H 2H 3 2H1233 2H1233 2H1233 2H1233 2H1233 2H1233 2H1233 2H1233 2H1233 2H1233 2H1233 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2H123 2. 1,69 H 2 O 2 (водн.) + 2H + (водн.) + 2e − 2H 2 O(л) 1,763 F 2 (г) + 2е − 2F − (водный) 2,87 Источник: UC Davis ChemWiki
Любые два проводящих материала, вступающих в реакции с разными стандартными потенциалами, могут образовать электрохимическую ячейку, потому что более сильный сможет отбирать электроны у более слабого. Но идеальным выбором для анода был бы материал, который вызывает реакцию со значительно более низким (более отрицательным) стандартным потенциалом, чем материал, который вы выбрали для своего катода. В итоге мы получаем, что электроны притягиваются к катоду от анода (и анод не пытается сильно сопротивляться), и когда у нас есть легкий путь туда — проводящий провод — мы можем использовать их энергию для обеспечения электрического тока. питание на фонарик, телефон или что-то еще.
В итоге мы получаем, что электроны притягиваются к катоду от анода (и анод не пытается сильно сопротивляться), и когда у нас есть легкий путь туда — проводящий провод — мы можем использовать их энергию для обеспечения электрического тока. питание на фонарик, телефон или что-то еще.
Разница в стандартном потенциале между электродами примерно равна силе, с которой электроны перемещаются между двумя электродами. Это известно как общий электрохимический потенциал ячейки, и он определяет напряжение ячейки. Чем больше разница, тем больше электрохимический потенциал и выше напряжение.
Чтобы увеличить напряжение батареи, у нас есть два варианта. Мы могли бы выбрать разные материалы для наших электродов, которые придадут клетке больший электрохимический потенциал. Или мы можем сложить несколько ячеек вместе. Когда элементы объединены определенным образом (последовательно), это оказывает аддитивное влияние на напряжение батареи. По сути, силу, с которой электроны движутся через батарею, можно рассматривать как общую силу, когда они движутся от анода первой ячейки через все ячейки, содержащиеся в батарее, к катоду последней ячейки.
Когда ячейки объединены другим способом (параллельно), это увеличивает возможный ток батареи, который можно рассматривать как общее количество электронов, протекающих через ячейки, но не как их напряжение.
Электролит
Но электроды – это только часть батареи. Помните бумажки Вольта, смоченные в соленой воде? Соленая вода была электролитом, еще одной важной частью картины. Электролит может быть жидкостью, гелем или твердым веществом, но он должен обеспечивать движение заряженных ионов.
Электроны имеют отрицательный заряд, и, поскольку мы посылаем поток отрицательных электронов по нашей цепи, нам нужен способ сбалансировать движение этого заряда. Электролит обеспечивает среду, через которую могут протекать положительные ионы, уравновешивающие заряд.
Поскольку химическая реакция на аноде приводит к образованию электронов, для поддержания баланса нейтрального заряда на электроде также производится соответствующее количество положительно заряженных ионов. Они не идут по внешнему проводу (это только для электронов!), а выбрасываются в электролит.
Они не идут по внешнему проводу (это только для электронов!), а выбрасываются в электролит.
В то же время катод также должен уравновешивать отрицательный заряд электронов, которые он получает, поэтому происходящая здесь реакция должна втягивать положительно заряженные ионы из электролита (в качестве альтернативы она может также высвобождать отрицательно заряженные ионы из электрода в электролит).
Таким образом, в то время как внешний провод обеспечивает путь для потока отрицательно заряженных электронов, электролит обеспечивает путь для передачи положительно заряженных ионов, чтобы сбалансировать отрицательный поток. Этот поток положительно заряженных ионов столь же важен, как и электроны, обеспечивающие электрический ток во внешней цепи, которую мы используем для питания наших устройств. Роль балансировки заряда, которую они выполняют, необходима для поддержания всей реакции.
Теперь, если позволить всем ионам, выпущенным в электролит, полностью свободно перемещаться через электролит, они закончат тем, что покроют поверхности электродов и засорят всю систему. Таким образом, у клетки обычно есть какой-то барьер, чтобы предотвратить это.
Таким образом, у клетки обычно есть какой-то барьер, чтобы предотвратить это.
Показывать метки во время анимации Начать анимацию
При использовании батареи возникает ситуация, при которой происходит непрерывный поток электронов (через внешнюю цепь) и положительно заряженных ионов (через электролит). Если этот непрерывный поток остановлен — если цепь разомкнута, например, когда ваш фонарик выключен — поток электронов остановится. Заряды будут накапливаться, и химические реакции, управляющие батареей, прекратятся.
По мере использования батареи и протекания реакций на обоих электродах производятся новые химические продукты. Эти продукты реакции могут создать своего рода сопротивление, которое может помешать протеканию реакции с той же эффективностью. Когда это сопротивление становится слишком большим, реакция замедляется. Электронное перетягивание каната между катодом и анодом также теряет свою силу, и поток электронов прекращается. Аккумулятор медленно садится.
Зарядка аккумулятора
Некоторые распространенные батареи предназначены только для одноразового использования (известные как первичные или одноразовые батареи). Путешествие электронов от анода к катоду является односторонним. Либо их электроды истощаются, когда они выделяют свои положительные или отрицательные ионы в электролит, либо накопление продуктов реакции на электродах препятствует продолжению реакции, и дело сделано и запылено. Аккумулятор попадает в мусорное ведро (или, надеюсь, на переработку, но это совсем другая тема Nova).
Но. Преимущество этого потока ионов и электронов в том, что он имеет место в некоторых типах батарей с соответствующими материалами электродов, заключается в том, что он также может двигаться в обратном направлении, возвращая нашу батарею в исходную точку и давая ей совершенно новую жизнь. . Точно так же, как батареи изменили то, как мы можем использовать различные электрические устройства, перезаряжаемые батареи еще больше изменили полезность и срок службы этих устройств.
Когда мы подключаем почти разряженную батарею к внешнему источнику электроэнергии и отправляем энергию обратно в батарею, она обращает вспять химическую реакцию, которая произошла во время разряда. Это отправляет положительные ионы, выпущенные из анода в электролит, обратно к аноду, а электроны, которые принял катод, также возвращаются к аноду. Возвращение как положительных ионов, так и электронов обратно в анод запускает систему, поэтому она снова готова к работе: ваша батарея перезаряжена.
Показывать метки во время анимации Начать анимацию
Однако процесс не идеален. Замена отрицательных и положительных ионов из электролита обратно на соответствующий электрод по мере перезарядки батареи происходит не так аккуратно и красиво, как электрод изначально. Каждый цикл зарядки ухудшает состояние электродов еще немного, а это означает, что батарея со временем теряет производительность, поэтому даже перезаряжаемые батареи не могут работать вечно.
В течение нескольких циклов зарядки и разрядки форма кристаллов батареи становится менее упорядоченной. Это усугубляется, когда батарея разряжается/перезаряжается с высокой скоростью, например, если вы едете на своем электромобиле большими рывками, а не постоянно. Циклирование с высокой скоростью приводит к тому, что кристаллическая структура становится более неупорядоченной, в результате чего батарея становится менее эффективной.
Эффект памяти и саморазряд
Почти полностью обратимые реакции разрядки и перезарядки также способствуют так называемому «эффекту памяти». Когда вы перезаряжаете некоторые типы перезаряжаемых батарей, предварительно не разрядив их в достаточной степени, они «вспоминают», на каком уровне они были в предыдущих циклах разрядки, и не заряжаются должным образом.
В некоторых элементах это вызвано тем, как металл и электролит реагируют с образованием соли (и тем, как соль затем снова растворяется, а металл заменяется на электродах при перезарядке).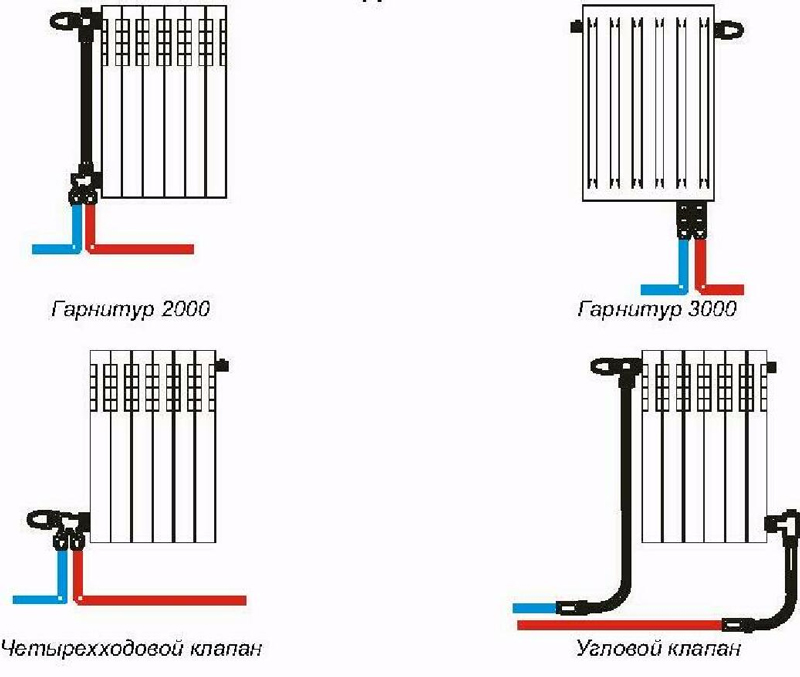 Мы хотим, чтобы наши клетки имели красивые, однородные маленькие кристаллы соли, покрывающие идеальную металлическую поверхность, но это не то, что мы получаем в реальном мире! Способ формирования некоторых кристаллов очень сложен, и способ осаждения некоторых металлов во время перезарядки также удивительно сложен, поэтому некоторые типы батарей имеют больший эффект памяти, чем другие. Несовершенства в основном зависят от состояния заряда батареи, температуры, зарядного напряжения и зарядного тока. Со временем недостатки в одном цикле зарядки могут вызвать то же самое в следующем цикле зарядки и т. д., и наша батарея накапливает некоторые плохие воспоминания. Эффект памяти силен для некоторых типов элементов, таких как батареи на основе никеля. Другие типы, такие как литий-ионные, не страдают от этой проблемы.
Мы хотим, чтобы наши клетки имели красивые, однородные маленькие кристаллы соли, покрывающие идеальную металлическую поверхность, но это не то, что мы получаем в реальном мире! Способ формирования некоторых кристаллов очень сложен, и способ осаждения некоторых металлов во время перезарядки также удивительно сложен, поэтому некоторые типы батарей имеют больший эффект памяти, чем другие. Несовершенства в основном зависят от состояния заряда батареи, температуры, зарядного напряжения и зарядного тока. Со временем недостатки в одном цикле зарядки могут вызвать то же самое в следующем цикле зарядки и т. д., и наша батарея накапливает некоторые плохие воспоминания. Эффект памяти силен для некоторых типов элементов, таких как батареи на основе никеля. Другие типы, такие как литий-ионные, не страдают от этой проблемы.
Еще один аспект перезаряжаемых батарей заключается в том, что химический состав, делающий их перезаряжаемыми, также означает, что они имеют более высокую склонность к саморазряду. Это когда внутри элемента батареи происходят внутренние реакции, даже когда электроды не подключены через внешнюю цепь. Это приводит к тому, что клетка со временем теряет часть своей химической энергии. Высокая скорость саморазряда серьезно ограничивает срок службы батареи и заставляет ее умирать при хранении.
Это когда внутри элемента батареи происходят внутренние реакции, даже когда электроды не подключены через внешнюю цепь. Это приводит к тому, что клетка со временем теряет часть своей химической энергии. Высокая скорость саморазряда серьезно ограничивает срок службы батареи и заставляет ее умирать при хранении.
Литий-ионные аккумуляторы в наших мобильных телефонах имеют довольно хорошую скорость саморазряда, около 2–3 % в месяц, и наши свинцово-кислотные автомобильные аккумуляторы также довольно разумны — они имеют тенденцию терять 4–6 %. в месяц. Аккумуляторы на основе никеля теряют около 10–15 процентов своего заряда в месяц, что не очень хорошо, если вы планируете хранить фонарь целый сезон, когда он вам не нужен! Неперезаряжаемая щелочная батарея теряет всего около 2–3 процентов своего заряда в год.
Напряжение, ток, мощность, мощность… в чем разница?
Все эти слова в основном описывают мощность батареи, верно? Ну вроде. Но все они немного разные.
Напряжение = сила, при которой реакция, приводящая в движение батарею, проталкивает электроны через ячейку. Это также известно как электрический потенциал и зависит от разности потенциалов между реакциями, происходящими на каждом из электродов, то есть от того, насколько сильно катод будет тянуть электроны (через цепь) от анода. Чем выше напряжение, тем большую работу может совершить одно и то же число электронов.
Это также известно как электрический потенциал и зависит от разности потенциалов между реакциями, происходящими на каждом из электродов, то есть от того, насколько сильно катод будет тянуть электроны (через цепь) от анода. Чем выше напряжение, тем большую работу может совершить одно и то же число электронов.
Ток = количество электронов, проходящих через любую точку цепи в данный момент времени. Чем больше сила тока, тем больше работы он может совершить при том же напряжении. Внутри ячейки вы также можете думать о токе как о количестве ионов, движущихся через электролит, умноженном на заряд этих ионов.
Мощность = напряжение x ток. Чем выше мощность, тем выше скорость, с которой батарея может работать — это соотношение показывает, насколько важны напряжение и ток для определения того, для чего подходит батарея.
Емкость = мощность батареи как функция времени, которая используется для описания периода времени, в течение которого батарея сможет питать устройство. Аккумулятор большой емкости сможет работать в течение более длительного периода, прежде чем разрядится или разрядится.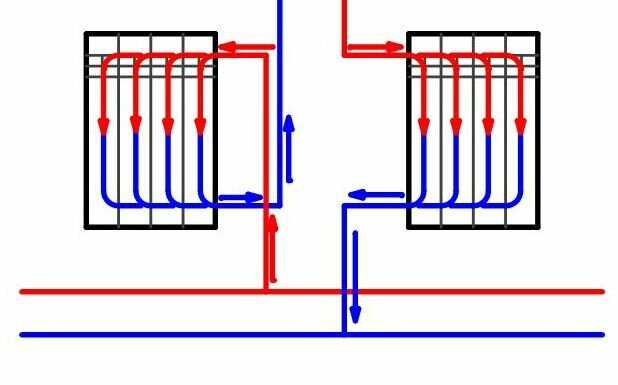 У некоторых аккумуляторов есть небольшая грустная особенность: если вы попытаетесь извлечь из них слишком много слишком быстро, вовлеченные химические реакции не смогут продолжаться, и емкость уменьшится! Таким образом, мы всегда должны быть осторожны, когда говорим о емкости батареи и помнить, для чего она будет использоваться.
У некоторых аккумуляторов есть небольшая грустная особенность: если вы попытаетесь извлечь из них слишком много слишком быстро, вовлеченные химические реакции не смогут продолжаться, и емкость уменьшится! Таким образом, мы всегда должны быть осторожны, когда говорим о емкости батареи и помнить, для чего она будет использоваться.
Другой популярный термин — «плотность энергии». Это количество энергии, которое устройство может удерживать на единицу объема, другими словами, какую отдачу вы получаете за свои деньги с точки зрения мощности и размера. С аккумулятором, как правило, чем выше плотность энергии, тем лучше, так как это означает, что аккумулятор может быть меньше и компактнее, что всегда является плюсом, когда он нужен для питания чего-то, что вы хотите держать в кармане. Для электромобилей это даже плюс — аккумулятор должен как-то влезать в машину!
Для некоторых приложений, таких как хранение электроэнергии на возобновляемой электростанции, такой как ветряная или солнечная электростанция, высокая плотность энергии не является большой проблемой, так как у них, скорее всего, будет достаточно места для хранения батарей. Основной целью такого использования было бы просто хранить как можно больше электроэнергии, как можно безопаснее и дешевле.
Основной целью такого использования было бы просто хранить как можно больше электроэнергии, как можно безопаснее и дешевле.
Видео: Как работают аккумуляторы? (TED-Ed/YouTube). Посмотреть подробности и расшифровку.
Почему так много типов?
Ряд материалов (раньше это были просто металлы) можно использовать в качестве электродов в батарее. За прошедшие годы было опробовано много-много различных комбинаций, но лишь немногие из них действительно прошли дистанцию. Но зачем вообще использовать разные комбинации металлов? Если у вас есть пара металлов, которые хорошо работают вместе в качестве электродов, зачем возиться с другими?
Различные материалы имеют разные электрохимические свойства, поэтому они дают разные результаты, когда вы кладете их вместе в элемент батареи. Например, некоторые комбинации будут создавать высокое напряжение очень быстро, но затем быстро падать, не в состоянии поддерживать это напряжение в течение длительного времени. Это хорошо, если вам нужно произвести, скажем, внезапную вспышку света, как вспышка фотокамеры.
Это хорошо, если вам нужно произвести, скажем, внезапную вспышку света, как вспышка фотокамеры.
Другие комбинации дадут лишь струйку тока, но они будут поддерживать эту струйку на века. Например, нам не нужно большое количество тока для питания детектора дыма, но мы хотим, чтобы наши детекторы дыма работали долгое время.
Еще одна причина для использования различных комбинаций металлов заключается в том, что часто для получения требуемого напряжения необходимо сложить два или более элемента батареи, и оказывается, что некоторые комбинации электродов складываются вместе гораздо лучше, чем другие комбинации. Например, литий-железо-фосфатные батареи (разновидность литий-ионных батарей), используемые в электромобилях, объединяются вместе для создания систем высокого напряжения (100 и даже более вольт), но вы никогда не сделаете этого с теми никель-кадмиевыми батареями Walkman, которые получают горячий!
Наши различные потребности со временем привели к разработке огромного количества типов батарей.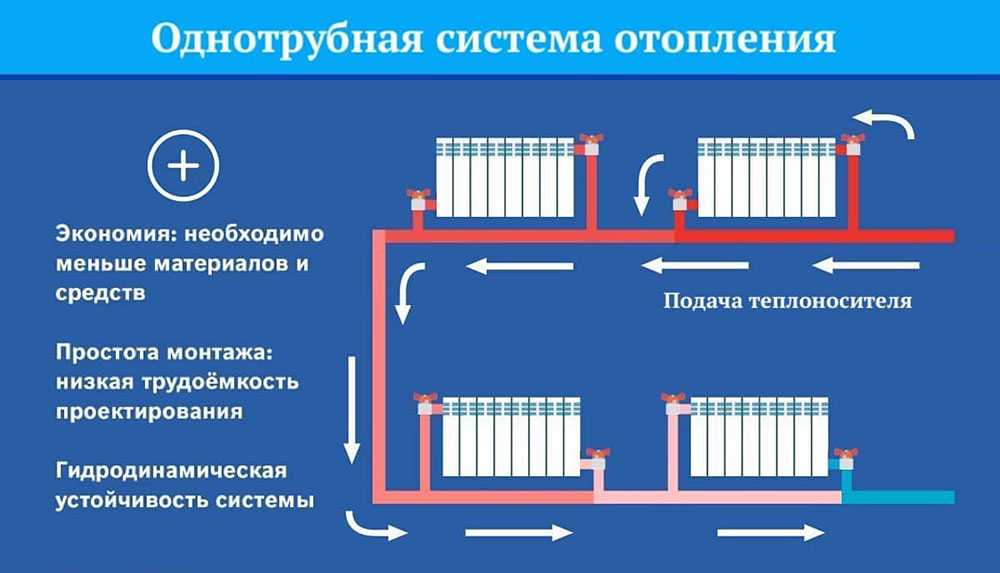 Чтобы узнать больше о них и о том, что ждет аккумулятор в будущем, ознакомьтесь с другими нашими темами Nova.
Чтобы узнать больше о них и о том, что ждет аккумулятор в будущем, ознакомьтесь с другими нашими темами Nova.
Колонка: Автопроизводители возвращаются в будущее, чтобы обезопасить аккумуляторные металлы
ЛОНДОН, 27 апреля (Рейтер) — Оказывается, Генри Форд был прав с самого начала.
После десятилетий оттачивания глобальных сетей поставок «точно в срок» автомобильные компании возвращаются к основополагающему принципу самодостаточности Форда.
Знаменитый комплекс Ford River Rouge в Дирборне, штат Мичиган, производил собственное железо и сталь, поставляемые грузовыми судами компании из собственных шахт по добыче железной руды и коксующегося угля в Мичигане и Кентукки.
Первая мировая война привела к нехватке материалов и нарушению логистики. Ответ Ford состоял в том, чтобы взять на себя полную ответственность за цепочку поставок автомобилей от шахты до продукта.
Ответ Ford состоял в том, чтобы взять на себя полную ответственность за цепочку поставок автомобилей от шахты до продукта.
Автомобильные компании сегодня сталкиваются с теми же проблемами, которые усугубляются необходимостью перехода на электричество, что означает создание совершенно новых цепочек поставок металлических изделий.
В то время как Форд беспокоился о железной руде и каучуке, его преемники борются с перебоями в поставках и резким ростом цен на ключевые материалы для аккумуляторов, такие как литий, никель и кобальт.
Если «безумные» цены на литий сохранятся, написал в Твиттере генеральный директор Tesla (TSLA.O) Илон Маск, компании «возможно, придется заняться добычей и переработкой непосредственно в масштабе».
Он не единственный руководитель автомобильной отрасли, думающий о самообеспечении минералами.
«Генри Форд… был прав», — считает действующий генеральный директор Ford Motors (F.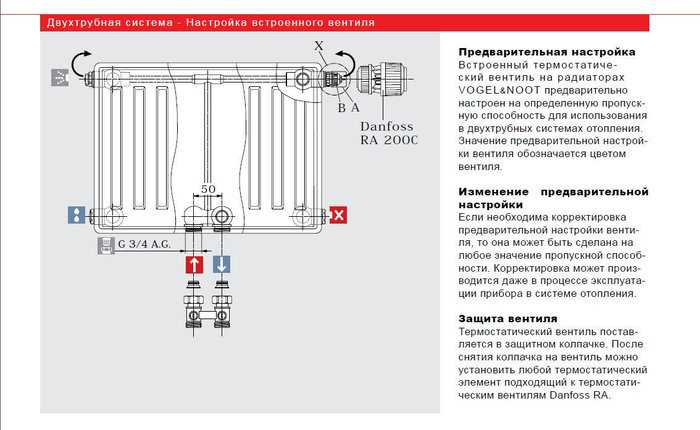 N) Джим Фарли. «Самое главное, что мы вертикально интегрируем». Компания намерена взять под контроль свои цепочки поставок «вплоть до шахт». подробнее
N) Джим Фарли. «Самое главное, что мы вертикально интегрируем». Компания намерена взять под контроль свои цепочки поставок «вплоть до шахт». подробнее
ЛИТИЕВЫЕ ТОРМОЗА
Проблемой, стоящей перед каждой автомобильной компанией, является скачок стоимости литий-ионных аккумуляторов, который вынудил многих, в том числе Tesla, поднять цены на электромобили (EV).
Стоимость аккумуляторных блоков ранее имела долгосрочную тенденцию к снижению благодаря постепенным техническим усовершенствованиям. Внезапный поворот цен на электромобили угрожает коллективной цели достижения ценового паритета с двигателями внутреннего сгорания.
Виной всему взбесившиеся цены на аккумуляторный металл.
Цена на кобальт выросла почти втрое с начала 2021 года. В марте цены на никель стали такими дикими, что Лондонской бирже металлов (LME) пришлось приостановить торги. При текущих $33 600 за тонну это на 59 больше.% на начало января.
При текущих $33 600 за тонну это на 59 больше.% на начало января.
Производители аккумуляторов отреагировали на это увеличением использования литий-железо-фосфатной химии, в которой не используются ни кобальт, ни никель, но это только способствовало ужесточению самого литиевого рынка, поскольку спотовые цены удвоились с начала года.
На металлы приходилось 40% затрат на аккумуляторы в 2015 году, а в этом году этот показатель вырос до 80%, по данным консалтинговой компании Benchmark Minerals.
Общей темой является то, что предложение не может достаточно быстро отреагировать на скачкообразное изменение спроса, поскольку продажи электромобилей ускоряются, а мир строит все больше гигафабрик для производства необходимых батарей.
Цены могут частично потерять свой недавний накал, но мало кто ожидает полного возврата к предыдущим более низким торговым диапазонам.
Это большая головная боль для каждого автопроизводителя. Но для некоторых это может оказаться экзистенциальным.
Benchmark Minerals предупреждает о возможном росте дефицита предложения в ближайшие годы. «Даже в самых оптимистичных сценариях, когда каждый отдельный сырьевой проект в стадии реализации и существующие операции агрессивно расширяются, к 2030 году не будет хватать сырья для цепочки поставок аккумуляторов».
Недостаточное предложение металлов может затормозить революцию электромобилей, поскольку те, кто не может обеспечить достаточное количество металлов, столкнутся с перспективой снижения производства и более медленных сроков развертывания.
Нынешние проблемы полупроводников в отрасли «являются небольшим аппендиксом к тому, что мы собираемся ощутить на аккумуляторных элементах в течение следующих двух десятилетий», — сказал Wall Street Journal Р. Дж. Скариндж, генеральный директор стартапа по производству электромобилей Rivian Automotive.
Дж. Скариндж, генеральный директор стартапа по производству электромобилей Rivian Automotive.
METALS RUSH
Страх перед высокими ценами и страх упустить полную выгоду заставляют автопроизводителей двигаться вверх по течению «вплоть до рудников».
Tesla сама по себе является своего рода первопроходцем, не скрывающим своих амбиций по производству собственных аккумуляторов из металла, полученного непосредственно от горняков.
У него есть будущие тоннажи, полученные от литиевых проектов в Соединенных Штатах и Австралии, и соглашение о закупке с предложенным Talon Metals Corp (TLO.TO) никелевым рудником Tamarack в Миннесоте.
BMW Group связала поставки как кобальта, так и лития для грядущего пятого поколения аккумуляторных элементов и предоставит «сырье, доступное двум производителям аккумуляторных элементов, CATL и Samsung SDI», заявила компания.
Это пример того, как автопроизводитель получает право собственности на металлы для аккумуляторов от колыбели до могилы и, возможно, даже дольше, если коммерческая переработка литий-ионных аккумуляторов наберет обороты.
Volkswagen (VOWG_p.DE) вышел за рамки простых сделок купли-продажи, сформировав альянс с китайской Tsingshan Group и Huayou Cobalt (603799.SS) для добычи и переработки достаточного количества никеля и кобальта для производства аккумуляторов для электромобилей мощностью 160 гигаватт-часов. читать дальше
Лихорадка аккумуляторных металлов уже началась, и твит Маска неизбежно вызвал несколько волнений в секторе акций горнодобывающей промышленности. Или, по крайней мере, так было до того, как он решил купить сам Twitter, а не добытчик лития.
Однако рыночная логика недостаточного предложения и завышенных цен означает, что это может быть только вопросом времени, когда Tesla и другие производители электромобилей начнут заниматься грязным бизнесом по добыче этого материала.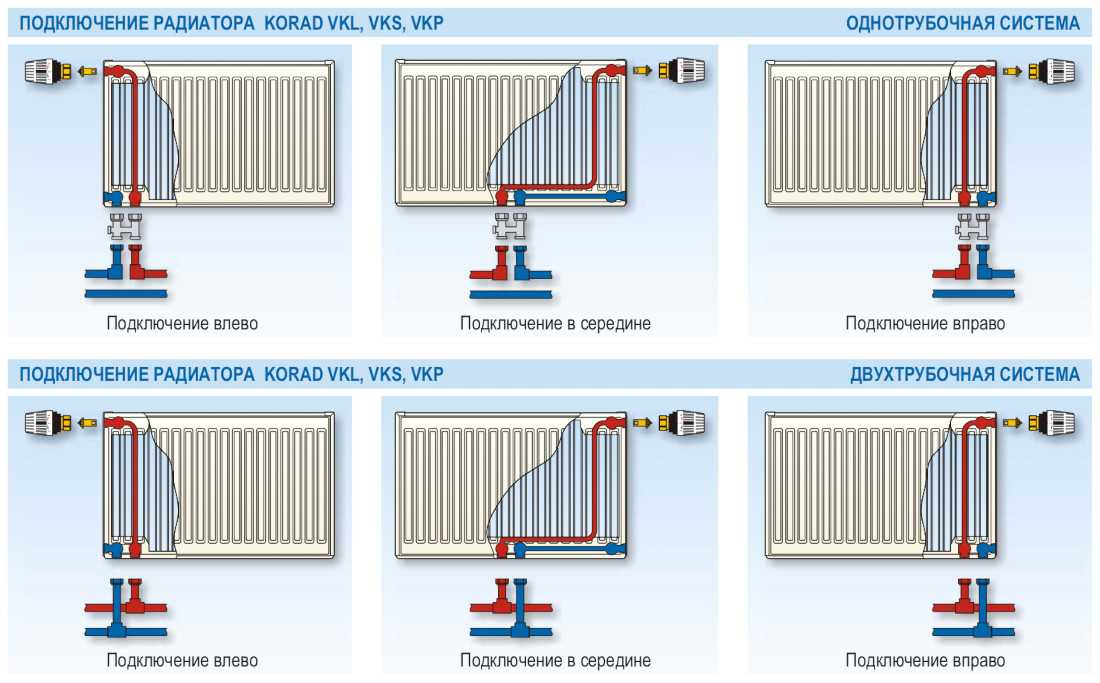
Самым большим препятствием для увеличения поставок лития и никеля является капитал. Новые рудники стоят больших денег, а время разработки увеличивается на несколько лет.
Волатильность цен не успокаивает традиционных кредиторов, а рынок бумаг все еще слишком неликвиден, чтобы хеджировать финансовые риски.
Автопроизводители могут использовать большой капитал. Они уже сделали это на этапе производства аккумуляторов в цепочке поставок. Расширение этой вертикальной интеграции на рудники, производящие необходимые металлы, сейчас становится неотложной задачей.
Те, кто пропустят, рискуют увидеть, как революция электромобилей ускоряется от них.
Мнения, выраженные здесь, принадлежат автору, обозревателю Reuters
Под редакцией Дэвида Эванса
Наши стандарты: Принципы доверия Thomson Reuters.
 Большое отклонение от этого показателя приведет к недостаточному прогреву нижнего уровня помещения или же спровоцирует сложности при уборке. Расстояние до подоконника должно составлять около 10-12 см – такое значение позволяет воздух свободно огибать препятствие и полноценно прогревать окно.
Большое отклонение от этого показателя приведет к недостаточному прогреву нижнего уровня помещения или же спровоцирует сложности при уборке. Расстояние до подоконника должно составлять около 10-12 см – такое значение позволяет воздух свободно огибать препятствие и полноценно прогревать окно.
 E 0 измеряется в вольтах.
E 0 измеряется в вольтах. .
. )
) )
) ) + 3H + (водн.) + 2e − HNO 2 (водн.) + H 2 O(l)
) + 3H + (водн.) + 2e − HNO 2 (водн.) + H 2 O(l) )+е − Се 3+ (водный)
)+е − Се 3+ (водный)