Материальный баланс процесса ректификации.
Исходная смесь при ректификации вводится в верхнюю часть исчерпывающей секции. Здесь она взаимодействует в противотоке с паром, начальный состав которого аналогичен составу остатка смеси, которая обедняется НК и обогащается ВК.
В укрепляющей секции пар, поступающий из нижней ступени, взаимодействует в противотоке с жидкостью, исходный состав которой аналогичен составу дистиллята. Происходит укрепление пара, т. е. обогащение его НК. Пар для питания ректификационного аппарата образуется в кубе (рис. 10) путем испарения части поступающей жидкости. Флегма для орошения аппарата образуется в дефлегматоре в ркзультате конденсации части пара, имеющего состав, близкий составу дистиллята.
Т
Рис. 10. К выводу уравнения материального баланса: 1 – укрепляющая часть колонны;2 – исчерпывающая часть колонны; 3 – куб; 4 – дефлегматор
 В дефлегматоре
происходит отвод тепла, вследствие чего
поступающие в него пары полностью или
частично конденсируются. Дистиллят из
дефлегматора отводится в жидком или
парообразном состоянии. Остаток отводится
из куба в виде жидкости.
В дефлегматоре
происходит отвод тепла, вследствие чего
поступающие в него пары полностью или
частично конденсируются. Дистиллят из
дефлегматора отводится в жидком или
парообразном состоянии. Остаток отводится
из куба в виде жидкости.Обозначим F количество поступающей на ректификацию смеси (в кмоль/с), через Р – количество получаемого дистиллята (в кмоль/с), через W – количество остатка (в кмоль/с) и через хF,хP,xW – составы смеси, дистиллята и остатка (в мол. долях НК).
Тогда уравнение материального баланса для всего количества смеси принимает вид
F= P+W, (9)
для НК
F хF = P хP +W xW . (10)
(10)При помощи уравнений (9) и (10) решаются все задачи, связанные с определением количества или состава веществ, участвующих в процессе ректификации. Обычно заданы количество смеси F и составы хF , хP , xW . Количество дистиллята Р и остатка W вычисляется совместным решением (9) и (10).
Уравнения применимы и при выражении величин F, Р и W в весовых количествах (в кг/с). При этом составы смеси, дистиллята и остатка должны быть выражены в весовых долях (аF
Для дальнейшего анализа процесса ректификации примем следующие допущения:
Молярная теплота испарения обоих компонентов одинакова, и каждый кмоль сконденсировавшегося пара испаряет 1 кмоль жидкости, вследствие чего количество поднимающегося пара и стекающей жидкости по высоте колонны не изменяется, а изменяется их состав.
 Надо отметить, что молярная теплота
испарения (в Дж/кмоль) различных веществ
приблизительно одинакова. Поэтому
сделанное допущение не приводит к
значительной ошибке, если расчет
процесса ректификации вести не в
весовых, а в молярных величинах.
Надо отметить, что молярная теплота
испарения (в Дж/кмоль) различных веществ
приблизительно одинакова. Поэтому
сделанное допущение не приводит к
значительной ошибке, если расчет
процесса ректификации вести не в
весовых, а в молярных величинах.Исходная жидкая смесь подается при температуре кипения, следовательно, нет расхода тепла на подогрев. В этих условиях количество стекающей жидкости в нижней части колонны (ниже ввода исходной смеси) увеличивается на количество введенной смеси.
При конденсации пара в дефлегматоре не происходит изменения его состава, он аналогичен составу дистиллята.
Составы пара нижней части колонны и остатка хW совпадают, потому что при испарении жидкости в кубе не происходит изменения концентрации комопнентов.
Обозначим
через G и L количества паровой и жидкой фаз, через y1 y2 – молярные
доли НК в парах при входе в колонну и на
выходе из нее, через х1 х2 – молярные
доли НК в жидкости на входе в колонну и
выходе из нее.
, (11)
откуда
. (12)
Аналогично, составляя материальный баланс по НК для части аппарата расположенной ниже сечения А–А,
, (13)
откуда
. (14)
Расход поднимающегося пара G постоянен во всей колонне. Часть пара из дефлегматора Ф возвращается в колонну в виде флегмы, а остальная часть Р отводится в виде дистиллята. Таким образом, G = Ф+Р.
Отношение
(15)
называется
флегмовым числом.
Из (15) следует Ф = PR и количество поднимающегося пара составляет
G= PR + P=P(R+1), (16)
т. е. на каждый кмоль дистиллята в кубе испаряется (R+1) кмоль остатка.
В укрепляющей колонне стекающая жидкость – флегма, следовательно справедливо
L=Ф=PR, (17)
а состав пара на выходе равен составу подаваемой на орошение флегмы
у2=х2=хР .
Подставляя значения
. (18)
Для х = хР, из уравнения (58) вычислим у = хР,
т. е. на у–х-диаграмме
рабочая линия укрепляющей колонны
проходит через лежащую на диагонали
точку a с абсциссой хР.
Тангенс угла наклона рабочей линии
,
а отрезок, отсекаемый на оси ординат,
составляет
е. на у–х-диаграмме
рабочая линия укрепляющей колонны
проходит через лежащую на диагонали
точку a с абсциссой хР.
Тангенс угла наклона рабочей линии
,
а отрезок, отсекаемый на оси ординат,
составляет
. (19)
В исчерпывающей колонне количество стекающей жидкости L больше, чем флегмы Ф на количество исходной жидкой смеси F. Обозначая , найдём для исчерпывающей части колонны
L=Ф+
F=P(R+f). (20)Составы поступающего в колонну пара и выходящей из нее жидкости равны составу остатка
y1=х1=х W.
После подстановки значений L и G, y1 и х1 получим
(21)
или
. (22)
(22)
При х = хW, по уравнению (22) у = хW, т. е. рабочая линия исчерпывающей колонны проходит через лежащую на диагонали точку c с абсциссой хW.
Найдем абсциссу b пересечения рабочих линий укрепляющей и исчерпывающей колонн, исходя из условия равенства ординат точек, определяемых по уравнениям (18) и (22):
. (23)
Умножив обе части этой формулы на (R+1), получим произведение подобных членов:
хР=fх – (f – 1)xW. (24)
Учитывая, что , решение уравнения (24) относительнох будет иметь следующий вид
, (25)
т. е. абсцисса точки b равна составу
исходной смеси хF.
е. абсцисса точки b равна составу
исходной смеси хF.
Д
Рис. 17. Построение рабочей линии
ректификационной колонны
ля построения нау–х -диаграмме рабочих линий
(рис. 17) откладывают на оси абсцисс точки хW, хF, хР,
соответствующие составам остатка,
исходной смеси и дистиллята, проводят
через эти точки вертикали хWс, хFb, хРa, /. Далее в зависимости от принятого
флегмового числа R откладывают на оси ординат отрезок оd.
Точку d на оси ординат и точку a пересечения вертикали хРa с диагональю соединяют прямой da. Точку b пересечения этой прямой
с вертикалью хFb соединяют с точкой c пересечения вертикали хWс с диагональю.
2.Материальный баланс ректификационной колонны.
Материальный баланс будет иметь вид:
для всей колонны
Для НКК
Подставив в последнее уравнение вместо W величину F — D, получим
Тогда относительный отбор ректификата составит
Соответственно относительный отбор остатка составит
3.Материальный баланс верхней части колонны.
Рассмотрим уравнения материальных балансов для части колонны, находящейся выше сечения 1—1 (см. рис. IV-5). Запишем материальные балансы:
G =g+D или G-g=D
Из уравнения
следует, что при стационарном режиме
работы колонны (потоки массы не изменяются)
разность потоков пара и жидкости в любом
сечении верхней части колонны — величина
постоянная, равная массе потока
ректификата D,
т.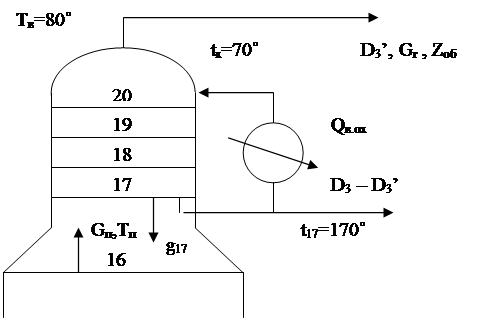 е. G >g. Следовательно,
при увеличении или уменьшении одного
из потоков (пара или жидкости) второй
поток изменяется соответственным
образом.
е. G >g. Следовательно,
при увеличении или уменьшении одного
из потоков (пара или жидкости) второй
поток изменяется соответственным
образом.
Или
Разделив числитель и знаменатель каждого слагаемого уравнения на D и обозначив флегмовое число через R = g/D, которое является важнейшим показателем процесса ректификации, получим
Уравнения называются уравнением рабочей линии, уравнением концентраций, или уравнением оперативной линии. Оно устанавливает связь между составами встречных потоков пара и жидкости в произвольном сечении колонны и является общим для любого сечения концентрационной части колонны.
4.Материальный баланс нижней части колонны.
У равнение рабочей линии для нижней части колонны. Перейдем к анализу работы нижней части колонны. Для этого рассмотрим потоки для
части колонны ниже
сечения 4—4. Материальный баланс для этой части
колонны запишется следующим образом:
Материальный баланс для этой части
колонны запишется следующим образом:
общий
g=G+W или g–G=W
И з данных уравнений следует, что для любого сечения в нижней части колонны масса жидкости больше массы паров, т. е. д > G, и массы обоих потоков изменяются в одном направлении, одновременно возрастая или убывая.
Или
Разделив числитель и знаменатель каждого слагаемого на W и обозначив паровое число через П = G/W, получим
Уравнения называются уравнением рабочей линии для нижней части колонны и устанавливают зависимость между концентрациями встречных потоков пара и жидкости в произвольном сечении нижней части колонны. Оно является общим для любого сечения отгонной части колонны.
5.Материальный баланс секции питания колонны.
П
однимается
паровая фаза от сырья GF, yF и с последней тарелки N0 (отгонная) GNo, yNo и
они объединяются Gm и образуют среднюю концентрацию ym.
Аналогично для жидкой фазы.
Т.о. в секции питания встречаются 4 потока.
F=GF+gF
– доля отгона
– уравнение материального баланса сырья, входящего в секцию питания
Линия сырья.
Учебное пособие по дистилляции II: метод дистилляции Маккейба-Тила Дизайн (Главная страница) Метод Маккейба-Тиле для проектирования перегонки представляет собой графический метод.
дизайна, который восходит к началу 20 го века. Используется в качестве вводного метода обучения
дизайн дистилляции и до сих пор используется инженерами, которые проектируют
дистилляционные колонны. Метод Маккейба-Тиле рассматривает бинарные
дистилляции, но также может использоваться для так называемых псевдобинарных
смеси (т. е. смеси, которые рассматриваются как бинарные путем идентификации легких
и тяжелые ключевые компоненты). 1. Вводные понятия. Основные характеристики Метод Маккейба-Тиле заключается в том, что это:
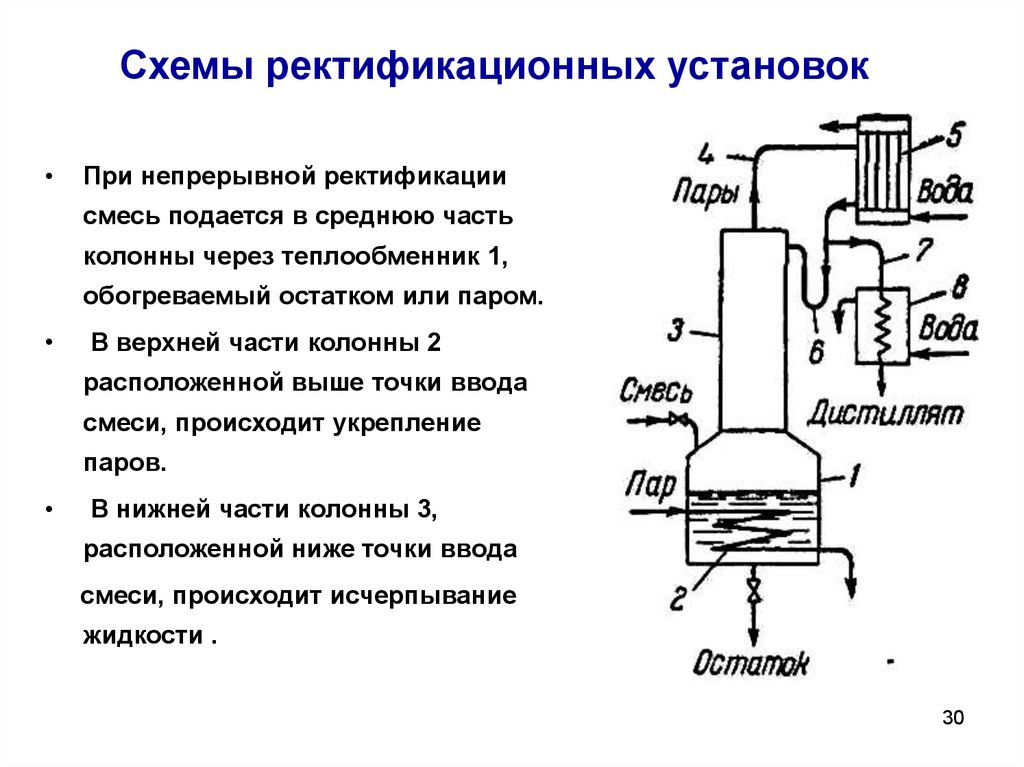
Бинарная перегонка. Самый простой способ понять Метод Маккейба-Тиле является графическим. Для этого начнем с чуть более подробная схема ректификационной колонны, чем показана на Рис. 1 Учебника I.  ступень f между верхом и низом и может быть жидкостью, паром или
смесь того и другого. Совокупность лотков над кормовой площадкой называется
ректификационная часть ректификационной колонны и продукт дистиллята
обычно выводится из верхней части столбца. Лотки под кормушкой
стадия включает отпарную секцию колонны и нижний продукт
выводится из ребойлера. Пар, который образуется при добавлении
тепло в ребойлер, течет вверх по колонне, потому что давление в
нижняя часть столбца (немного) выше, чем верхняя. Жидкость,
с другой стороны, стекает вниз по колонне и образуется за счет конденсации
часть пара поступает в конденсатор. Порция жидкости
из холодильника, который возвращается в ректификационную колонну, называется
рефлюкс, в то время как пар, который образуется в ребойлере, называется паром
вскипеть. ступень f между верхом и низом и может быть жидкостью, паром или
смесь того и другого. Совокупность лотков над кормовой площадкой называется
ректификационная часть ректификационной колонны и продукт дистиллята
обычно выводится из верхней части столбца. Лотки под кормушкой
стадия включает отпарную секцию колонны и нижний продукт
выводится из ребойлера. Пар, который образуется при добавлении
тепло в ребойлер, течет вверх по колонне, потому что давление в
нижняя часть столбца (немного) выше, чем верхняя. Жидкость,
с другой стороны, стекает вниз по колонне и образуется за счет конденсации
часть пара поступает в конденсатор. Порция жидкости
из холодильника, который возвращается в ректификационную колонну, называется
рефлюкс, в то время как пар, который образуется в ребойлере, называется паром
вскипеть. 2. Метод Маккейба-Тиле. Одна из ключевых особенностей
Метод Маккейба-Тиле (как и другие методы проектирования дистилляции)
предполагается, что пар, поступающий со ступени ниже, и жидкость
поступающие из лотка выше соприкасаются друг с другом и оставляют
любой данной стадии в равновесии. Графические этапы метода Маккейба-Тиле
Мы также можем начать спуск ступеней в любой дистилляционной колонне, начиная с точки x B на линии 45 градусов и двигаясь вверх. Также можно указать желаемую степень кипения, с, вместо желаемого флегмового числа r. Практические упражнения. Понимание графической природы Метод Маккейба-Тиле — важный первый шаг в понимании дистилляционная конструкция. Рассмотрим 30-70% смесь этана и пропана при 150 фунтов на квадратный дюйм, когда сырье является насыщенной жидкостью при температуре начала кипения. Предположим, что желаемый состав донных отложений равен x В = 0,05 и желаемый состав дистиллята х D = 0,99. Пусть закипит коэффициент должен быть указан при s = 2. Ответьте на следующий вопрос:
Просто нажмите кнопку воспроизведения. 3. Уравнения метода Маккейба-Тиле. Есть число важных уравнений, вытекающих из метода Маккейба-Тила, которые связанные с балансом массы и энергии. Эти уравнения включают в себя операционные линии (т.е. линии выпрямления и очесывания), линия подачи, зависимость между флегмовым числом и коэффициентом кипения, а также определение потребности в отоплении и охлаждении. Вопросы баланса массы. Балансировка массы является важным
часть конструкции дистилляционной колонны, анализа и моделирования. Предполагать
мы
вернитесь к нашему изображению делителя C2, в который подается 100 фунтов моль/ч
смесь 50-50% этана и этилена, имеет насыщенную подачу
жидкость при точке кипения и работает при давлении 100 фунтов на квадратный дюйм. Операционные линии. Вернитесь к рис. 1 и нарисуйте воображаемый (массовый баланс) бокс, в котором находится ребойлер и все ступени до и включая стадию j в нижней части колонны, так что только нижний продукт и потоки, входящие или выходящие из стадии j, пересекают эту воображаемый ящик. Этот воображаемый ящик часто называют массовым балансом. конверт. Если мы теперь запишем полный баланс массы для этого воображаемого ящика мы получаем
Если мы также напишем массовый баланс компонентов для этилена, который мы вызываем компонент 1, получаем
Решим уравнение. 2.2 для y j . Это дает
Теперь воспользуемся формулой. 2.1, чтобы исключить L j+1 из уравнения. 2.3. К для этого просто замените V j + B на L j+1 в уравнении. 2.3. Это дает
Если мы определим s, коэффициент испарения или кипения, как s = V/B, то уравнение 2.4 можно переписать как
Наконец, мы можем заменить s/s на 1 в первом члене на дальнем конце.
, которая называется линией зачистки. Сейчас вам важно
видим, что наклон этой линии равен (s+1)/s и что она пересекает
Линия под углом 45 градусов в точке x B . Во-первых, мы рассматриваем уравнение. 2,6
определить y j как функцию x j+1 . Таким образом, уравнение 2,6
можно записать в привычной форме y = mx + b. Если вы затем сравните уравнение
2.6 до y = mx + b, наклон равен (s+1)/s. Понимание того, почему уравнение 2,6
пересекает линию под углом 45 градусов в точке x B немного сложнее. Здесь
вы должны понимать, что пересечение линии под углом 45 градусов в точке x B означает y j = x j+1 = x B . Итак, если мы установим
y j = x B в уравнении 2.6 и проделаем простую алгебру
должно получиться, что x j+1 = x B . Давайте так.
Однако из уравнения. 2.5 мы знаем, что последний член в уравнении. 2,8 также может можно записать как [1 + 1/s]x j+1 . Следовательно, уравнение 2.8 может быть пишется как
Разделив обе части уравнения. 2.9 на [1 + 1/с], мы видим, что х j+1 = х В . Практические упражнения. Чтобы укрепить свои навыки балансировки массы,
ответить на следующие вопросы.
Энергетические аспекты метода Маккейба-Тиле. Помнить мы сказали, что дистилляция может использовать большое количество энергии. Эта энергия подается в виде тепла в ребойлер и охлаждения в конденсатор. Хотя это и не очевидно, метод Маккейба-Тиле работает. учитывать энергетические соображения приближенным образом через коэффициенты кипения и флегмы s и r соответственно. определение с s = V/B, где B — расход кубового продукта, а V — расход пар из ребойлера. Использование общего баланса массы вокруг ребойлера (см. рис. 1) мы видим, что общее количество жидкого материала, поступающего ребойлер
Поскольку жидкий остаток B и пар V покидают ребойлер, V представляет собой количество поступающей жидкости L, которая испаряется при добавлении нагревать. Мы можем выразить эту часть через коэффициент кипения s как следует. Разделив обе части уравнения. 2.10 на V получаем
Преобразование уравнения. 2.11 получаем
, что показывает, что V — это просто L, умноженное на дробь s/(s+1).
Обратите внимание, что s/(s+1) должно лежать между 0 и 1. Для s = 0 не существует
поток пара, так как Ls = 0, и это согласуется с тем, что s =
V/B = 0 означает, что V = 0. Для s = 0,5 количество пара равно V = [0,5/1,5] л.
= л/3. Это говорит о том, что поток пара составляет одну треть от потока жидкости.
в ребойлер при s = V/B = 0,5.
так что все нормально. По мере увеличения s количество пара увеличивается от минимума 0 при s = 0 до максимума L, когда s = бесконечность, s/(s+1) = 1 и B = 0. Теперь, когда у нас есть способ рассчитать расход пара V, мы также можем
вычислить тепловую энергию, необходимую для производства этого пара. Чтобы рассчитать
необходимого количества тепла, необходимо сначала определить теплоту парообразования
в
нижний продукт. Для этого нам понадобятся теплоты парообразования обоих
компонентов в нашей смеси, и мы также должны использовать очень распространенный инженерный
приближение усреднения веса. Предположим, что мы обозначаем теплоту
испарения этилена в нашем примере за счет l1 и теплоты
испарение этана по l2. Нижний продукт имеет состав
х B , где x B – мольная доля этилена
так как это легкая составляющая.
, где λB используется для обозначения теплоты парообразования нижний продукт. Количество тепла, необходимое в ребойлере, которое мы обозначаем Q R , теперь можно рассчитать с помощью уравнения
Мы также можем определить степень охлаждения, необходимую для конденсатора почти так же, как мы только что определили потребности в отоплении для ребойлера. Для этого мы можем просто использовать усреднение веса формула
где здесь λ D – теплота парообразования дистиллятный продукт, х D – состав этилена в дистиллятный продукт, а (1 – х D ) представляет собой композицию этана в дистилляте. Величину охлаждения можно рассчитать, используя формула
где V – количество пара, поступающего в конденсатор или пар со стадии N-1. Обратите внимание, что это предполагает, что весь поток пара поступающий в конденсатор конденсируется, а затем разделяется на жидкий флегм и жидкий дистиллят. Практические упражнения.
Энергетические балансы и поведение CMO. Ступени, кроме ступеней подачи. Для любой стадии дистилляции, скажем, этап j, без внешнего потока подачи, CMO подразумевает, что
Эти уравнения получаются путем составления баланса воображаемой энергии оболочка вокруг любой отдельной ступени в секциях выпрямления или отпарки дистилляционной колонны – кроме стадии подачи – как показано на рис. 3 в сочетании с некоторым физическим приближением.
Уравнения 2. Быстрые упражнения. Определить, насколько разумно руководство по маркетингу предположение, отвечая на следующее:
Ступени подачи. Соображения энергетического баланса вокруг любого
ступень, имеющая внешнее питание, должна учитывать тепловую
качество (или содержание энергии) потока сырья.
Мы используем символ q для обозначения качества корма, где q = L F /F и представляет собой жидкую фракцию корма. Таким образом сразу видим, что для насыщенной жидкости q = 1. Для насыщенной пара, q = 0. Для смеси жидкого и парового сырья 0 < q < 1. Для переохлажденная жидкая подача, q > 1, и перегретая паровая подача, q < 0,
Теперь важно понять, что уравнения. 2,23, 2,24 и 2,25 на самом деле относятся ко всем пяти случаям качества корма. Это хорошо, потому что то только один набор уравнений может быть использован для выполнения аппроксимации энергия балансовые расчеты и их влияние на изменения в жидкости и паре потока на любой стадии с внешней подачей. Практические упражнения. Чтобы лучше понять уравнения. 2,23, 2.24 и 2.25, ответьте на следующие вопросы:
q или наклон линии подачи. Для подключения предыдущего обсуждение приблизительного энергетического баланса, термического качества сырья и метод Маккейба-Тиле, нам нужно показать, что уравнение. 2,25 вместе с определением q = L F /F можно разместить на Маккейб-Тил заговор и смысл. Для этого нам нужно понять, что q связано с наклоном линии подачи. Этот расчет q очень удобно и позволяет нам правильно провести линию подачи от пересечение вертикальной линии, проведенной из состава корма и Линия 45 градусов. Математически наклон линии подачи задается простой уравнение
Если вы задумаетесь об этом на минуту и вернетесь к своим вычислениям для q вы увидите, что
Быстрое упражнение. За результаты последней тренировки упражнений, нарисуйте линию подачи для насыщенной жидкости, насыщенного пара, смесь жидкости и пара, переохлажденной жидкости и перегретого пара кормить. Взаимосвязь энергетического баланса между флегмовым числом и вскипанием Соотношение. Использование энергетического баланса на протяжении всей дистилляции колонке, иногда называемой общим энергетическим балансом, можно показывают, что флегмовое число r и коэффициент кипения s связаны соотношением следующее уравнение
Таким образом, количество пара, образующегося в ребойлере, привязано к количество пара, сконденсированного в конденсаторе, что имеет смысл. Итоговые практические упражнения. Ответьте на следующие вопросы в чтобы практиковать то, что вы узнали во втором уроке, с учетом разделения пропилена и пропана (делитель С3) при 200 фунтов на квадратный дюйм. Пусть сырье представляет собой 50-50 мол. % смесь насыщенного пара и имеют скорость потока 100 фунт-моль/ч, x D = 0,99 и x Б = 0,01. Также пусть флегмовое число равно r = 3,5.
|
Модель стадии баланса массы и энергии для циклической дистилляции
%PDF-1.
 Надо отметить, что молярная теплота
испарения (в Дж/кмоль) различных веществ
приблизительно одинакова. Поэтому
сделанное допущение не приводит к
значительной ошибке, если расчет
процесса ректификации вести не в
весовых, а в молярных величинах.
Надо отметить, что молярная теплота
испарения (в Дж/кмоль) различных веществ
приблизительно одинакова. Поэтому
сделанное допущение не приводит к
значительной ошибке, если расчет
процесса ректификации вести не в
весовых, а в молярных величинах.
 Прежде чем представить уравнения
Метод Маккейба-Тиле иллюстрируем графически для смеси 50-50 %.
насыщенного жидкого этилена и этана при 100 фунтов на квадратный дюйм. Мы будем называть это
колонка сплиттер C2. Наконец, мы указываем флегмовое число равным r =
3,9. Мы предлагаем вам следовать каждому шагу, обращаясь к рис. 2.
ниже.
Прежде чем представить уравнения
Метод Маккейба-Тиле иллюстрируем графически для смеси 50-50 %.
насыщенного жидкого этилена и этана при 100 фунтов на квадратный дюйм. Мы будем называть это
колонка сплиттер C2. Наконец, мы указываем флегмовое число равным r =
3,9. Мы предлагаем вам следовать каждому шагу, обращаясь к рис. 2.
ниже.


 Желаемый
состав кубового продукта x B = 0,05 и
состав дистиллята х D = 0,98. Мы сейчас
проиллюстрировать, как массовая балансировка определяет выпрямление и зачистку
линии в методе Маккейба-Тиле.
Желаемый
состав кубового продукта x B = 0,05 и
состав дистиллята х D = 0,98. Мы сейчас
проиллюстрировать, как массовая балансировка определяет выпрямление и зачистку
линии в методе Маккейба-Тиле. 2)
2) справа от уравнения 2.5 и получите
справа от уравнения 2.5 и получите
