виды, истинная и средняя. Теплоемкость
смеси
Каждое тело обладает своей, присущей только этому телу теплоемкостью.
Теплоемкостью – называют количества теплоты, необходимое для изменения температуры тела на 1 градус.
Средняя и истинная теплоемкости.
[Cm] Средней в интервале температур Т1 и Т2 температурой тела называется количество теплоты q, необходимое для повышения температуры тела на 1 градус.
(9.7)
при << ,Cm следует к истинное с – эта формула определяет истинную теплообменность тела.
В практических расчетах гораздо удобнее пользоваться средней теплоемкостью (С).
Удельная
теплоемкость – для характеристики теплоемкости
различных веществ, для возможного
сравнения между собой и для технических
расчетов вели удельную теплоемкость.
Удельной теплоемкостью – называется количество теплоты, необходимое для изменения температурное единицы количества вещества на 1 градус.
В зависимости от выбранных единиц различают теплоемкости:
Удельную массовую:
(Дж/кг*град) (9.8)
Удельную объемную
(Дж/м3*град) (9.9)
Удельную мольную
(дж/моль*гр) (9.10)
Все 3 вида связанны следующей зависимостью:
Объемная с массовой С=с*р (9.11)
Массовая с мольной (9.12)
Мольная с объемной (9.13)
Q количество подведенной теплоты
Q=m*Cpm*(t2-t1)
(9. 14)
14)
При изохорном подогреве газа его объем не больше 1.Следовательно, он не совершает работу против внешних сил.
При изобарном подогреве газ расширяется, преодолевая внутреннюю силу, действующую на поршень, т.е. совершает работу.
Следовательно, при нагревании одного и того же газа до одинаковой температуры в одних условиях при изобарном процессе нужно затратить больше тепла, чем при изохорном.
Опыт
След. 2 случая нагрев и охлаждение.
изменяется состояние при постоянном объеме V=const
изменяется состояние при постоянном давлении p=const
Затрачиваемая на нагревание 1 кг газовой смеси, расходуется на нагрев и ее отдельных компонентов, находящихся в смеси, то температура смеси = сумме произведений температуры компонентов, состоящих в смеси, на массу и объемную доли:
Если составим смесь заданной по массе газа, то теплоемкость смеси определяется:
Cсм = с1g1 + c2g2 +…+cndn
кДж/ (моль·град) | Ккал/ (кмоль·град) | ||||
Одноатомные Двухатомный Трех- и много-атомные | 12,56 20,93 29,31 | 20,93 29,31 37,68 | 3 5 7 | 5 7 9 | 5. 7./5 9./7 |
Теплоемкость изобарная и изохорная.
Газ | Истинная теплоемкость при p=const, кДж/(моль·град) | Средняя теплоемкость p=const, кДж/(кмоль) |
N2 О2 H2 ∞ CO2 SO2 Воздух H2O | = 28,5372 + 0,005390t = 29,5802 + 0,006971t = 28,3446 + 0,003152t = 28,7395 + 0,005862t = 41,3697 + 0,014498t = 42,8728 + 0,013204t = 28,7558 + 0,005721t = 32,8367 + 0,011661t | 28,7340 + 0,002349 t 29,2080 + 0,004072t 28,7210 + 0,001201t 28,8563 + 0,002681t 38,3955 + 0,010584t 40,4386 + 0,009956t 28,8270 + 0,002708t 33,1494 + 0,005275t |
Таблица
10. 4.
4.
Массовая теплоемкость некоторых газов при постоянном (атмосферном) давлении в кДж/(кг · °C)
t, °C | Кислород О2 | Азот N2 | Водород H2 | Оксид угле-рода CO | Углекислый газ CO2 | Вода H2O | Метан CH4 | Воздух |
0 100 200 300 400 500 600 700 800 900 1000 11001200 1330 1440 1500 | 0,917 0,925 0,938 0,950 0,967 0,980 0,992 1,005 1,017 1,026 1,034 1,042 1,051 1,059 1,063 1,072 | 1,017 1,042 1,047 1,051 1,059 1,076 1,089 1,101 1,109 1,118 1,130 1,139 1,147 1,155 1,164 | 14,21 14,35 14,43 14,46 14,49 14,52 14,56 14,60 14,66 14,72 14,79 14,87 14,95 15,04 15,13 15,22 | 1,042 1,042 1,047 1,055 1,063 1,076 1,088 1,101 1,109 1,122 1,130 1,143 1,151 1,160 1,168 1,176 | 0,8205 0,8708 0,9127 0,9503 0,9838 1,013 1,042 1,066 1,088 1,109 1,126 1,143 1,160 1,172 1,185 1,197 | 1,855 1,867 1,888 1,913 1,938 1,968 2,001 2,030 2,064 2,097 2,131 2,164 2,194 2,227 2,257 2,286 | 2,190 2,471 2,800 3,206 3,650 4,104 4,545 4,991 ─ ─ ─ ─ ─ ─ ─ ─ | 1,005 1,005 1,013 1,017 1,030 1,038 1,051 1,063 1,072 1,084 1,093 1,101 1,109 1,118 1,126 1,130 |
Таблицы удельной теплоемкости веществ: газов, жидкостей, металлов, продуктов
Представлены таблицы удельной теплоемкости веществ: газов, металлов, жидкостей, строительных и теплоизоляционных материалов, а также пищевых продуктов — более 400 веществ и материалов.
- Удельная теплоемкость газов
- Удельная теплоемкость некоторых металлов и сплавов
- Удельная теплоемкость жидкостей
- Удельная теплоемкость твердых веществ
- Удельная теплоемкость пищевых продуктов
Удельной теплоемкостью вещества называется отношение количества тепла, сообщенного единице массы этого вещества в каком-либо процессе, к соответствующему изменению его температуры.
Удельная теплоемкость веществ зависит от их химического состава, термодинамического состояния и способа сообщения им тепла. В Международной системе единиц эта величина измеряется в Дж/(кг·К).
Необходимо отметить, что экспериментальное определение удельной теплоемкости жидкостей и газов производится при постоянном давлении или при постоянном объеме. В первом случае удельная теплоемкость обозначается Cp, во втором — Cv. Для жидкостей и газов наиболее часто применяется удельная теплоемкость при постоянном давлении Cp.
Для твердых веществ теплоемкости Cp и Cv не различаются. Кроме того, по отношению к твердым телам, помимо удельной массовой теплоемкости применяются также удельная атомная и молярная теплоемкости.
Таблица удельной теплоемкости газов
В таблице приведена удельная теплоемкость газов Cp при температуре 20°С и нормальном атмосферном давлении (101325 Па).
| Газы | Cp, Дж/(кг·К) |
|---|---|
| Азот N2 | 1051 |
| Аммиак NH3 | 2244 |
| Аргон Ar | 523 |
| Ацетилен C2H2 | 1683 |
| Водород H2 | 14270 |
| Воздух | 1005 |
| Гелий He | 5296 |
| Кислород O2 | 913 |
| Криптон Kr | 251 |
| Ксенон Xe | 159 |
| Метан CH4 | 2483 |
| Неон Ne | 1038 |
| Оксид азота N2O | 913 |
| Оксид азота NO | 976 |
| Оксид серы SO2 | 625 |
| Оксид углерода CO | 1043 |
| Пропан C3H8 | 1863 |
| Сероводород H2S | 1026 |
| Углекислый газ CO2 | 837 |
| Хлор Cl | 520 |
| Этан C2H6 | 1729 |
| Этилен C2H4 | 1528 |
Таблица удельной теплоемкости некоторых металлов и сплавов
В таблице даны значения удельной теплоемкости некоторых распространенных металлов и сплавов при температуре 20°С. Значения теплоемкости большинства металлов при других температурах вы можете найти в этой таблице.
Значения теплоемкости большинства металлов при других температурах вы можете найти в этой таблице.
| Металлы и сплавы | C, Дж/(кг·К) |
|---|---|
| Алюминий Al | 897 |
| Бронза алюминиевая | 420 |
| Бронза оловянистая | 380 |
| Вольфрам W | 134 |
| Дюралюминий | 880 |
| Железо Fe | 452 |
| Золото Au | 129 |
| Константан | 410 |
| Латунь | 378 |
| Манганин | 420 |
| Медь Cu | 383 |
| Никель Ni | 443 |
| Нихром | 460 |
| Олово Sn | 228 |
| Платина Pt | 133 |
| Ртуть Hg | 139 |
| Свинец Pb | 128 |
| Серебро Ag | 235 |
| Сталь стержневая арматурная | 482 |
| Сталь углеродистая | 468 |
| Сталь хромистая | 460 |
| Титан Ti | 520 |
| Уран U | 116 |
| Цинк Zn | 385 |
| Чугун белый | 540 |
| Чугун серый | 470 |
Таблица удельной теплоемкости жидкостей
В таблице представлены значения удельной теплоемкости Cp распространенных жидкостей при температуре 10…25°С и нормальном атмосферном давлении.
| Жидкости | Cp, Дж/(кг·К) |
|---|---|
| Азотная кислота (100%-ная) NH3 | 1720 |
| Анилин C6H5NH2 | 2641 |
| Антифриз (тосол) | 2990 |
| Ацетон C3H6O | 2160 |
| Бензин | 2090 |
| Бензин авиационный Б-70 | 2050 |
| Бензол C6H6 | 1050 |
| Вода H2O | 4182 |
| Вода морская | 3936 |
| Вода тяжелая D2O | 4208 |
| Водка (40% об.) | 3965 |
| Водный раствор хлорида натрия (25%-ный) | 3300 |
| Газойль | 1900 |
| Гидроксид аммония | 4610 |
| Глицерин C3H5(OH)3 | 2430 |
| Даутерм | 1590 |
| Карборан C2H12B10 | 1720 |
| Керосин | 2085…2220 |
| Кефир | 3770 |
| Мазут | 2180 |
| Масло АМГ-10 | 1840 |
| Масло ВМ-4 | 1480 |
| Масло касторовое | 2219 |
| Масло кукурузное | 1733 |
| Масло МС-20 | 2030 |
| Масло подсолнечное рафинированное | 1775 |
| Масло ТМ-1 | 1640 |
| Масло трансформаторное | 1680 |
| Масло хлопковое рафинированное | 1737 |
| Масло ХФ-22 | 1640 |
| Молоко сгущенное с сахаром | 3936 |
| Молоко цельное | 3906 |
| Нефть | 2100 |
| Парафин жидкий (при 50С) | 3000 |
| Пиво | 3940 |
| Серная кислота (100%-ная) H2SO4 | 1380 |
| Сероуглерод CS2 | 1000 |
| Силикон | 2060 |
| Скипидар | 1800 |
| Сливки (35% жирности) | 3517 |
| Сок виноградный | 2800…3690 |
| Спирт метиловый (метанол) CH3OH | 2470 |
| Спирт этиловый (этанол) C2H5OH | 2470 |
| Сыворотка молочная | 4082 |
| Толуол C7H8 | 1130 |
| Топливо дизельное (солярка) | 2010 |
| Топливо реактивное | 2005 |
| Уротропин C6H12N4 | 1470 |
| Фреон-12 CCl2F2 | 840 |
| Эфир этиловый C4H10O | 2340 |
Таблица удельной теплоемкости твердых веществ
В таблице дана удельная теплоемкость твердых веществ: стройматериалов (песка, асфальта и т. д.), теплоизоляции различных типов и других распространенных материалов в интервале температуры от 0 до 50°С при нормальном атмосферном давлении.
д.), теплоизоляции различных типов и других распространенных материалов в интервале температуры от 0 до 50°С при нормальном атмосферном давлении.
| Строительные, теплоизоляционные и другие материалы | C, Дж/(кг·К) |
|---|---|
| АБС пластик | 1300…2300 |
| Аглопоритобетон и бетон на топливных (котельных) шлаках | 840 |
| Алмаз | 502 |
| Аргиллит | 700…1000 |
| Асбест волокнистый | 1050 |
| Асбестоцемент | 1500 |
| Асботекстолит | 1670 |
| Асбошифер | 837 |
| Асфальт | 920…2100 |
| Асфальтобетон | 1680 |
| Аэрогель (Aspen aerogels) | 700 |
| Базальт | 850…920 |
| Барит | 461 |
| Береза | 1250 |
| Бетон | 710…1130 |
| Битумоперлит | 1130 |
| Битумы нефтяные строительные и кровельные | 1680 |
| Бумага | 1090…1500 |
| Вата минеральная | 920 |
| Вата стеклянная | 800 |
| Вата хлопчатобумажная | 1675 |
| Вата шлаковая | 750 |
| Вермикулит | 840 |
| Вермикулитобетон | 840 |
| Винипласт | 1000 |
| Войлок шерстяной | 1700 |
| Воск | 2930 |
| Газо- и пенобетон, газо- и пеносиликат, газо- и пенозолобетон | 840 |
| Гетинакс | 1400 |
| Гипс формованный сухой | 1050 |
| Гипсокартон | 950 |
| Глина | 750 |
| Глина огнеупорная | 800 |
| Глинозем | 700…840 |
| Гнейс (облицовка) | 880 |
| Гравий (наполнитель) | 850 |
| Гравий керамзитовый | 840 |
| Гравий шунгизитовый | 840 |
| Гранит (облицовка) | 880…920 |
| Графит | 708 |
| Грунт влажный (почва) | 2010 |
| Грунт лунный | 740 |
| Грунт песчаный | 900 |
| Грунт сухой | 850 |
| Гудрон | 1675 |
| Диабаз | 800…900 |
| Динас | 737 |
| Доломит | 600…1500 |
| Дуб | 2300 |
| Железобетон | 840 |
| Железобетон набивной | 840 |
| Зола древесная | 750 |
| Известняк (облицовка) | 850…920 |
| Изделия из вспученного перлита на битумном связующем | 1680 |
| Ил песчаный | 1000…2100 |
| Камень строительный | 920 |
| Капрон | 2300 |
| Карболит черный | 1900 |
| Картон гофрированный | 1150 |
| Картон облицовочный | 2300 |
| Картон плотный | 1200 |
| Картон строительный многослойный | 2390 |
| Каучук натуральный | 1400 |
| Кварц кристаллический | 836 |
| Кварцит | 700…1300 |
| Керамзит | 750 |
| Керамзитобетон и керамзитопенобетон | 840 |
| Кирпич динасовый | 905 |
| Кирпич карборундовый | 700 |
| Кирпич красный плотный | 840…880 |
| Кирпич магнезитовый | 1055 |
| Кирпич облицовочный | 880 |
| Кирпич огнеупорный полукислый | 885 |
| Кирпич силикатный | 750…840 |
| Кирпич строительный | 800 |
| Кирпич трепельный | 710 |
| Кирпич шамотный | 930 |
| Кладка «Поротон» | 900 |
| Кладка бутовая из камней средней плотности | 880 |
| Кладка газосиликатная | 880 |
| Кладка из глиняного обыкновенного кирпича | 880 |
| Кладка из керамического пустотного кирпича | 880 |
| Кладка из силикатного кирпича | 880 |
| Кладка из трепельного кирпича | 880 |
| Кладка из шлакового кирпича | 880 |
| Кокс порошкообразный | 1210 |
| Корунд | 711 |
| Краска масляная (эмаль) | 650…2000 |
| Кремний | 714 |
| Лава вулканическая | 840 |
| Латунь | 400 |
| Лед из тяжелой воды | 2220 |
| Лед при температуре 0°С | 2150 |
| Лед при температуре -100°С | 1170 |
| Лед при температуре -20°С | 1950 |
| Лед при температуре -60°С | 1700 |
| Линолеум | 1470 |
| Листы асбестоцементные плоские | 840 |
| Листы гипсовые обшивочные (сухая штукатурка) | 840 |
| Лузга подсолнечная | 1500 |
| Магнетит | 586 |
| Малахит | 740 |
| Маты и полосы из стекловолокна прошивные | 840 |
| Маты минераловатные прошивные и на синтетическом связующем | 840 |
| Мел | 800…880 |
| Миканит | 250 |
| Мипора | 1420 |
| Мрамор (облицовка) | 880 |
| Настил палубный | 1100 |
| Нафталин | 1300 |
| Нейлон | 1600 |
| Неопрен | 1700 |
| Пакля | 2300 |
| Парафин | 2890 |
| Паркет дубовый | 1100 |
| Паркет штучный | 880 |
| Паркет щитовой | 880 |
| Пемзобетон | 840 |
| Пенобетон | 840 |
| Пенопласт ПХВ-1 и ПВ-1 | 1260 |
| Пенополистирол | 1340 |
| Пенополистирол «Пеноплекс» | 1600 |
| Пенополиуретан | 1470 |
| Пеностекло или газостекло | 840 |
| Пергамин | 1680 |
| Перекрытие армокерамическое с бетонным заполнением без штукатурки | 850 |
| Перекрытие из железобетонных элементов со штукатуркой | 860 |
| Перекрытие монолитное плоское железобетонное | 840 |
| Перлитобетон | 840 |
| Перлитопласт-бетон | 1050 |
| Перлитофосфогелевые изделия | 1050 |
| Песок для строительных работ | 840 |
| Песок речной мелкий | 700…840 |
| Песок речной мелкий (влажный) | 2090 |
| Песок сахарный | 1260 |
| Песок сухой | 800 |
| Пихта | 2700 |
| Пластмасса полиэфирная | 1000…2300 |
| Плита пробковая | 1850 |
| Плиты алебастровые | 750 |
| Плиты древесно-волокнистые и древесно-стружечные (ДСП, ДВП) | 2300 |
| Плиты из гипса | 840 |
| Плиты из резольноформальдегидного пенопласта | 1680 |
| Плиты из стеклянного штапельного волокна на синтетическом связующем | 840 |
| Плиты камышитовые | 2300 |
| Плиты льнокостричные изоляционные | 2300 |
| Плиты минераловатные повышенной жесткости | 840 |
| Плиты минераловатные полужесткие на крахмальном связующем | 840 |
| Плиты торфяные теплоизоляционные | 2300 |
| Плиты фибролитовые и арболит на портландцементе | 2300 |
| Покрытие ковровое | 1100 |
| Пол гипсовый бесшовный | 800 |
| Поливинилхлорид (ПВХ) | 920…1200 |
| Поликарбонат (дифлон) | 1100…1120 |
| Полиметилметакрилат | 1200…1650 |
| Полипропилен | 1930 |
| Полистирол УПП1, ППС | 900 |
| Полистиролбетон | 1060 |
| Полихлорвинил | 1130…1200 |
| Полихлортрифторэтилен | 920 |
| Полиэтилен высокой плотности | 1900…2300 |
| Полиэтилен низкой плотности | 1700 |
| Портландцемент | 1130 |
| Пробка | 2050 |
| Пробка гранулированная | 1800 |
| Раствор гипсовый затирочный | 900 |
| Раствор гипсоперлитовый | 840 |
| Раствор гипсоперлитовый поризованный | 840 |
| Раствор известково-песчаный | 840 |
| Раствор известковый | 920 |
| Раствор сложный (песок, известь, цемент) | 840 |
| Раствор цементно-перлитовый | 840 |
| Раствор цементно-песчаный | 840 |
| Раствор цементно-шлаковый | 840 |
| Резина мягкая | 1380 |
| Резина пористая | 2050 |
| Резина твердая обыкновенная | 1350…1400 |
| Рубероид | 1500…1680 |
| Сера | 715 |
| Сланец | 700…1600 |
| Слюда | 880 |
| Смола эпоксидная | 800…1100 |
| Снег лежалый при 0°С | 2100 |
| Снег свежевыпавший | 2090 |
| Сосна и ель | 2300 |
| Сосна смолистая 15% влажности | 2700 |
| Стекло зеркальное (зеркало) | 780 |
| Стекло кварцевое | 890 |
| Стекло лабораторное | 840 |
| Стекло обыкновенное, оконное | 670 |
| Стекло флинт | 490 |
| Стекловата | 800 |
| Стекловолокно | 840 |
| Стеклопластик | 800 |
| Стружка деревянная прессованая | 1080 |
| Текстолит | 1470…1510 |
| Толь | 1680 |
| Торф | 1880 |
| Торфоплиты | 2100 |
| Туф (облицовка) | 750…880 |
| Туфобетон | 840 |
| Уголь древесный | 960 |
| Уголь каменный | 1310 |
| Фанера клееная | 2300…2500 |
| Фарфор | 750…1090 |
| Фибролит (серый) | 1670 |
| Циркон | 670 |
| Шамот | 825 |
| Шифер | 750 |
| Шлак гранулированный | 750 |
| Шлак котельный | 700…750 |
| Шлакобетон | 800 |
| Шлакопемзобетон (термозитобетон) | 840 |
| Шлакопемзопено- и шлакопемзогазобетон | 840 |
| Штукатурка гипсовая | 840 |
| Штукатурка из полистирольного раствора | 1200 |
| Штукатурка известковая | 950 |
| Штукатурка известковая с каменной пылью | 920 |
| Штукатурка перлитовая | 1130 |
| Штукатурка фасадная с полимерными добавками | 880 |
| Шунгизитобетон | 840 |
| Щебень и песок из перлита вспученного | 840 |
| Щебень из доменного шлака, шлаковой пемзы и аглопорита | 840 |
| Эбонит | 1430 |
| Эковата | 2300 |
| Этрол | 1500…1800 |
Таблица удельной теплоемкости пищевых продуктов
В таблице приведены значения средней удельной теплоемкости пищевых продуктов (овощей, фруктов, мяса, рыбы, хлеба, вина и т. д.) в диапазоне температуры 5…20°С и нормальном атмосферном давлении.
д.) в диапазоне температуры 5…20°С и нормальном атмосферном давлении.
| Продукты | C, Дж/(кг·К) |
|---|---|
| Абрикосы | 3770 |
| Ананасы | 3684 |
| Апельсины | 3730 |
| Арбуз | 3940 |
| Баклажаны | 3935 |
| Брюква | 3810 |
| Ветчина | 2140 |
| Вино крепленое | 3690 |
| Вино сухое | 3750 |
| Виноград | 3550 |
| Вишня | 3650 |
| Говядина и баранина жирная | 2930 |
| Говядина и баранина маложирная | 3520 |
| Горох | 3684 |
| Грибы свежие | 3894 |
| Груши | 3680 |
| Дрожжи прессованные | 1550…3516 |
| Дыни | 3850 |
| Ежевика | 3642 |
| Земляника | 3684 |
| Зерно пшеничное | 1465…1549 |
| Кабачки | 3900 |
| Капуста | 3940 |
| Картофель | 3430 |
| Клубника | 3810 |
| Колбасы | 1930…2810 |
| Крыжовник | 3890 |
| Лимоны | 3726 |
| Лук | 2638 |
| Макароны не приготовленные | 1662 |
| Малина | 3480 |
| Мандарины | 3770 |
| Маргарин сливочный | 2140…3182 |
| Масло анисовое | 1846 |
| Масло мятное | 2080 |
| Масло сливочное | 2890…3100 |
| Масло сливочное топленое | 2180 |
| Мед | 2300…2428 |
| Молоко сухое | 1715…2090 |
| Морковь | 3140 |
| Мороженое (при -10С) | 2175 |
| Мука | 1720 |
| Огурцы | 4060 |
| Пастила | 2090 |
| Патока | 2512…2700 |
| Перец сладкий | 3935 |
| Печенье | 2170 |
| Помидоры | 3980 |
| Пряники | 1800…1930 |
| Редис | 3970 |
| Рыба жирная | 2930 |
| Рыба нежирная | 3520 |
| Салат зеленый | 4061 |
| Сало топленое | 2510 |
| Сахар кусковой | 1340 |
| Сахарный песок | 720 |
| Свекла | 3340 |
| Свинина жирная | 260 |
| Свинина нежирная | 3010 |
| Слива | 3750 |
| Сметана | 3010 |
| Смородина черная | 3740 |
| Сода | 2256 |
| Соль поваренная (2% влажности) | 920 |
| Спаржа | 3935 |
| Сыр жирный | 2430 |
| Творог | 3180 |
| Телятина жирная | 3180 |
| Телятина нежирная | 3520 |
| Тесто заварное | 2910 |
| Тыква | 3977 |
| Хлеб (корка) | 1680 |
| Хлеб (мякиш) | 2800 |
| Черешня | 3770 |
| Чернослив | 3181 |
| Чеснок | 3140 |
| Шоколад | 2340…2970 |
| Шпинат | 3977 |
| Яблоки | 3760 |
| Яйцо куриное | 3180 |
Кроме таблиц удельной теплоемкости, вы также можете ознакомиться с подробнейшей таблицей плотности веществ и материалов, которая содержит данные по величине плотности более 500 веществ (металлов, пластика, резины, продуктов, стекла и др. ).
).
Источники:
- Исаченко В. П., Осипова В. А., Сукомел А. С. Теплопередача. Учебник для вузов, изд. 3-е, перераб. и доп. — М.: «Энергия», 1975.
- Тепловые свойства металлов и сплавов. Справочник. Лариков Л. Н., Юрченко Ю. Ф. — Киев: Наукова думка, 1985. — 439 с.
- Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др. Под ред. И. С. Григорьева — М.: Энергоатомиздат, 1991. — 1232 с.
- Еремкин А. И., Королева Т. И. Тепловой режим зданий: Учебное пособие. — М.: Издательство ACB, 2000 — 368 с.
- Кириллов П. Л., Богословская Г. П. Тепломассобмен в ядерных энергетических установках: Учебник для вузов.
- Михеев М. А., Михеева И. М. Основы теплопередачи. Изд. 2-е, стереотип. М.: «Энергия», 1977. — 344 с. с ил.
- Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
- Франчук А. У. Таблицы теплотехнических показателей строительных материалов, М.: НИИ строительной физики, 1969 — 142 с.

- Добрынин В. М., Вендельштейн Б. Ю., Кожевников Д. А. Петрофизика: Учеб. для вузов. 2-ое изд. перераб. и доп. под редакцией доктора физико-математических наук Д. А. Кожевникова — М.: ФГУП Издательство «Нефть и газ» РГУ нефти и газа им. И.М. Губкина, 2004. — 368 с., ил.
- В. Блази. Справочник проектировщика. Строительная физика. М.: Техносфера, 2005. — 536 с.
- Енохович А. С. Справочник по физике. М.: «Просвещение», 1978. — 415 с. с ил.
- Строительная теплотехника СНиП II-3-79. Минстрой России — Москва 1995.
- Мустафаев Р. А. Теплофизические свойства углеводородов при высоких параметрах состояния. М.: Энергоатомиздат, 1991. — 312 с.
- Новиченок Н. Л., Шульман З. П. Теплофизические свойства полимеров. Минск, «Наука и техника» 1971. — 120 с.
- Шелудяк Ю. Е., Кашпоров Л. Я. и др. Теплофизические свойства компонентов горючих систем. М., 1992. — 184 с.
Теплоемкость
Engineering ToolBox – Ресурсы, инструменты и базовая информация для проектирования и проектирования технических приложений!
Количество тепла, необходимое для изменения температуры вещества на один градус.

Рекламные ссылки
Теплоемкость – C – характеристика объекта – количество тепла, необходимое для изменения его температуры на один градус.
- Теплоемкость выражается в единицах энергии на градус.
Количество тепла, переданного для нагревания объекта, можно выразить следующим образом:
Q = C dt (1)
, где
Q = количество подведенного тепла (Дж, БТЕ)
C = теплоемкость системы или объекта (Дж/К, БТЕ/ или F)
dt = изменение температуры (K, C ° , o F)
Единица СИ для теплоемкости Дж/К (джоуль на кельвин). В английской системе единицами измерения являются британские тепловые единицы на фунт на градус Фаренгейта (Btu/ или F). В некоторых случаях вместо Дж используются кДж или кал и ккал.
Никогда не используйте табличные значения теплоемкости без проверки единиц измерения фактических значений!
Удельная теплоемкость ( c ) — это количество тепла, необходимое для изменения температуры единицы массы вещества на один градус. Удельная теплоемкость является более распространенным термином для того же самого.
Удельная теплоемкость является более распространенным термином для того же самого.
Количество теплоты, переданное массе, можно выразить как
dQ = m c dt (1)
где
dQ = подведенное тепло (Дж, кДж БТЕ)
m = масса единицы (г, кг, фунт)
c = удельная теплоемкость (Дж/г K, кДж/кг o C, кДж/кг K, БТЕ/фунт o F)
dt = изменение температуры (K, C 90 024° , o F)
(1) можно перевести в выражение удельной теплоемкости как:
c = dQ / m dt (1b)
Пример: требуется 0,45 джоуля тепла, чтобы поднять один грамм железа. на один градус Кельвина.
Загрузите и распечатайте Подведенное тепло в зависимости от удельной теплоемкости и изменения температуры в диаграмме
Удельная теплоемкость газов
Существует два определения удельной теплоемкости для паров и газов:
c p = (δh / δT) p – Удельная теплоемкость при постоянном давлении (Дж/гK)
c v = (δh / δT) v – Удельная Тепло при постоянном объеме ( Дж/гК)
Для твердых и жидких тел, c p = c v
Воспользуйтесь ссылками, чтобы увидеть табличные значения удельной полуметаллы, обычные твердые тела и другие обычные вещества.
Газовая постоянная
Индивидуальная газовая постоянная R может быть выражена как
R = c p – c v (2)
Коэффициент удельной теплоемкости (3)
Молярная теплоемкость ( C p ) – количество теплоты, необходимое для повышения температуры одного моля вещества на один градус при постоянном давлении.
Выражается в джоулях на моль на градусы Кельвина (или Цельсия), Дж/(моль К) .
Пример: Молярная теплоемкость железа равна 25,10 Дж/(моль·К), что означает, что требуется 25,10 Дж тепла, чтобы поднять 1 моль железа на 1 градус Кельвина.
Табличные значения молярной теплоемкости, C p, многих органических и неорганических веществ можно найти в Стандартная энтальпия образования, Гиббсовская свободная энергия образования, энтропия и молярная теплоемкость органических веществ и Стандартное состояние и энтальпия образование, свободная энергия Гиббса образования, энтропия и теплоемкость вместе с ΔH° f , ΔG° f и S° для тех же веществ при 25°C.
Перевод удельной теплоемкости в молярную теплоемкость
Удельную теплоемкость можно рассчитать по молярной теплоемкости и наоборот:
c p = C p / M и
C 90 136 р = с р . M
где
c p = удельная теплоемкость
C p = молярная теплоемкость емкость
M = молярная масса фактического вещества (г/моль).
Пример: Метанол (с молекулярной формулой Ch4OH) имеет молярную теплоемкость C p , равную 81,1 Дж/(моль·К). Какова удельная теплоёмкость, c p ?
Сначала вычисляем (или находим) молярную массу метанола: 1*12,01 г/моль C + 4*1,008 г/моль H + 1*16,00 г/моль O = 32,04 г/моль CH 3 OH
Тогда удельная теплоемкость метанола: c p = 81,8 Дж/(мольК) / 32,04 г/моль = 2,53 Дж/(г·К)
Перевод общеупотребительных единиц
- 1 БТЕ/фунт м o F = 4186,8 Дж/кг K = 1 ккал/кг o C
- Online конвертер единиц удельной теплоемкости
Пример – Нагрев алюминия
2 кг алюминия нагревается от 20 o C до 100 o C . Удельная теплоемкость алюминия 0,91 кДж/кг 0 С , а необходимое количество тепла можно рассчитать как
Удельная теплоемкость алюминия 0,91 кДж/кг 0 С , а необходимое количество тепла можно рассчитать как
dQ = (2 кг) (0,91 кДж/кг 0 Кл) ((100 o Кл) – (20 o Кл))
900 02 = 145,6 (кДж)Пример – нагревательная вода
Один литр воды нагревается от 0 o C до кипения 100 o C 9 0012 . Удельная теплоемкость воды составляет 4,19 кДж/кг 0 C , а необходимое количество тепла можно рассчитать как
dQ = (1 литр) (1 кг/литр) (4,19 кДж/кг 0 C) ((100 o C) – (0 o C))
900 11 = 419 (кДж )
= 419 (кВт·с) (1/3600 ч/с)
= 0,12 кВт·ч
- Запас энергии в нагретой воде – кВт·ч 9 0018
Рекламные ссылки
Похожие темы
Основы
Система СИ, конвертеры величин, физические константы, чертежные масштабы и многое другое.
Свойства материалов
Свойства материалов газов, жидкостей и твердых тел — плотность, теплоемкость, вязкость и т. д.Термодинамика
Работа, тепловые и энергетические системы.
Связанные документы
Ацетон – теплофизические свойства
Химические, физические и термические свойства ацетона, также называемого 2-пропаноном, диметилкетоном и пироуксусной кислотой. Фазовая диаграмма включена.Аммиак – удельная теплоемкость в зависимости от температуры и давления
Онлайн-калькулятор, рисунки и таблицы, показывающие удельную теплоемкость C P и C V газообразного и жидкого аммиака при температуре от -73 до 425°C (от -100 до 800°F) при давлении от 1 до 100 бар абс. (14,5–1450 фунтов на кв. дюйм) — единицы СИ и имперские единицы.Бензол. Теплофизические свойства
Химические, физические и термические свойства бензола, также называемого бензолом. Фазовая диаграмма включена.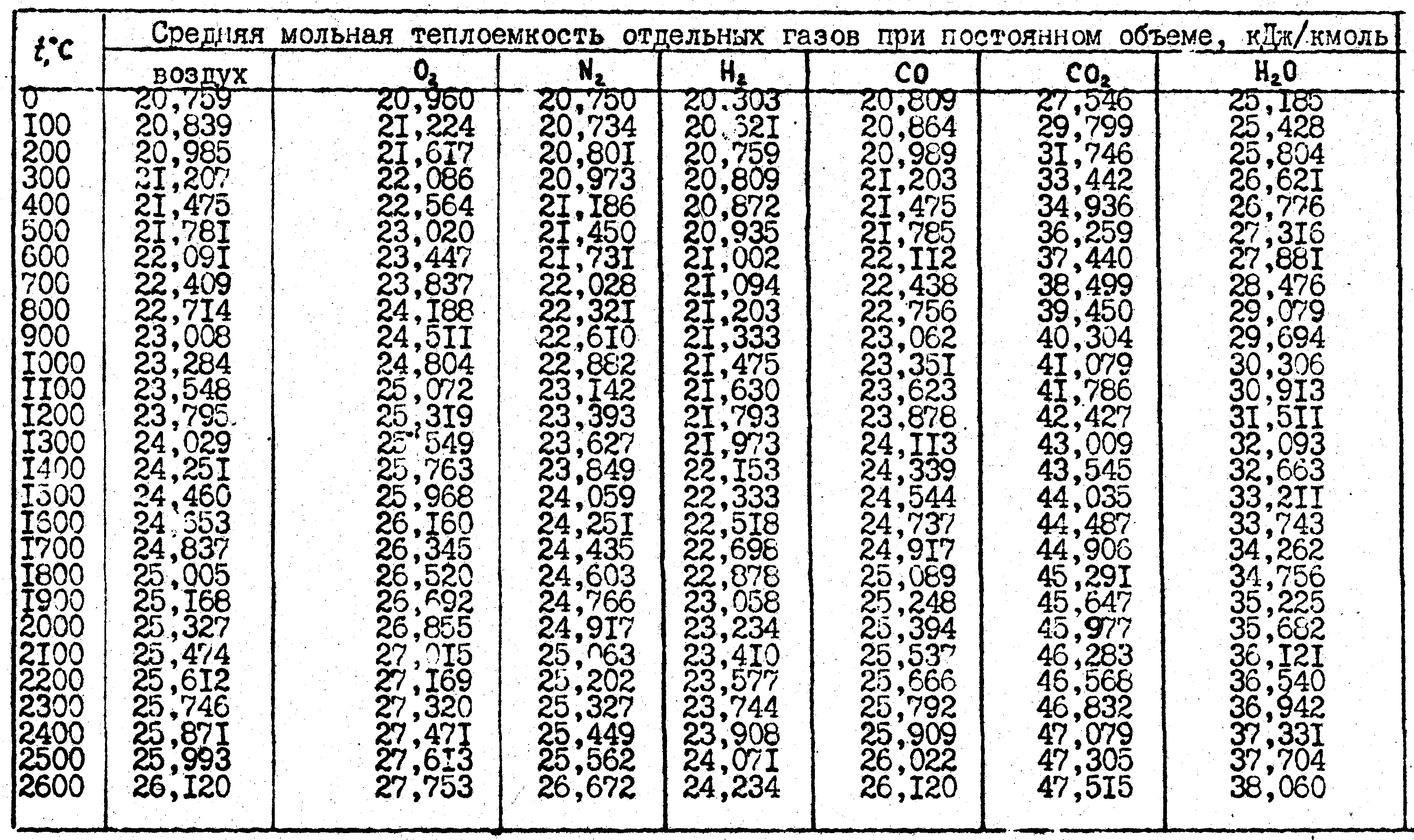
Бутан — удельная теплоемкость в зависимости от температуры и давления
Онлайн-калькуляторы, рисунки и таблицы, показывающие удельную теплоемкость, Cp и Cv, газообразного и жидкого бутана, C 4 H 10 , при различных температуре и давлении, SI и Имперские единицы.Теплота сгорания
Теплота сгорания (энергосодержание) некоторых обычных веществ – с примерами расчета теплоты сгорания.Энергия, аккумулированная в нагретой воде – кВтч
Количество тепловой энергии, запасенной в нагретой воде.Этилен – теплофизические свойства
Химические, физические и термические свойства этилена, также называемого этеном, ацетеном и маслянистым газом. Фазовая диаграмма включена.Продукты питания и пищевые продукты – Удельная теплоемкость
Удельная теплоемкость обычных продуктов питания, таких как яблоки, окунь, говядина, свинина и многие другие.Газы. Коэффициенты удельной теплоемкости
Коэффициенты удельной теплоемкости газов при постоянном давлении и объемных процессах.
Газы – удельная теплоемкость и индивидуальные газовые постоянные
Удельная теплоемкость при постоянном объеме, удельная теплоемкость при постоянном давлении, удельная теплоемкость и отдельная газовая постоянная – R – распространенные газы, такие как аргон, воздух, эфир, азот и многие другие.Теплота, работа и энергия
Теплота, работа и энергия.Тяжелая вода – теплофизические свойства
Термодинамические свойства тяжелой воды (D 2 O), такие как плотность, температура плавления, температура кипения, скрытая теплота плавления, скрытая теплота испарения, критическая температура и другие.Жидкости и жидкости – Удельная теплоемкость
Удельная теплоемкость некоторых обычных жидкостей и жидкостей – ацетона, масла, парафина, воды и многих других.Металлы – удельная теплоемкость
Удельная теплоемкость широко используемых металлов, таких как алюминий, железо, ртуть и многие другие – в имперских единицах и единицах СИ.
Азот – Температуропроводность в зависимости от температуры и давления
Рисунки и таблицы, показывающие температуропроводность азота при различных температуре и давлении, СИ и имперские единицы.Фенолы, спирты и карбоновые кислоты – значения pKa
Для кислородсодержащих органических соединений приводятся: pKa (отрицательный логарифм константы диссоциации кислоты), молекулярная структура, молярная масса, плотность, температуры плавления и кипения.Твердые вещества – удельная теплоемкость
Обычные твердые вещества, такие как кирпич, цемент, стекло и многие другие, и их удельная теплоемкость – в имперских единицах и единицах СИ.Удельная теплоемкость обычных веществ
Удельная теплоемкость таких продуктов, как влажный шлам, гранит, песчаная глина, кварцевый песок и др.Стандартная энтальпия образования, энергия Гиббса образования, энтропия и молярная теплоемкость органических веществ
Стандартная энтальпия образования, энергия Гиббса образования, энтропия и молярная теплоемкость сведены в таблицы для более чем ста органических веществ.
Стандартное состояние и энтальпия образования, свободная энергия Гиббса образования, энтропия и теплоемкость
Определение и объяснение терминов стандартное состояние и стандартная энтальпия образования с перечислением значений стандартной энтальпии и свободной энергии Гиббса образования, а также стандартной энтропии и молярной теплоемкости 370 неорганических соединений.Ключевые термодинамические значения Согласованные на международном уровне
Согласованные на международном уровне, внутренне согласованные значения термодинамических свойств (стандартная энтальпия образования, энтропия и [H°(298)-H°(0)]) ключевых химических веществ.Термодинамические термины – функции и отношения
Общие термодинамические термины и функции – потенциальная энергия, кинетическая энергия, тепловая или внутренняя энергия, химическая энергия, ядерная энергия и многое другое.Вода – удельная теплоемкость в зависимости от температуры
Онлайн-калькулятор, рисунки и таблицы, показывающие удельную теплоемкость жидкой воды при постоянном объеме или постоянном давлении при температуре от 0 до 360 °C (32-700 °F) – единицы СИ и имперские единицы.
Вода – теплофизические свойства
Тепловые свойства воды при различных температурах, такие как плотность, температура замерзания, температура кипения, скрытая теплота плавления, скрытая теплота испарения, критическая температура и т.д.
Рекламные ссылки
Engineering ToolBox — Расширение SketchUp — 3D-моделирование онлайн!
Добавляйте стандартные и настраиваемые параметрические компоненты, такие как балки с полками, пиломатериалы, трубопроводы, лестницы и т. д., в свою модель Sketchup с помощью Engineering ToolBox — расширение SketchUp, которое можно использовать с потрясающими, интересными и бесплатными приложениями SketchUp Make и SketchUp Pro. . Добавьте расширение Engineering ToolBox в свой SketchUp из хранилища расширений SketchUp Pro Sketchup!
Перевести
О Engineering ToolBox!
Мы не собираем информацию от наших пользователей. Подробнее о
- Политика конфиденциальности Engineering ToolBox
Реклама в ToolBox
Если вы хотите продвигать свои продукты или услуги в Engineering ToolBox, используйте Google Adwords. Вы можете настроить таргетинг на Engineering ToolBox с помощью управляемых мест размещения AdWords.
Вы можете настроить таргетинг на Engineering ToolBox с помощью управляемых мест размещения AdWords.
Цитирование
Эту страницу можно цитировать как
- Инженерный набор инструментов (2003 г.). Теплоемкость . [онлайн] Доступно по адресу: https://www.engineeringtoolbox.com/heat-capacity-d_338.html [День, месяц, год].
Изменить дату доступа.
. .закрыть
Сделать ярлык на главный экран?
Удельная теплоемкость и вода
Тепло – это форма энергии, часто называемая тепловой энергией. Энергия может быть преобразована из одной формы в другую (блендер превращает электрическую энергию в механическую), но ее нельзя ни создать, ни уничтожить; скорее, энергия сохраняется.
Содержание
- Что такое теплоемкость?
- Что такое удельная теплоемкость?
- Удельная теплоемкость воды
- Часто задаваемые вопросы – Часто задаваемые вопросы
Что такое теплоемкость?
Теплоемкость , сП, представляет собой количество теплоты, необходимое для изменения теплосодержания 1 моля материала ровно на 1°C.
Согласно основам термодинамики, чем выше температура материала, тем большей тепловой энергией он обладает. Кроме того, при данной температуре чем больше данного вещества, тем большей полной тепловой энергией будет обладать материал.
Изображение удельной теплоемкости воды
На атомарном уровне поглощенное тепло заставляет атомы твердого тела вибрировать, как если бы они были связаны друг с другом посредством пружин. С повышением температуры энергия колебаний увеличивается. В металле это единственно возможное движение. В жидкости или газе поглощенное тепло заставляет атомы в молекуле вибрировать, а сама молекула вращаться и перемещаться с места на место. Поскольку в жидкостях и газах больше возможностей «аккумулировать» энергию, их теплоемкость больше, чем у металлов.
Рекомендуемые видео
Что такое удельная теплоемкость?
Удельная теплоемкость , Csp, представляет собой количество теплоты, необходимое для изменения теплосодержания ровно 1 грамма материала ровно на 1°C.
Удельная теплотворная способность может быть определена следующим образом: когда два материала, каждый из которых изначально имеет разную температуру, соприкасаются друг с другом, тепло всегда переходит от более теплого материала к более холодному до тех пор, пока оба материала не достигнут одинаковой температуры. . Согласно закону сохранения энергии теплота, полученная изначально более холодным материалом, должна быть равна теплоте, отданной изначально более теплым материалом.
Мы знаем, что когда тепловая энергия поглощается веществом, его температура увеличивается. Если одно и то же количество теплоты дается равным массам различных веществ, то наблюдается, что повышение температуры для каждого вещества различно. Это связано с тем, что разные вещества обладают разной теплоемкостью. Таким образом, теплоемкостью вещества называется количество теплоты, необходимое для повышения температуры всего вещества на один градус. Если масса вещества равна единице, то теплоемкость называется Удельная теплоемкость или Удельная теплоемкость .
Формула удельной теплоемкости
- Q = количество теплоты, поглощаемой телом
- м = масса тела
- ∆t = Повышение температуры
- C = Удельная теплоемкость вещества зависит от природы материала вещества.
- Единица удельной теплоемкости в системе СИ равна Дж кг -1 К -1 .
Единица измерения удельной теплоемкости
| Теплоемкость = удельная теплоемкость x масса |
Его единица измерения в системе СИ равна Дж К -1 .
Удельная теплоемкость воды
Для жидкости при комнатной температуре и давлении значение удельной теплоемкости (Cp) составляет приблизительно 4,2 Дж/г°C. Это означает, что требуется 4,2 Дж энергии, чтобы поднять 1 грамм воды на 1 градус Цельсия. Это значение для Cp на самом деле довольно велико. Это (1 кал/г.град) и есть удельная теплоемкость воды в жидком состоянии или удельная теплоемкость жидкой воды.
Это (1 кал/г.град) и есть удельная теплоемкость воды в жидком состоянии или удельная теплоемкость жидкой воды.
Одна калория = 4,184 Дж; 1 джоуль = 1 кг(м) 2 (с) -2 = 0,23
36 калорияУдельная теплоемкость водяного пара при комнатной температуре также выше, чем у большинства других материалов. Для водяного пара при комнатной температуре и давлении значение удельной теплоемкости (Cp) составляет приблизительно 1,9 Дж/г°C.
Как и у большинства жидкостей, температура воды увеличивается по мере того, как она поглощает тепло, и уменьшается по мере того, как тепло выделяется. Однако температура жидких водопадов и повышается медленнее, чем у большинства других жидкостей. Можно сказать, что вода поглощает тепло без немедленного повышения температуры. Он также сохраняет свою температуру намного дольше, чем другие вещества.
Мы используем это свойство воды в нашем организме для поддержания постоянной температуры тела. Если бы вода имела более низкое значение Cуд, то было бы много случаев перегрева и недогрева.
Если бы вода имела более низкое значение Cуд, то было бы много случаев перегрева и недогрева.
Удельная теплоемкость Пояснение
Мы можем объяснить причину высокой удельной теплоемкости воды за счет водородных связей. Чтобы повысить температуру воды с множеством соединенных водородных связей, молекулы должны колебаться. Из-за наличия такого большого количества водородных связей требуется большее количество энергии, чтобы заставить молекулы воды разорваться, вибрируя их.
Точно так же, чтобы горячая вода остыла, требуется некоторое время. По мере рассеивания тепла температура снижается, а колебательное движение молекул воды замедляется. Выделяемое тепло противодействует охлаждающему эффекту потери тепла жидкой водой.
Часто задаваемые вопросы – Часто задаваемые вопросы
Q1
Как вы измеряете удельную теплоемкость?
Удельная тепловая эффективность измеряется количеством тепловой энергии, необходимой для нагревания одного грамма продукта на один градус Цельсия. Удельная тепловая мощность воды составляет 4,2 Дж на грамм на градус Цельсия или 1 калорию на грамм на градус Цельсия.
Удельная тепловая мощность воды составляет 4,2 Дж на грамм на градус Цельсия или 1 калорию на грамм на градус Цельсия.
Q2
В чем преимущество теплоемкости воды?
Поскольку вода обладает высокой теплоемкостью, для повышения температуры на один градус требуется больше энергии. Солнце излучает более или менее постоянный уровень энергии, который быстрее нагревает песок и воду.
Q3
В чем разница между теплоемкостью и удельной теплоемкостью?
Удельная теплоемкость – это количество тепла, необходимое для повышения температуры вещества на 1 градус Цельсия. Точно так же теплоемкость – это отношение между энергией, переданной веществу, и соответствующим повышением его температуры.
Q4
Почему удельная теплоемкость воды выше, чем металла?
Это связано с тем, что удельная тепловая эффективность металлической ложки намного меньше, чем у жидкости для супа. Вода имеет самую высокую удельную теплоемкость среди всех жидкостей.
 /3
/3
