Таблицы удельной теплоемкости веществ: газов, жидкостей, металлов, продуктов
Представлены таблицы удельной теплоемкости веществ: газов, металлов, жидкостей, строительных и теплоизоляционных материалов, а также пищевых продуктов — более 400 веществ и материалов.
Перечень таблиц:
- Удельная теплоемкость газов
- Удельная теплоемкость некоторых металлов и сплавов
- Удельная теплоемкость жидкостей
- Удельная теплоемкость твердых веществ
- Удельная теплоемкость пищевых продуктов
Удельной теплоемкостью вещества называется отношение количества тепла, сообщенного единице массы этого вещества в каком-либо процессе, к соответствующему изменению его температуры.
Удельная теплоемкость веществ зависит от их химического состава, термодинамического состояния и способа сообщения им тепла. В Международной системе единиц эта величина измеряется в Дж/(кг·К).
Необходимо отметить, что экспериментальное определение удельной теплоемкости жидкостей и газов производится при постоянном давлении или при постоянном объеме.
Для твердых веществ теплоемкости Cp и Cv не различаются. Кроме того, по отношению к твердым телам, помимо удельной массовой теплоемкости применяются также удельная атомная и молярная теплоемкости.
Таблица удельной теплоемкости газов
В таблице приведена удельная теплоемкость газов Cp при температуре 20°С и нормальном атмосферном давлении (101325 Па).
| Газы | Cp, Дж/(кг·К) |
|---|---|
| Азот N2 | 1051 |
| Аммиак NH3 | 2244 |
| Аргон Ar | 523 |
| Ацетилен C2H2 | 1683 |
| Водород H2 | 14270 |
| Воздух | 1005 |
| Гелий He | 5296 |
| Кислород O2 | 913 |
| Криптон Kr | 251 |
| Ксенон Xe | 159 |
| Метан CH4 | 2483 |
| Неон Ne | 1038 |
| Оксид азота N2O | 913 |
| Оксид азота NO | 976 |
| Оксид серы SO2 | 625 |
| Оксид углерода CO | 1043 |
| Пропан C3H8 | 1863 |
| Сероводород H2S | 1026 |
| Углекислый газ CO2 | 837 |
| Хлор Cl | 520 |
| Этан C2H6 | 1729 |
| Этилен C2H4 | 1528 |
Таблица удельной теплоемкости некоторых металлов и сплавов
В таблице даны значения удельной теплоемкости некоторых распространенных металлов и сплавов при температуре 20°С.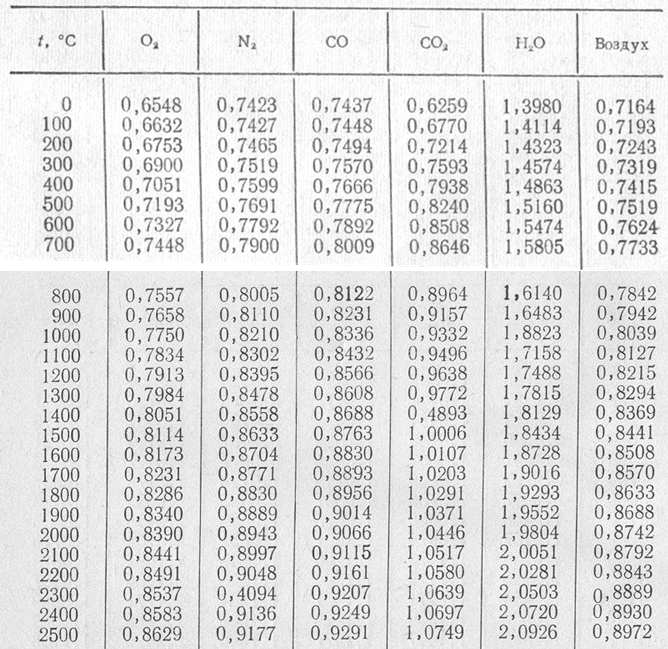 Значения теплоемкости большинства металлов при других температурах вы можете найти в этой таблице.
Значения теплоемкости большинства металлов при других температурах вы можете найти в этой таблице.
| Металлы и сплавы | C, Дж/(кг·К) |
|---|---|
| Алюминий Al | 897 |
| Бронза алюминиевая | 420 |
| Бронза оловянистая | 380 |
| Вольфрам W | 134 |
| Дюралюминий | 880 |
| Железо Fe | 452 |
| Золото Au | 129 |
| Константан | 410 |
| Латунь | 378 |
| Манганин | 420 |
| Медь Cu | 383 |
| Никель Ni | 443 |
| Нихром | 460 |
| Олово Sn | 228 |
| Платина Pt | 133 |
| Ртуть Hg | 139 |
| Свинец Pb | 128 |
| Серебро Ag | 235 |
| Сталь стержневая арматурная | 482 |
| Сталь углеродистая | 468 |
| Сталь хромистая | 460 |
| Титан Ti | 520 |
| Уран U | 116 |
| Цинк Zn | 385 |
| Чугун белый | 540 |
| Чугун серый | 470 |
Таблица удельной теплоемкости жидкостей
В таблице представлены значения удельной теплоемкости Cp распространенных жидкостей при температуре 10…25°С и нормальном атмосферном давлении.
| Жидкости | |
|---|---|
| Азотная кислота (100%-ная) NH3 | 1720 |
| Анилин C6H5NH2 | 2641 |
| Антифриз (тосол) | 2990 |
| Ацетон C3H6O | 2160 |
| Бензин | 2090 |
| Бензин авиационный Б-70 | 2050 |
| Бензол C6H6 | 1050 |
| Вода H2O | 4182 |
| Вода морская | 3936 |
| Вода тяжелая D2O | 4208 |
| Водка (40% об.) | 3965 |
| Водный раствор хлорида натрия (25%-ный) | 3300 |
| Газойль | 1900 |
| Гидроксид аммония | 4610 |
| Глицерин C3H5(OH)3 | 2430 |
| Даутерм | 1590 |
| Карборан C2 H12B10 | 1720 |
| Керосин | 2085…2220 |
| Кефир | 3770 |
| Мазут | 2180 |
| Масло АМГ-10 | 1840 |
| Масло ВМ-4 | 1480 |
| Масло касторовое | 2219 |
| Масло кукурузное | 1733 |
| Масло МС-20 | 2030 |
| Масло подсолнечное рафинированное | 1775 |
| Масло ТМ-1 | 1640 |
| Масло трансформаторное | 1680 |
| Масло хлопковое рафинированное | 1737 |
| Масло ХФ-22 | 1640 |
| Молоко сгущенное с сахаром | 3936 |
| Молоко цельное | 3906 |
| Нефть | 2100 |
| Парафин жидкий (при 50С) | 3000 |
| Пиво | 3940 |
| Серная кислота (100%-ная) H2SO4 | 1380 |
| Сероуглерод CS2 | 1000 |
| Силикон | 2060 |
| Скипидар | 1800 |
| Сливки (35% жирности) | 3517 |
| Сок виноградный | 2800…3690 |
| Спирт метиловый (метанол) CH3OH | 2470 |
| Спирт этиловый (этанол) C2H5OH | 2470 |
| Сыворотка молочная | 4082 |
| Толуол C7H8 | 1130 |
| Топливо дизельное (солярка) | 2010 |
| Топливо реактивное | 2005 |
| Уротропин C6H12N4 | 1470 |
| Фреон-12 CCl2F2 | 840 |
| Эфир этиловый C4H10O | 2340 |
Таблица удельной теплоемкости твердых веществ
В таблице дана удельная теплоемкость твердых веществ: стройматериалов (песка, асфальта и т.
| Строительные, теплоизоляционные и другие материалы | C, Дж/(кг·К) |
|---|---|
| АБС пластик | 1300…2300 |
| Аглопоритобетон и бетон на топливных (котельных) шлаках | 840 |
| Алмаз | 502 |
| Аргиллит | 700…1000 |
| Асбест волокнистый | 1050 |
| Асбестоцемент | 1500 |
| Асботекстолит | 1670 |
| Асбошифер | 837 |
| Асфальт | 920…2100 |
| Асфальтобетон | 1680 |
| Аэрогель (Aspen aerogels) | 700 |
| 850…920 | |
| Барит | 461 |
| Береза | 1250 |
| Бетон | 710…1130 |
| Битумоперлит | 1130 |
| Битумы нефтяные строительные и кровельные | 1680 |
| Бумага | 1090…1500 |
| Вата минеральная | 920 |
| Вата стеклянная | 800 |
| Вата хлопчатобумажная | 1675 |
| Вата шлаковая | 750 |
| Вермикулит | 840 |
| Вермикулитобетон | 840 |
| Винипласт | 1000 |
| Войлок шерстяной | 1700 |
| Воск | 2930 |
| Газо- и пенобетон, газо- и пеносиликат, газо- и пенозолобетон | 840 |
| Гетинакс | 1400 |
| Гипс формованный сухой | 1050 |
| Гипсокартон | 950 |
| Глина | 750 |
| Глина огнеупорная | 800 |
| Глинозем | 700…840 |
| Гнейс (облицовка) | 880 |
| Гравий (наполнитель) | 850 |
| Гравий керамзитовый | 840 |
| Гравий шунгизитовый | 840 |
| Гранит (облицовка) | 880…920 |
| Графит | 708 |
| Грунт влажный (почва) | 2010 |
| Грунт лунный | 740 |
| Грунт песчаный | 900 |
| Грунт сухой | 850 |
| Гудрон | 1675 |
| Диабаз | 800…900 |
| Динас | 737 |
| Доломит | 600…1500 |
| Дуб | 2300 |
| Железобетон | 840 |
| Железобетон набивной | 840 |
| Зола древесная | 750 |
| Известняк (облицовка) | 850…920 |
| Изделия из вспученного перлита на битумном связующем | 1680 |
| Ил песчаный | 1000…2100 |
| Камень строительный | 920 |
| Капрон | 2300 |
| Карболит черный | 1900 |
| Картон гофрированный | 1150 |
| Картон облицовочный | 2300 |
| Картон плотный | 1200 |
| Картон строительный многослойный | 2390 |
| Каучук натуральный | 1400 |
| Кварц кристаллический | 836 |
| Кварцит | 700…1300 |
| Керамзит | 750 |
| Керамзитобетон и керамзитопенобетон | 840 |
| Кирпич динасовый | 905 |
| Кирпич карборундовый | 700 |
| Кирпич красный плотный | 840…880 |
| Кирпич магнезитовый | 1055 |
| Кирпич облицовочный | 880 |
| Кирпич огнеупорный полукислый | 885 |
| Кирпич силикатный | 750…840 |
| Кирпич строительный | 800 |
| Кирпич трепельный | 710 |
| Кирпич шамотный | 930 |
| Кладка «Поротон» | 900 |
| Кладка бутовая из камней средней плотности | 880 |
| Кладка газосиликатная | 880 |
| Кладка из глиняного обыкновенного кирпича | 880 |
| Кладка из керамического пустотного кирпича | 880 |
| Кладка из силикатного кирпича | 880 |
| Кладка из трепельного кирпича | 880 |
| Кладка из шлакового кирпича | 880 |
| Кокс порошкообразный | 1210 |
| Корунд | 711 |
| Краска масляная (эмаль) | 650…2000 |
| Кремний | 714 |
| Лава вулканическая | 840 |
| Латунь | 400 |
| Лед из тяжелой воды | 2220 |
| Лед при температуре 0°С | 2150 |
| Лед при температуре -100°С | 1170 |
| Лед при температуре -20°С | 1950 |
| Лед при температуре -60°С | 1700 |
| Линолеум | 1470 |
| Листы асбестоцементные плоские | 840 |
| Листы гипсовые обшивочные (сухая штукатурка) | 840 |
| Лузга подсолнечная | 1500 |
| Магнетит | 586 |
| Малахит | 740 |
| Маты и полосы из стекловолокна прошивные | 840 |
| Маты минераловатные прошивные и на синтетическом связующем | 840 |
| Мел | 800…880 |
| Миканит | 250 |
| Мипора | 1420 |
| Мрамор (облицовка) | 880 |
| Настил палубный | 1100 |
| Нафталин | 1300 |
| Нейлон | 1600 |
| Неопрен | 1700 |
| Пакля | 2300 |
| Парафин | 2890 |
| Паркет дубовый | 1100 |
| Паркет штучный | 880 |
| Паркет щитовой | 880 |
| Пемзобетон | 840 |
| Пенобетон | 840 |
| Пенопласт ПХВ-1 и ПВ-1 | 1260 |
| Пенополистирол | 1340 |
| Пенополистирол «Пеноплекс» | 1600 |
| Пенополиуретан | 1470 |
| Пеностекло или газостекло | 840 |
| Пергамин | 1680 |
| Перекрытие армокерамическое с бетонным заполнением без штукатурки | 850 |
| Перекрытие из железобетонных элементов со штукатуркой | 860 |
| Перекрытие монолитное плоское железобетонное | 840 |
| Перлитобетон | 840 |
| Перлитопласт-бетон | 1050 |
| Перлитофосфогелевые изделия | 1050 |
| Песок для строительных работ | 840 |
| Песок речной мелкий | 700…840 |
| Песок речной мелкий (влажный) | 2090 |
| Песок сахарный | 1260 |
| Песок сухой | 800 |
| Пихта | 2700 |
| Пластмасса полиэфирная | 1000…2300 |
| Плита пробковая | 1850 |
| Плиты алебастровые | 750 |
| Плиты древесно-волокнистые и древесно-стружечные (ДСП, ДВП) | 2300 |
| Плиты из гипса | 840 |
| Плиты из резольноформальдегидного пенопласта | 1680 |
| Плиты из стеклянного штапельного волокна на синтетическом связующем | 840 |
| Плиты камышитовые | 2300 |
| Плиты льнокостричные изоляционные | 2300 |
| Плиты минераловатные повышенной жесткости | 840 |
| Плиты минераловатные полужесткие на крахмальном связующем | 840 |
| Плиты торфяные теплоизоляционные | 2300 |
| Плиты фибролитовые и арболит на портландцементе | 2300 |
| Покрытие ковровое | 1100 |
| Пол гипсовый бесшовный | 800 |
| Поливинилхлорид (ПВХ) | 920…1200 |
| Поликарбонат (дифлон) | 1100…1120 |
| Полиметилметакрилат | 1200…1650 |
| Полипропилен | 1930 |
| Полистирол УПП1, ППС | 900 |
| Полистиролбетон | 1060 |
| Полихлорвинил | 1130…1200 |
| Полихлортрифторэтилен | 920 |
| Полиэтилен высокой плотности | 1900…2300 |
| Полиэтилен низкой плотности | 1700 |
| Портландцемент | 1130 |
| Пробка | 2050 |
| Пробка гранулированная | 1800 |
| Раствор гипсовый затирочный | 900 |
| Раствор гипсоперлитовый | 840 |
| Раствор гипсоперлитовый поризованный | 840 |
| Раствор известково-песчаный | 840 |
| Раствор известковый | 920 |
| Раствор сложный (песок, известь, цемент) | 840 |
| Раствор цементно-перлитовый | 840 |
| Раствор цементно-песчаный | 840 |
| Раствор цементно-шлаковый | 840 |
| Резина мягкая | 1380 |
| Резина пористая | 2050 |
| Резина твердая обыкновенная | 1350…1400 |
| Рубероид | 1500…1680 |
| Сера | 715 |
| Сланец | 700…1600 |
| Слюда | 880 |
| Смола эпоксидная | 800…1100 |
| Снег лежалый при 0°С | 2100 |
| Снег свежевыпавший | 2090 |
| Сосна и ель | 2300 |
| Сосна смолистая 15% влажности | 2700 |
| Стекло зеркальное (зеркало) | 780 |
| Стекло кварцевое | 890 |
| Стекло лабораторное | 840 |
| Стекло обыкновенное, оконное | 670 |
| Стекло флинт | 490 |
| Стекловата | 800 |
| Стекловолокно | 840 |
| Стеклопластик | 800 |
| Стружка деревянная прессованая | 1080 |
| Текстолит | 1470…1510 |
| Толь | 1680 |
| Торф | 1880 |
| Торфоплиты | 2100 |
| Туф (облицовка) | 750…880 |
| Туфобетон | 840 |
| Уголь древесный | 960 |
| Уголь каменный | 1310 |
| Фанера клееная | 2300…2500 |
| Фарфор | 750…1090 |
| Фибролит (серый) | 1670 |
| Циркон | 670 |
| Шамот | 825 |
| Шифер | 750 |
| Шлак гранулированный | 750 |
| Шлак котельный | 700…750 |
| Шлакобетон | 800 |
| Шлакопемзобетон (термозитобетон) | 840 |
| Шлакопемзопено- и шлакопемзогазобетон | 840 |
| Штукатурка гипсовая | 840 |
| Штукатурка из полистирольного раствора | 1200 |
| Штукатурка известковая | 950 |
| Штукатурка известковая с каменной пылью | 920 |
| Штукатурка перлитовая | 1130 |
| Штукатурка фасадная с полимерными добавками | 880 |
| Шунгизитобетон | 840 |
| Щебень и песок из перлита вспученного | 840 |
| Щебень из доменного шлака, шлаковой пемзы и аглопорита | 840 |
| Эбонит | 1430 |
| Эковата | 2300 |
| Этрол | 1500…1800 |
Таблица удельной теплоемкости пищевых продуктов
В таблице приведены значения средней удельной теплоемкости пищевых продуктов (овощей, фруктов, мяса, рыбы, хлеба, вина и т. д.) в диапазоне температуры 5…20°С и нормальном атмосферном давлении.
д.) в диапазоне температуры 5…20°С и нормальном атмосферном давлении.
| Продукты | C, Дж/(кг·К) |
|---|---|
| Абрикосы | 3770 |
| Ананасы | 3684 |
| Апельсины | 3730 |
| Арбуз | 3940 |
| Баклажаны | 3935 |
| Брюква | 3810 |
| Ветчина | 2140 |
| Вино крепленое | 3690 |
| Вино сухое | 3750 |
| Виноград | 3550 |
| Вишня | 3650 |
| Говядина и баранина жирная | 2930 |
| Говядина и баранина маложирная | 3520 |
| Горох | 3684 |
| Грибы свежие | 3894 |
| Груши | 3680 |
| Дрожжи прессованные | 1550…3516 |
| Дыни | 3850 |
| Ежевика | 3642 |
| Земляника | 3684 |
| Зерно пшеничное | 1465…1549 |
| Кабачки | 3900 |
| Капуста | 3940 |
| Картофель | 3430 |
| Клубника | 3810 |
| Колбасы | 1930…2810 |
| Крыжовник | 3890 |
| Лимоны | 3726 |
| Лук | 2638 |
| Макароны не приготовленные | 1662 |
| Малина | 3480 |
| Мандарины | 3770 |
| Маргарин сливочный | 2140…3182 |
| Масло анисовое | 1846 |
| Масло мятное | 2080 |
| Масло сливочное | 2890…3100 |
| Масло сливочное топленое | 2180 |
| Мед | 2300…2428 |
| Молоко сухое | 1715…2090 |
| Морковь | 3140 |
| Мороженое (при -10С) | 2175 |
| Мука | 1720 |
| Огурцы | 4060 |
| Пастила | 2090 |
| Патока | 2512…2700 |
| Перец сладкий | 3935 |
| Печенье | 2170 |
| Помидоры | 3980 |
| Пряники | 1800…1930 |
| Редис | 3970 |
| Рыба жирная | 2930 |
| Рыба нежирная | 3520 |
| Салат зеленый | 4061 |
| Сало топленое | 2510 |
| Сахар кусковой | 1340 |
| Сахарный песок | 720 |
| Свекла | 3340 |
| Свинина жирная | 260 |
| Свинина нежирная | 3010 |
| Слива | 3750 |
| Сметана | 3010 |
| Смородина черная | 3740 |
| Сода | 2256 |
| Соль поваренная (2% влажности) | 920 |
| Спаржа | 3935 |
| Сыр жирный | 2430 |
| Творог | 3180 |
| Телятина жирная | 3180 |
| Телятина нежирная | 3520 |
| Тесто заварное | 2910 |
| Тыква | 3977 |
| Хлеб (корка) | 1680 |
| Хлеб (мякиш) | 2800 |
| Черешня | 3770 |
| Чернослив | 3181 |
| Чеснок | 3140 |
| Шоколад | 2340…2970 |
| Шпинат | 3977 |
| Яблоки | 3760 |
| Яйцо куриное | 3180 |
Кроме таблиц удельной теплоемкости, вы также можете ознакомиться с подробнейшей таблицей плотности веществ и материалов, которая содержит данные по величине плотности более 500 веществ (металлов, пластика, резины, продуктов, стекла и др. ).
).
Источники:
- Исаченко В. П., Осипова В. А., Сукомел А. С. Теплопередача. Учебник для вузов, изд. 3-е, перераб. и доп. — М.: «Энергия», 1975.
- Тепловые свойства металлов и сплавов. Справочник. Лариков Л. Н., Юрченко Ю. Ф. — Киев: Наукова думка, 1985. — 439 с.
- Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др. Под ред. И. С. Григорьева — М.: Энергоатомиздат, 1991. — 1232 с.
- Еремкин А. И., Королева Т. И. Тепловой режим зданий: Учебное пособие. — М.: Издательство ACB, 2000 — 368 с.
- Кириллов П. Л., Богословская Г. П. Тепломассобмен в ядерных энергетических установках: Учебник для вузов.
- Михеев М. А., Михеева И. М. Основы теплопередачи. Изд. 2-е, стереотип. М.: «Энергия», 1977. — 344 с. с ил.
- Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
- Франчук А. У. Таблицы теплотехнических показателей строительных материалов, М.: НИИ строительной физики, 1969 — 142 с.

- Добрынин В. М., Вендельштейн Б. Ю., Кожевников Д. А. Петрофизика: Учеб. для вузов. 2-ое изд. перераб. и доп. под редакцией доктора физико-математических наук Д. А. Кожевникова — М.: ФГУП Издательство «Нефть и газ» РГУ нефти и газа им. И.М. Губкина, 2004. — 368 с., ил.
- В. Блази. Справочник проектировщика. Строительная физика. М.: Техносфера, 2005. — 536 с.
- Енохович А. С. Справочник по физике. М.: «Просвещение», 1978. — 415 с. с ил.
- Строительная теплотехника СНиП II-3-79. Минстрой России — Москва 1995.
- Мустафаев Р. А. Теплофизические свойства углеводородов при высоких параметрах состояния. М.: Энергоатомиздат, 1991. — 312 с.
- Новиченок Н. Л., Шульман З. П. Теплофизические свойства полимеров. Минск, «Наука и техника» 1971. — 120 с.
- Шелудяк Ю. Е., Кашпоров Л. Я. и др. Теплофизические свойства компонентов горючих систем. М., 1992. — 184 с.
Теплоемкость газов
При тепловых расчетах газопроводов
часто приходится пользоваться понятием
удельной теплоемкости газа. Удельной
теплоемкостью газа называется количество
теплоты, необходимой для нагрева единицы
массы вещества (или объема) на один
градус в определенном процессе:
Удельной
теплоемкостью газа называется количество
теплоты, необходимой для нагрева единицы
массы вещества (или объема) на один
градус в определенном процессе:
, (1.15)
где – количество теплоты, подведенной к единице массы (или объема) газа в процессе его нагрева от температуры до температуры ; и – соответственно начальная и конечная температура газа.
На практике наиболее часто используются теплоемкости изобарного и изохорного процессов. Эти теплоемкости называются изобарной и изохорной и обозначаются соответственно и . Теплоемкость – величина переменная, зависящая от температуры и давления, а для идеальных газов – только от температуры. Теплоемкость, определяемую уравнением (1.15), называют средней теплоемкостью и обозначают и в отличие от истинных теплоемкостей и , определяемых для конкретно заданной температуры.
Средняя теплоемкость газа в интервале
заданных температур процесса определяется
по значению среднеарифметической
температуры процесса
,
т. е. для того чтобы найти среднюю
теплоемкость
,
необходимо знать среднюю температуру
процесса
.
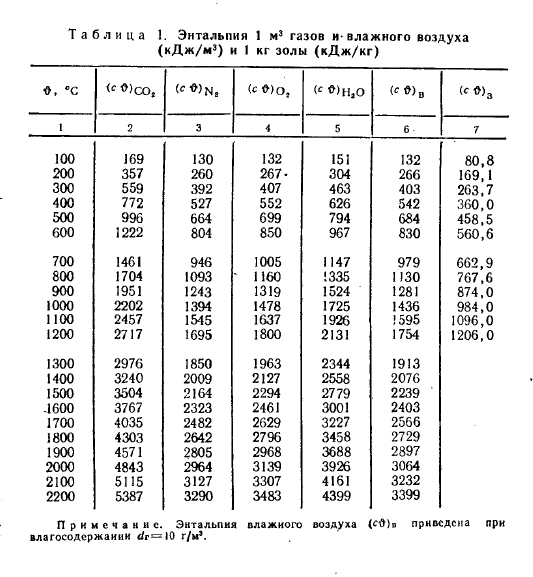
По найденному значению средней температуры
определяется с использованием специальных
таблиц (табл. 1.1) теплоемкость газов.
е. для того чтобы найти среднюю
теплоемкость
,
необходимо знать среднюю температуру
процесса
.
По найденному значению средней температуры
определяется с использованием специальных
таблиц (табл. 1.1) теплоемкость газов.
В практических расчетах среднюю теплоемкость наиболее просто определять по соотношению:
, (1.16)
где и – энтальпии природного газа в начале и в конце процесса. Значения энтальпий определяются по соответствующим таблицам или диаграммам для данного газа или вещества.
Таблица 1.1
#G0Температура °С | Кислород О | Азот N | Водород Н | Углекисл. газ СО | Вода НО | Метан СН | Воздух |
0 | 0,917 | 1,010 | 14,21 | 0,820 | 1,855 | 2,190 | 1,005 |
100 | 0,925 | 1,038 | 14,35 | 0,871 | 1,867 | 2,471 | 1,005 |
200 | 0,938 | 1,047 | 14,43 | 0,913 | 1,888 | 2,800 | 1,013 |
300 | 0,950 | 1,051 | 14,46 | 0,950 | 1,913 | 3,206 | 1,017 |
400 | 0,967 | 1,056 | 14,49 | 0,984 | 1,938 | 3,650 | 1,030 |
500 | 0,980 | 1,060 | 14,52 | 1,013 | 1,968 | 4,104 | 1,038 |
600 | 0,992 | 1,073 | 14,56 | 1,042 | 2,001 | 4,545 | 1,051 |
700 | 1,005 | 1,089 | 14,60 | 1,066 | 2,030 | 4,991 | 1,063 |
800 | 1,017 | 1,101 | 14,66 | 1,088 | 2,064 | – | 1,072 |
900 | 1,026 | 1,109 | 14,72 | 1,109 | 2,097 | – | 1,084 |
1000 | 1,034 | 1,118 | 14,79 | 1,126 | 2,131 | – | 1,093 |
1100 | 1,042 | 1,130 | 14,87 | 1,143 | 2,164 | – | 1,101 |
1200 | 1,051 | 1,139 | 14,95 | 1,160 | 2,194 | – | 1,109 |
1300 | 1,059 | 1,147 | 15,04 | 1,172 | 2,227 | – | 1,118 |
1400 | 1,063 | 1,155 | 15,13 | 1,185 | 2,257 | – | 1,126 |
1500 | 1,072 | 1,164 | 15,22 | 1,197 | 2,286 | – | 1,130 |
Свойства различных идеальных газов (при 300 К)
Свойства различных идеальных газов (при 300 К)
| Газ | Формула | Молярная масса | Газовая постоянная | Удельная теплоемкость при пост.  Нажимать. Нажимать. | Удельная теплоемкость при пост. Том. | Удельная теплоемкость Отношение |
| Воздух | 28,97 | 0,287 | 1.005 | 0,718 | 1,4 | |
| Аргон | 39,948 | 0,2081 | 0,5203 | 0,3122 | 1,667 | |
| Бутан | 58. | 0,1433 | 1.7164 | 1,5734 | 1.091 | |
| Двуокись углерода | 44.01 | 0,1889 | 0,846 | 0,657 | 1,289 | |
| Угарный газ | 28.011 | 0,2968 | 1,04 | 0,744 | 1,4 | |
| Этан | 30. | 0,2765 | 1.7662 | 1.4897 | 1,186 | |
| Этилен | 28.054 | 0,2964 | 1,5482 | 1.2518 | 1,237 | |
| Гелий | 4.003 | 2.0769 | 5.1926 | 3.1156 | 1,667 | |
| Водород | 2. | 4.124 | 14.307 | 10.183 | 1.405 | |
| Метан | 16.043 | 0,5182 | 2,2537 | 1.7354 | 1,299 | |
| Неон | 20.183 | 0,4119 | 1.0299 | 0,6179 | 1,667 | |
| Азот | 28. | 0,2968 | 1,039 | 0,743 | 1,4 | |
| Октан | 114.231 | 0,0729 | 1.7113 | 1.6385 | 1.044 | |
| Кислород | 31,999 | 0,2598 | 0,918 | 0,658 | 1,395 | |
| Пропан | 44. | 0,1885 | 1,6794 | 1.4909 | 1.126 | |
| Пар | 18.015 | 0,4615 | 1,8723 | 1.4108 | 1,327 |
Адаптировано из TEST ( T he E xpert S система для T Гермодинамика) < www.thermofluids.net > С. Бхаттачарджи, Государственный университет Сан-Диего
Газы с теплоемкостью – определение, расчет, единицы измерения, формула
Что такое теплоемкость?
Теплоемкость (Удельная) газов определяется как количество тепла, необходимое для повышения температуры одного грамма газов на единицу градуса, но на моль газа называется молярной теплоемкостью или просто теплоемкостью. Обычно для ее расчета в физике или химии используют уравнение теплоемкости, выраженное при постоянном давлении (C p ) и объеме (C v ) и единице энергии.
Обычно для ее расчета в физике или химии используют уравнение теплоемкости, выраженное при постоянном давлении (C p ) и объеме (C v ) и единице энергии.
Одноатомные молекулы благородных газов, такие как гелий, неон, аргон, при нагревании в постоянном объеме подводимое тепло будет использоваться для увеличения поступательной кинетической энергии, поскольку эти молекулы не имеют колебательного или вращательного момента. Эти одноатомные газы при постоянном объеме без энергии не могут быть использованы для совершения какой-либо механической работы. Но если нагревать при постоянном давлении, газ расширяется против поршня и совершает механическую работу. Для многоатомных газов подведенное тепло использует не только поступательную кинетическую энергию, но также колебательную или вращательную энергию.
Твердые тела также обладают теплоемкостью, измеренной на основании экспериментальных данных Дюлонга Пети о том, что атомная теплота всех кристаллических твердых элементов является постоянной величиной и приблизительно равна 6,4 калориям. Атомная теплота является произведением удельной теплоемкости и атомного веса элемента. Этот закон справедлив для многих элементов таблицы Менделеева, таких как серебро, золото, алюминий, свинец, железо и т. д.0535 кг -1 , потому что количество теплоты, необходимое для повышения температуры, зависит от массы веществ. Но молярная теплоемкость является интенсивным свойством в термодинамике и имеет единицу Дж К -1 моль -1 . Мы также используем единицы СГС и калории для определения теплоемкости твердых и газообразных веществ. Но если мы сохранили молярную и удельную теплоемкость, то на моль и на грамм или кг, используемые в этих единицах.
Атомная теплота является произведением удельной теплоемкости и атомного веса элемента. Этот закон справедлив для многих элементов таблицы Менделеева, таких как серебро, золото, алюминий, свинец, железо и т. д.0535 кг -1 , потому что количество теплоты, необходимое для повышения температуры, зависит от массы веществ. Но молярная теплоемкость является интенсивным свойством в термодинамике и имеет единицу Дж К -1 моль -1 . Мы также используем единицы СГС и калории для определения теплоемкости твердых и газообразных веществ. Но если мы сохранили молярную и удельную теплоемкость, то на моль и на грамм или кг, используемые в этих единицах.
Теплоемкость при постоянном давлении
Количество тепла или тепловой энергии, необходимое для повышения температуры одного грамма вещества на 1°К, называется удельной теплоемкостью, а для одного моля называется молярной теплоемкостью. Следовательно, C p = M × c p , где C p измеряется при постоянном давлении, а c p – их удельная теплоемкость. Из этой формулы температура одного гм-моля газа, повышенная на один градус при постоянном давлении, называется теплоемкостью при постоянном давлении или просто С р .
Из этой формулы температура одного гм-моля газа, повышенная на один градус при постоянном давлении, называется теплоемкостью при постоянном давлении или просто С р .
Теплоемкость при постоянном объеме
Опять же из определения, C v = M × c v , где C v измерено при постоянном объеме, c v – их удельная теплоемкость. Поэтому температуру одного гм-моля газа, повышенную на один градус при постоянном объеме, называют теплоемкостью при постоянном объеме или просто С v .
Теплоемкость в термодинамике
Следовательно, как и внутренняя энергия, энтальпия, энтропия и свободная энергия, теплоемкость также и термодинамические свойства. Пусть dq энергия, необходимая для повышения температуры dT одного моля газообразного вещества. Следовательно, термодинамическое определение удельной теплоемкости C = dq/dT, где dq = функция пути. Следовательно, значения изменения теплоты зависят от фактического процесса, который следует за этим измерением.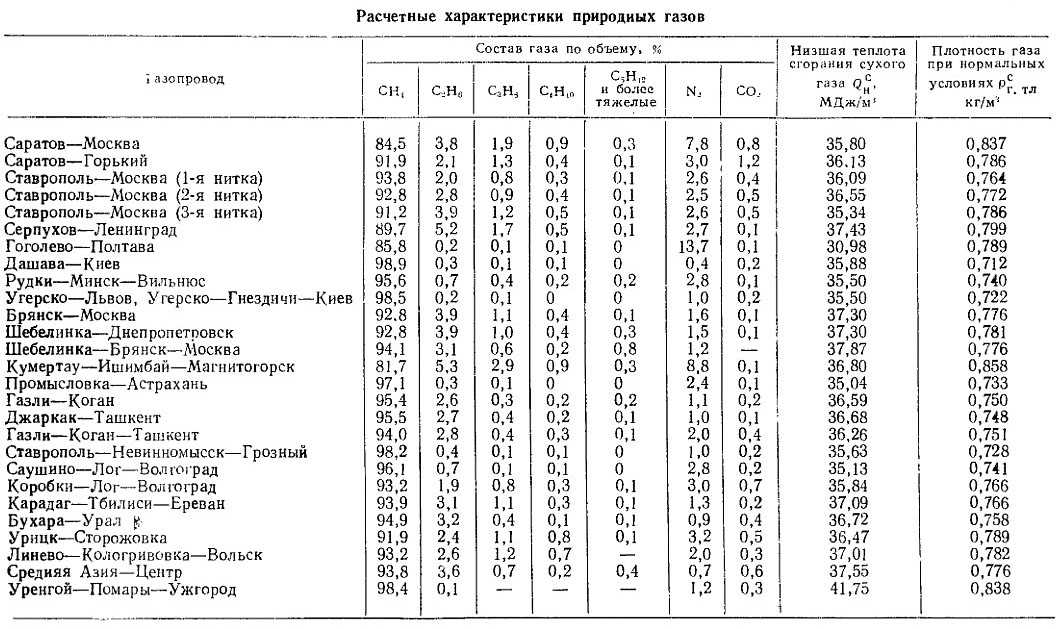 Но мы можем наложить некоторые ограничения, чтобы получить точные значения C p и C v . Обычные ограничения при постоянном давлении и при постоянном объеме.
Но мы можем наложить некоторые ограничения, чтобы получить точные значения C p и C v . Обычные ограничения при постоянном давлении и при постоянном объеме.
Значения Cp и Cv для газов
Расчет C p или C v зависит от давления и объема, особенно в случаях свойств газов. Следовательно, наблюдаемое количество в двух операциях будет разным. Следовательно, для измерения теплоемкости необходимо указать условия давления и объема. При изучении химии и физики С p , C v, и C p /C v или γ некоторых газов при давлении 1 атм и температуре 298 K приведены ниже в таблице,
Газы 9012| Сп | резюме | γ | |
| Аргон (Ar) | 4,97 | 2,98 | 1,66 |
| Гелий (He) | 4,97 | 2,98 | 1,66 |
| Ртуть (Hg) | 5,00 | 3,00 | 1,67 |
| Водород (H 2 ) | 6,85 | 4,86 | 1,40 |
| Азот (N 2 ) | 6,96 | 4,97 | 1,40 |
| Кислород (O 2 ) | 7. 03 03 | 5.03 | 1,40 |
| Углекислый газ (CO 2 ) | 8,83 | 6,80 | 1,30 |
| Диоксид серы (SO 2 ) | 9,65 | 7,50 | 1,29 |
| вода (H 2 O) | 8,67 | 6,47 | 1,34 |
| Метан (СН 4 ) | 8,50 | 6,50 | 1,31 |
Задача: Газы C p и C v имеют 0,125 и 0,075 кал гм -1 K -1 соответственно, как рассчитать молекулярную массу и формулу газа из уравнения удельной теплоемкости. Если можно, назовите газ.
Решение: M = 40 и ⋎ = 1,66 (моноатомный), Ar (аргон).
Формула механической работы
Одноатомный газ можно нагреть при постоянном давлении и постоянном объеме в цилиндре, снабженном поршнем. Когда газ расширяется против поршня, дает механическую энергию. Чтобы добиться повышения температуры на 1°, подведенного тепла должно быть достаточно для увеличения энергии молекул, а также для совершения дополнительной механической работы.
Чтобы добиться повышения температуры на 1°, подведенного тепла должно быть достаточно для увеличения энергии молекул, а также для совершения дополнительной механической работы.
Следовательно, C p равно некоторой механической энергии, необходимой для подъема поршня из объема V 1 в V 2 . C P – C V = механическая работа или энергия = PdV = P(V 2 – V 1 ) = PV 2 – PV 1 . Если газы подчиняются закону идеального газа, PV = RT. Следовательно, C p – C v = R(T + 1) – RT, или C p – C v = R = 2 калории.
Формула теплоемкости
Рассмотрим одноатомные газы, такие как аргон или гелий. Если такие газы нагревают при постоянном объеме, это используется для увеличения кинетической энергии поступательного движения. Так как одноатомные молекулы газа не могут ни поглощаться при колебательном, ни вращательном движении. Если теплота не используется для совершения механической работы расширения, когда объем газа остается постоянным. Следовательно, кинетическая энергия одномолярных идеальных газов при температуре T равна E = 3PV/2 = 3RT/2. Увеличение кинетической энергии при повышении температуры на 1° для одноатомного газа гелия или аргона, ΔE = 3{R(T+1) – RT}/2 = 3R/2 =3 калории.
Если теплота не используется для совершения механической работы расширения, когда объем газа остается постоянным. Следовательно, кинетическая энергия одномолярных идеальных газов при температуре T равна E = 3PV/2 = 3RT/2. Увеличение кинетической энергии при повышении температуры на 1° для одноатомного газа гелия или аргона, ΔE = 3{R(T+1) – RT}/2 = 3R/2 =3 калории.
Теплота, подведенная при постоянном объеме, равна увеличению кинетической энергии на единицу градуса повышения температуры. Следовательно, C v = ΔE = 3 калории. Для одного моля одноатомного газа отношение C p / C v , универсально выраженное символом γ, вычисляется по следующему уравнению: γ = C p / C v и C p – C v = R. Следовательно, γ = (C v + R)/C v
= (3 + 2)/3 = 1,66.
Cp и Cv для многоатомного газа
Для многоатомных молекул подведенное тепло расходуется не только на увеличение кинетической энергии, но также на увеличение колебательной или вращательной энергии. Пусть x калорий используется для увеличения вибрационных или вращательных целей.
Пусть x калорий используется для увеличения вибрационных или вращательных целей.
C p – C v = 2 калории остаются постоянными для этого уравнения энергии, но расчет C p /C v отличается от газа к газу.
Уравнение энергии и удельная теплоемкость
Теплота, подводимая к одному грамм-молю газа при постоянном объеме для повышения температуры на один градус, имеет C v для одноатомных или многоатомных газов. Но одноатомные газы используют эту энергию для увеличения поступательной кинетической энергии, а многоатомные газы используют ее для увеличения поступательной, колебательной и вращательной кинетической энергии.
Расчет теплоемкости
Экспериментальные и расчетные значения С р и С v ревела обусловлены следующими фактами. Из-за идеального расположения одноатомных газов C v /R = 1,5. Поэтому значения C p и C v не зависят от температуры в широком диапазоне.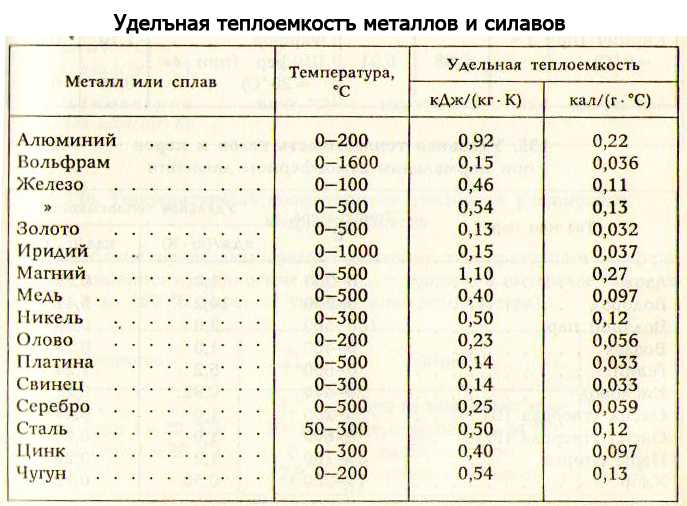
 124
124 07
07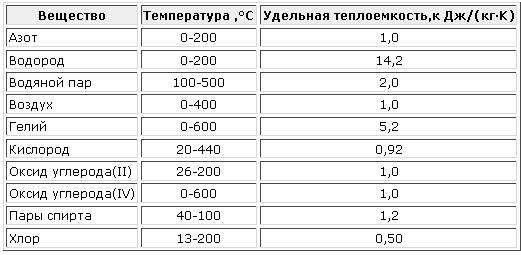 016
016 013
013 097
097