Гальваническая коррозия
МЕТАЛЛЫ В МОРСКОЙ СРЕДЕ
Крепеж
Когда речь заходит про крепеж, в дело вступают дополнительные факторы. Он должен, естественно, обладать прочностью и желательно при этом иметь разумную стоимость, поскольку количество его даже для самой миниатюрной лодки исчисляется сотнями. Но, пожалуй, самым важным для него является то, что, будучи установлен, он не должен ни корродировать сам, ни вызывать коррозию того, что он крепит – по крайней мере в течение достаточно длительного времени. В данном контексте имеются два вида коррозии, о которых следует помнить: гальваническая и химическая.
Гальваническая коррозия
Первый ее вид – гальваническая коррозия, которая возникает в тех случаях, когда два разных металла находятся в контакте друг с другом в присутствии электролита. Морская вода является (увы!) отличным электролитом и проникает на лодке повсюду. Гальваническая шкала ниже демонстрирует электрические потенциалы металлов, обычно применяемых в малом судостроении. Постараемся не слишком не углубляться в химические дебри, а заострим ваше внимание на трех основных моментах, чтобы понять ее практический смысл:
- Когда два металла находятся в контакте, находящийся левее будет корродировать.
- Разность потенциалов в 0.1 В является безопасной, 0.2 – приемлемой в зависимости от следующего условия.
- Темпы коррозии зависят помимо всего прочего от площадей поверхностей открытых металлов. Если крепеж менее инертен, чем деталь, он корродирует довольно скоро. Если же он из более благородного металла, срок его службы будет достаточен.
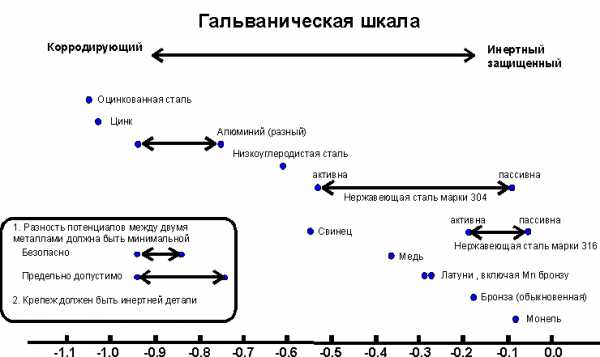
Каков практический смысл этой диаграммы?
- Из диаграммы понятно, почему элементы крепежа обычно делаются из материалов правой ее части. С алюминием у вас будут проблемы, поэтому позаботьтесь, чтобы вытяжные заклепки были из монеля (алюминиевые широко используются в автомобильной промышленности).
(Монель – сплав Ni с 23-27% Cu, 2-3% Fe, 1-2% Mn) - Вы сами можете решить, какой крепеж использовать для каких деталей (см. таблицу далее). Оцинкованного крепежа следует, естественно, избегать на нержавейке и алюминии. Менее явно то, что латунные винты представляют собой неудовлетворительный, а скорее даже опасный выбор для крепления бронзовых деталей.
- Существуют сплавы, сами по себе способные являться гальваническими парами. Самым ярким примером является латунь, у которой в присутствии электролита одна из “фаз” начинает корродировать. Явление именуется “децинкификация”. Латунный элемент, подверженный этому явлению, представляет собой неприятное зрелище и теряет свою прочность.
|
Крепеж |
||
|
Материал детали |
Допустимо |
Недопустимо |
|
Оцинкованная сталь |
Оцинкованный или нерж. |
Латунь и бронза |
|
Алюминий |
Нержавеющий |
Оцинкованный, латунь |
|
Латунь |
Латунь или бронза |
Нержавеющий |
| Бронза |
Бронза или нерж. |
Латунь |
|
Нерж. сталь |
Нерж. или монель |
Оцинк. или латунь |
Химическая коррозия
Второй вид коррозии, о котором не стоит забывать, является следствием воздействия различных химических веществ. Как правило, металлы защищают сами себя оксидной пленкой на поверхности и главное тут, является ли она самовосстанавливающейся, как в случае нержавеющей стали, алюминия и цветных металлов или же отваливается хлопьями, как у стали. Последствия этого могут быть разными – от чисто косметических в случае коррозии бронзового или оцинкованного палубного оборудования, до весьма серьезных – в случае коррозии гвоздей обшивки. Последнее в основном вызывается образованием в древесине кислот по мере ее пропитывания, дуб в этой ситуации является наихудшим вариантом. Всем хорошо известно, что может ожидать стальной крепеж, а стало быть килевые болты и гвозди. Гораздо чаще забывают, что нержавеющая сталь тоже уязвима.
Нержавеющая сталь
Поскольку существует огромное количество ложных представлений о нержавеющей стали (впрочем, само это название вводит в заблуждение), стоит провести небольшой ликбез по этой части. Помимо железа и углерода, нержавеющая сталь содержит ряд легирующих добавок. Из них самой важной является хром (Cr). Если сталь содержит его более 12%, вся поверхность покрывается пленкой из оксида хрома. Эта пленка “пассивна”, стойка к большинству воздействий и самовосстанавливается в присутствии кислорода. Нержавеющая сталь, содержащая один только хром, довольно хрупкая и поэтому в нее добавляют в два раза меньшее хрома количество никеля (Ni). 304-я нержавейка (она же A2), одна из самых распространенных, содержит 18% Cr и 10% Ni. Мойка или выхлопная труба скорее всего сделаны именно из 304-й и если вы пробовали чистить раковину мойки или релинг, то могли обратить внимание, что они в некоторой степени подвержены воздействию органических кислот, образующихся в пищевых продуктах, отпечатков пальцев и прочих загрязнений.
Химическая и пищевая промышленность снижают остроту этой проблемы путем добавления в сталь небольшого количества молибдена (Mo). Таким образом 316-я нержавейка (она же А4) обычно содержит 17% Cr, 11% Ni, 2 % Mo и широко используется для хранения и транспортировки агрессивных жидкостей. Из этого напрашивается вывод, что она представляет собой идеальный материал для крепежа древесины (или к ней) и с точки зрения воздействия одних только химических веществ вы скорее всего будете правы. Но надо еще принимать во внимание и ту среду, в которой предстоит работать крепежному элементу. Представим себе болт, гвоздь или шуруп, крепящий доску обшивки к шпангоуту ниже ватерлинии. Его шляпка, находящаяся на поверхности или вблизи нее будет иметь достаточный приток кислорода для поддержания оксидной пленки. Само же тело, находящееся внутри конструкции, скорее всего будет испытывать его недостаток, при этом находясь в окружении разных кислот и хлоридов. При подобных обстоятельствах пассивная пленка может разрушиться, сделав таким образом нержавейку “активной”. Последствий у этого может быть два. Во-первых, взгляните на гальваническую диаграмму, и вы увидите, что разность активных и пассивных потенциалов у 304-й нержавейки (у 316-й в меньшей степени) вполне достаточна, чтобы вызвать гальваническую коррозию. Подобно латуни, она способна сама собой образовывать гальваническую пару. Во-вторых, лишенная защитной пленки, нержавейка корродирует такими же темпами, как и самая обычная сталь. В результате этого нержавеющий крепеж ниже ватерлинии, независимо от его марки, может не иметь никаких преимуществ по сравнению с простой низкоуглеродистой сталью. Выше ватерлинии (где больше кислорода и меньше электролита) такой крепеж ведет себя превосходно.
В заключение хотелось бы еще указать на неразумность пескоструйной обработки оборудования из нержавеющей стали с целью придания ему вида оцинкованного. Способность пассивной пленки к самовосстановлению выше, если поверхность отполирована. При образовании на поверхности миллионов маленьких “пиков” вы значительно снижаете такую способность, в результате чего деталь покрывается ржавчиной. Если вам надо, чтобы деталь выглядела как оцинкованная, лучше такую и взять.
Сталь и оцинковка
Низкоуглеродистой стали без защитного покрытия нет места на борту лодки по причине ее склонности к коррозии, но при наличии покрытия — это вполне пригодный материал. Обычно этого достигают, нанося на нее слой цинка, получая при этом два плюса. Во-первых, цинк хорошо сопротивляется химической коррозии, а во-вторых, в присутствии электролита он корродирует прежде стали. Существует ряд способов нанесения слоя цинка, основная разница между ними заключается в толщине формируемого слоя. Чтобы получить приемлемый срок службы в морской среде, слой должен иметь толщину порядка 100 мкм. Этого можно достичь лужением (до 125 мкм при горячем погружении), окраской (около 40 мкм на слой), но только не электрогальваникой, где толщина обычно ограничивается 20 мкм. Поэтому тот блестящий оцинкованный крепеж, что продается в магазинах хозтоваров, годится для строительства теплицы, на лодке же жизнь его будет недолгой. “Морской” крепеж должен быть луженый.
Медь
Медные гвозди с шайбами широко применяется в классической деревянной конструкции. Для такого рода сравнительно гибких конструкций медные гвозди представляют идеальный материал: легко крепятся, коррозионно-устойчивы, достаточно эластичны, чтобы позволить подвижку элементов. С выходом на сцену клееных конструкций и тем более стеклопластиковых корпусов, довольно удивительно, что медные корабельные гвозди до сих пор имеются в продаже. Однако их выбор постепенно сужается. К примеру, 5-6 мм шайбы более не выпускаются, поэтому строителям каноэ приходится теперь расклепывать гвозди. Также исчезают и нестандартные размеры, полезные при ремонте обшивки, когда выбор гвоздей на размер выше поможет решить проблему течи.
Латунь
Латунь чаще всего выступает в роли шурупов. Помня о проблемах децинкификации, латунный крепеж следует использовать только в защищенных местах – во внутренней обстройке или в тех местах, где от него не зависит ваша жизнь.
Бронза
Стандартным материалом для крепежа является кремниевая бронза. Помимо использования ее в виде болтов и гвоздей, она является одним из немногих материалов, из которого делают гигантского размера шурупы (вплоть до №30). Она достаточно коррозионно-устойчива и служит очень долго – от тридцати до пятидесяти лет. Поэтому, несмотря на свою стоимость, бронзовый крепеж конкурентоспособен.
|
Виды медных сплавов и химический состав |
||||
|
Наименование |
Обозначение |
Состав |
Применение |
|
|
Латуни |
Обычная латунь |
CZ108 |
Zn 37% |
Внутреннее оборудование |
|
Морская латунь |
CZ112 |
Zn 37% Sn1% |
Оборудование довоенных лодок |
|
|
Высокопрочная латунь |
CZ114 |
Zn 37% Mn 2% Al 1.5% Fe 1% Pb 1.5% Sn 0.8% |
Такелажные скобы, гребные винты, лебедки |
|
|
Коррозионностойкая латунь |
CZ132 |
Zn 36% Pb 2.8% As 0.1% |
Водозапорная и трубная арматура |
|
|
Бронзы |
Алюминиевая бронза |
CA104 |
Al 10% Ni5% Fe5% |
Высокопрочное оборудование |
|
Фосфористая бронза |
PB102 |
Sn 5% P 0.2% |
Сборное и кованое оборудование |
|
|
Кремнистая бронза |
CS101 |
Si 3% Mn1% |
Крепеж |
|
|
Оружейная бронза |
LG2 |
Sn 5% Pb5% Zn5% |
Литье |
|
|
Алюминиевая бронза для литья |
AB2 |
Al 10% Ni5% Fe3% |
Леерное и мачтовое оборудование |
|
|
Al – алюминий, As – мышьяк, Fe – железо, Mn – марганец, Ni – никель |
||||
metalvis-yug.ru
Как правильно соединить провода алюминий и медь
Практически все уже знают, что алюминиевая проводка это наследие прошлого века, и ее обязательно нужно менять при ремонте квартиры. Мало кто проводит капремонт и забывает об этом.
Однако случаются ситуации, когда ремонт проводится частично, и возникает крайняя необходимость соединить алюминиевый провод с медным или просто их нарастить, добавив несколько лишних сантиметров жилы.
Электрохимическая коррозия
 При этом алюминий и медь не совместимы гальванически. Если вы их соедините напрямую, это будет что-то вроде мини батарейки.
При этом алюминий и медь не совместимы гальванически. Если вы их соедините напрямую, это будет что-то вроде мини батарейки.
При прохождении тока через такое соединение, даже при минимальной влажности, происходит электролизная химическая реакция. Проблемы обязательно рано или поздно себя проявят.
Окисление, ослабление контакта, его дальнейший нагрев с оплавлением изоляции. Переход в короткое замыкание, либо отгорание жилы.
К чему может в итоге привести такой контакт, смотрите на фото.
Как же сделать такое соединение грамотно и надежно, чтобы избежать проблем в будущем.
Вот несколько распространенных способов, которые применяют электрики. Правда не все они удобны для работы в монтажных коробках.
Рассмотрим подробнее каждый из них и выберем наиболее надежный, не требующий последующего обслуживания и ревизий.
Соединение через болт и стальные шайбы
 Здесь для соединения используется стальная шайба и болт. Это один из наиболее проверенных и простых методов. Правда получается очень габаритная конструкция.
Здесь для соединения используется стальная шайба и болт. Это один из наиболее проверенных и простых методов. Правда получается очень габаритная конструкция.
Для монтажа, закручиваете кончики проводов колечками. Далее подбираете шайбы.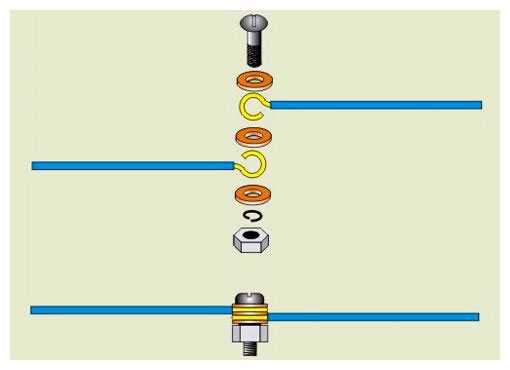
Они должны быть такого диаметра, чтобы все ушко провода спряталось за ними и не могло контактировать с другим проводником.
Самое главное, как расположить колечко. Его нужно одевать так, чтобы во время закручивания гайки, ушко не разворачивалось, а наоборот стягивалось во внутрь.
Стальные шайбы между проводниками из разных материалов препятствуют процессам окисления. При этом не забывайте про установку гравера или пружинной шайбы.
Без нее контакт со временем ослабнет.
Особо нужно отметить, что не рекомендуется использовать оцинкованные болты или шайбы.
Дело в том, что безопасно соединять между собой можно металлы, у которых электрохимический потенциал соединения не превышает 0,6мВ.
Вот таблица таких потенциалов.
Как видите у меди и цинка здесь целых 0,85мВ! Такое подключение даже хуже чем прямой контакт алюминиевых и медных жил (0,65мВ). А значит, соединение будет не надежным.
Однако, несмотря на простоту резьбовой сборки, в итоге получается большая, неудобная конструкция, формой похожая на улей.
И запихнуть все это дело в не глубокий подрозетник, не всегда есть возможность. Более того, даже в такой простой конструкции многие умудряются напортачить.
Последствия себя не заставят ждать через очень короткое время.
 Еще один способ — это применение соединительного сжима типа орех.
Еще один способ — это применение соединительного сжима типа орех.
Он часто используется для ответвления от питающего кабеля гораздо большего сечения, чем отпайка.
Причем здесь даже не требуется разрезание магистрального провода. Достаточно снять с него верхний слой изоляции. Некоторые нашли ему применение для подключения вводного кабеля к СИПу.
Однако делать этого не стоит. Почему, читайте в статье ниже.
Но опять же, для распаечных коробок орехи не подходят. Более того, и такие зажимы бывает, выгорают. Вот реальный отзыв от пользователя на одном из форумов:
 Есть серия специальных зажимов, которыми можно стыковать медь с алюминием.
Есть серия специальных зажимов, которыми можно стыковать медь с алюминием.
Внутри таких клемм находится противоокислительная паста.
Однако споры о 100% надежности таких зажимов, тем более для розеточных, а не осветительных групп, не утихают до сих пор. При определенной укладке в ограниченном пространстве, контакт может ослабнуть, что неминуемо приведет к выгоранию.
Причем произойти это может даже при нагрузке ниже минимальной на которую рассчитаны Ваго. Почему и когда это происходит?
Дело в том, что когда сжимаются соединяемые проводники, между прижимной пластиной и местом контакта появляется небольшой зазор. Отсюда и все проблемы с нагревом.

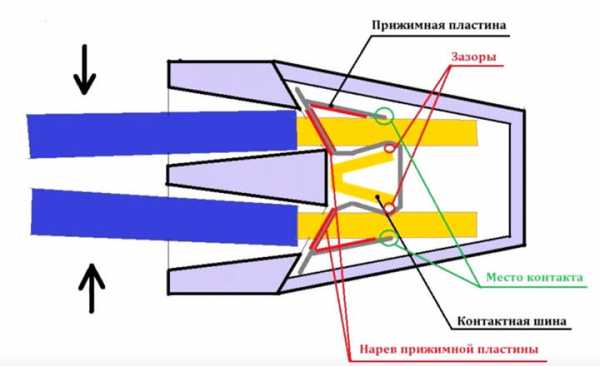
Вот очень наглядное видео, без лишних слов объясняющее данную проблему.
Клеммная колодка
 Данный способ имеет один существенный минус. Большинство продаваемых колодок очень низкого качества.
Данный способ имеет один существенный минус. Большинство продаваемых колодок очень низкого качества.
Некоторые исхитряются и чтобы избежать прямого контакта меди и алюминия, медную жилку припаивают сбоку такого зажима, а не вставляют во внутрь.
Правда клемму для этого придется разобрать. Кроме того, надежный контакт алюминия под винтом без ревизии, не живет очень долго.
Винтики каждые полгода-год нужно будет подтягивать. Частота ревизионных работ будет напрямую зависеть от нагрузки и ее колебаний в периоды максимума и минимума.
Забудете подтянуть и ждите беды. А если все это соединение запрятано глубоко в подрозетнике, то лезть туда каждый раз, не совсем удобное занятие.
Поэтому остается самый надежный из доступных способов – опрессовка. Здесь не будем рассматривать применение специализированных медно-алюминиевых гильз ГАМ, так как они начинаются от сечений 16мм2.
Для домашней же проводки, как правило наращивать нужно провода 1,5-2,5мм2 не более.
Соединение меди с алюминием опрессовкой
Рассмотрим наиболее распространенный случай, который встречается в панельных домах. Допустим, вам нужно запитать одну или несколько дополнительных розеток от уже существующего алюминиевого вывода в сквозной нише.
Для наращивания берете ГИБКИЙ медный провод сечением 2,5мм2. Это уменьшит механическое воздействие на алюминиевою жилу, когда вы будете укладывать провода в подрозетник.
Зачищаете концы медного провода. Далее, для такого соединения их нужно обязательно пропаять. Это исключит непосредственный контакт в гильзе меди и алюминия.
При этом перед пайкой флюсом снимите с жилы оксидный слой.
Сам процесс лужения заключается в окунании провода в специальное отверстие в паяльнике, заполненное оловом.
После остывания жилы остатки флюса удаляются растворителем.
Далее переходите к алюминиевым проводам, торчащим из стены. Аккуратно зачищаете их концы и также удаляете слой окиси.
Для этого можно воспользоваться оксидной токопроводящей пастой. Такая же паста используется при монтаже модульных штыревых систем заземления.
Она рассчитана на работу в любых условиях и исключает дальнейшее появление окиси на поверхности провода. Имейте в виду, что оксидная пленка может в последствии иметь сопротивление в несколько раз большее, чем сам алюминий.
И не удалив ее, вся ваша дальнейшая работа пойдет насмарку. Более того, температура плавления такой пленки достигает 2000 градусов (против примерно 600С у Al).

У некоторых возникнет логичный вопрос, а не продавится ли при опрессовке слой припоя на жиле? Тогда получается что все манипуляции по лужению будут напрасны.
Главное здесь правильно подобрать по сечению гильзу и матрицы инструмента для обжатия.
В этом случае мягкий припой как бы загерметизирует контактное пятно медноалюминиевого соединения. А без отсутствия доступа кислорода к этой точке, эрозии контакта наблюдаться не будет.
Будьте внимательны, при работе с алюминиевыми проводниками нужно действовать крайне осторожно, так как это очень ломкий материал. Одно неосторожное движение и облом жилы вам обеспечен.
После опрессовки необходимо заизолировать данное соединение клеевой термоусадкой.
Именно клеевой тип обеспечит 100% герметичность и предотвратит поступление кислорода к контактным местам. Чтобы не рисковать и не прожечь изоляцию, нагревать термоусадку лучше строительным феном, а не зажигалкой или портативной горелкой.
Полученный пучок проводов укладывать в подрозетник нужно с большой осторожностью, так как алюминий не любит резких перегибов.
Так как наращенные медные жили гибкие, то на концы этих проводников одеваете изолированные наконечники НШВИ.
Только после этого их можно смело заводить в клеммные колодки розеток и затягивать винты.
Безусловно, это не единственный способ наращивания алюминиевых проводов, но он является одним из самых простых (в отличии от сварки или пайки) и надежных (в отличии от скрутки). Подробнее
Подробнее
Если же у вас есть малейшая возможность сменить целиком алюминиевую проводку, делайте это обязательно, не экономьте на своей безопасности.
Статьи по теме
domikelectrica.ru
Что нужно знать о гальванических парах
Что нужно знать о гальванических парах
Совет.
При сборке антенны следует избегать контактирования разнородных металлов и гальванических покрытий, образующих недопустимые гальванические пары.
Наличие таких гальванических пар приводит к коррозии в месте стыка, особенно в условиях влажного климата. Допустимые и недопустимые контакты между металлами и покрытиями приведены в табл. 1.
Степень допустимости электрохимических контактных пар при эксплуатации на открытом воздухе Таблица 1
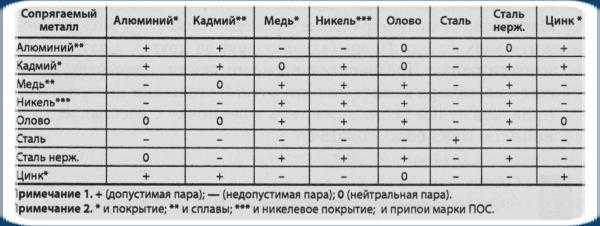
Например, к стальным трубкам вибраторов можно присоединять медную жилу коаксиального кабеля тремя способами:
♦ способ 1 – зажимом под стальную оцинкованную шайбу с таким же винтом и с обязательным предварительным лужением конца медной жилы;
♦ способ 2 – пайкой к стальному оцинкованному лепестку, с обязательным предварительным лужением конца жилы и части поверхности трубки;
♦ способ 3 – контактной сваркой.
Недопустимо приклепывать к медной трубке стальные лепестки, независимо от того, оцинкованы они или нет, а также прижимать необлуженную медную жилу кабеля к стальной трубке, так как в этих случаях образуются электрохимические пары медь-сталь или медь-цинк.
Паяные соединения, выполненные припоями марок ПОС-40, ПОС-6О и другими, содержащими олово и свинец, обладают невысокой механической прочностью, поэтому кабель рядом с местом пайки дополнительно нужно закрепить скобой и винтом.
Примечание.
Нельзя припаивать провода и элементы антенны кислотными припоями, надо использовать только бескислотные флюсы, канифоль и спирто-канифольные присадки.
Перед пайкой все детали антенн необходимо тщательно очистить от грязи и ржавчины, зачистить до металлического блеска, затем прочно соединить друг с другом, а после пайки закрасить масляной краской. Для защиты любых контактных пар можно использовать нитрокраски, шпаклевки и эпоксидную смолу, а также быстровысыхающие клеи.
Несовместимыми гальваническими парами в общем случае являются такие:
1 пара:
1) Алюминий и все сплавы на его основе.
2) Медь и ее сплавы, серебро, золото, платина, палладий, родий, олово, никель, хром.
2 пара:
1) Магниево-алюминиевые сплавы
2) Сталь легированная и нелегированная, хром, никель, медь, свинец, олово, золото, серебро, платина, палладий, родий.
3 пара:
1) Цинк и его сплавы.
2) Медь и ее сплавы, серебро, золото, платина, палладий, родий.
4 пара:
1) Сталь нелегированная, олово, свинец, кадмий.
2) Медь, серебро, золото, платина, палладий, родий.
www.smoldomrem.ru
Коррозия металлов Сплав Cu-Al (Ph20)
При контакте алюминия с медью возникает гальваническая пара Cu – Al. При электрохимической коррозии анодом в гальванической паре анодом становится металл, обладающего меньшим значением электродного потенциала, а катодом – металл с большим значением электродного потенциала. Поскольку в электрохимическом ряду напряжений медь стоит правее, чем алюминий, то медь имеет большее значение электродного потенциала восстановления, чем алюминий. Значит, в данной гальванической паре медь будет являться катодом, а алюминий – анодом. Е°(Al(3+)/Al) = − 1,70 В Е°(Cu(2+)/Cu) = + 0,338 В Е°(Cu(2+)/Cu) > Е°(Al(3+)/Al) При электрохимической коррозии на аноде происходит окисление (разрушение) металла. На катоде в атмосфере влажного воздуха в щелочной среде (рН = 10) происходит восстановление молекулярного кислорода – коррозия с кислородной деполяризацией. Анод(-) Al(0) – 3e → Al(3+) | 4 – окисление Катод(+) 2h3O + О2 + 4e → 4OH(-) | 3 – восстановление Суммируя реакции на аноде и катоде, получаем уравнение, которое в ионной форме, выражает происходящую в гальванической паре реакцию. 4Al(0) + 6h3O + 3О2 → 4Al(3+) + 12OH(-) Уравнение электрохимической коррозии в молекулярной форме. 4Al + 6h3O + 3О2 → 4Al(OH)3↓ Схема гальванической пары Анод (–) | Al | h3O + О2 | Cu | Катод (+) Электродный потенциал катода найдем по уравнению Нернста как потенциал кислородного электрода исходя из уравнения реакции, происходящей на катоде при условии, что p(O2) = 1 атм. Е(катода) = Eº(2h3О, O2/4ОН(-)) + (0,059/4)*lg(p(O2)/[OH]^4) = Eº(2h3О, O2/4ОН(-)) + 0,059*рОН = 0,401 + 0,059*4 = + 0,637 В рОН = 14 – рН = 14 – 10 = 4 Электродный потенциал анода равен стандартному электродному потенциалу алюминия. Е(анода) = Eº(Al(3+)/Al) = – 1,70 В ЭДС гальванической пары. ЭДСº = Е(катода) – Е(анода) = 0,637 – (– 1,70) = 1,063 B Коррозия сплава некоторое время будет протекать, однако образовавшийся на поверхности сплава в результате электрохимической коррозии нерастворимый гидроксид алюминия защитит сплав от дальнейшей коррозии.
touch.otvet.mail.ru
Гальваническая пара – это… Что такое Гальваническая пара?
Коррозия между двумя типами сталиПара не являющихся одинаковыми проводников (разные материалы), обычно металлов, в электрическом контакте.
Названа в честь Луиджи Гальвани. На явление, получившее название “опыт Гальвани”, он наткнулся случайно и не смог правильно объяснить, поскольку исходил из ложной гипотезы о существовании некоего животного электричества. Результаты исследований он изложил в “Трактате о силах электричества при мышечном движении”
Гальваническую пару также исследовал Жан-Жак Зульцер (по другим источникам шведский философ Иоган Георг Зульцер) [1], который писал:
“Если два куска металла, один оловянный, другой серебряный, соединить таким образом, чтобы оба края их были на одной плоскости, и если приложить их к языку, то в последнем будет ощущаться некоторый вкус, довольно похожий на вкус железного купороса, в то же время каждый кусок металла в отдельности не дает и следа этого вкуса…”
Опыты Зульцера повторил и расширил Алессандро Вольта
Гальваническая пара, погруженная в кислотный (щелочной) раствор, будет корродировать (разрушаться под действием коррозии). Этот процесс называется гальваническая коррозия. Как правило, соединения разных металлов всегда подвержены коррозии (если не электролитической, так атмосферной). Но некоторые пары металлов корродируют намного сильнее, ниже список металлов, которые не рекомендуется применять в паре.
Недопустимые гальванические пары:
1 пара:
1) Алюминий и все сплавы на его основе
2) Медь и её сплавы, серебро, золото, платина, палладий, родий, олово, никель, хром
2 пара:
1) Магниево-алюминиевые сплавы
2) Сталь легированная и нелегированная, хром, никель, медь, свинец, олово, золото, серебро, платина, палладий, родий
3 пара:
1) Цинк и его сплавы
2) Медь и её сплавы, серебро, золото, платина, палладий, родий
4 пара:
1) Сталь нелегированная, олово, свинец, кадмий
2) Медь, серебро, золото, платина, палладий, родий
5 пара:
1) Никель, хром
2) Серебро, золото, платина, палладий, родий
6 пара:
1) Титан и его сплавы
2) Алюминий и его сплавы
Необходимо избегать механического соединения деталей, изготовленных из металлов с заметно разными электрохимическими потенциалами. Например, недопустимо соединять латунные детали алюминиевой заклепкой. Для выбора материалов в этих случаях можно руководствоваться таблицей электрохимических потенциалов (так называемый электрохимический ряд).
Примечания
Ссылки
biograf.academic.ru
Гальваническая пара – это… Что такое Гальваническая пара?
Коррозия между двумя типами сталиПара не являющихся одинаковыми проводников (разные материалы), обычно металлов, в электрическом контакте.
Названа в честь Луиджи Гальвани. На явление, получившее название “опыт Гальвани”, он наткнулся случайно и не смог правильно объяснить, поскольку исходил из ложной гипотезы о существовании некоего животного электричества. Результаты исследований он изложил в “Трактате о силах электричества при мышечном движении”
Гальваническую пару также исследовал Жан-Жак Зульцер (по другим источникам шведский философ Иоган Георг Зульцер) [1], который писал:
“Если два куска металла, один оловянный, другой серебряный, соединить таким образом, чтобы оба края их были на одной плоскости, и если приложить их к языку, то в последнем будет ощущаться некоторый вкус, довольно похожий на вкус железного купороса, в то же время каждый кусок металла в отдельности не дает и следа этого вкуса…”
Опыты Зульцера повторил и расширил Алессандро Вольта
Гальваническая пара, погруженная в кислотный (щелочной) раствор, будет корродировать (разрушаться под действием коррозии). Этот процесс называется гальваническая коррозия. Как правило, соединения разных металлов всегда подвержены коррозии (если не электролитической, так атмосферной). Но некоторые пары металлов корродируют намного сильнее, ниже список металлов, которые не рекомендуется применять в паре.
Недопустимые гальванические пары:
1 пара:
1) Алюминий и все сплавы на его основе
2) Медь и её сплавы, серебро, золото, платина, палладий, родий, олово, никель, хром
2 пара:
1) Магниево-алюминиевые сплавы
2) Сталь легированная и нелегированная, хром, никель, медь, свинец, олово, золото, серебро, платина, палладий, родий
3 пара:
1) Цинк и его сплавы
2) Медь и её сплавы, серебро, золото, платина, палладий, родий
4 пара:
1) Сталь нелегированная, олово, свинец, кадмий
2) Медь, серебро, золото, платина, палладий, родий
5 пара:
1) Никель, хром
2) Серебро, золото, платина, палладий, родий
6 пара:
1) Титан и его сплавы
2) Алюминий и его сплавы
Необходимо избегать механического соединения деталей, изготовленных из металлов с заметно разными электрохимическими потенциалами. Например, недопустимо соединять латунные детали алюминиевой заклепкой. Для выбора материалов в этих случаях можно руководствоваться таблицей электрохимических потенциалов (так называемый электрохимический ряд).
Примечания
Ссылки
dal.academic.ru
Гальваническая пара – это… Что такое Гальваническая пара?
Коррозия между двумя типами сталиПара не являющихся одинаковыми проводников (разные материалы), обычно металлов, в электрическом контакте.
Названа в честь Луиджи Гальвани. На явление, получившее название “опыт Гальвани”, он наткнулся случайно и не смог правильно объяснить, поскольку исходил из ложной гипотезы о существовании некоего животного электричества. Результаты исследований он изложил в “Трактате о силах электричества при мышечном движении”
Гальваническую пару также исследовал Жан-Жак Зульцер (по другим источникам шведский философ Иоган Георг Зульцер) [1], который писал:
“Если два куска металла, один оловянный, другой серебряный, соединить таким образом, чтобы оба края их были на одной плоскости, и если приложить их к языку, то в последнем будет ощущаться некоторый вкус, довольно похожий на вкус железного купороса, в то же время каждый кусок металла в отдельности не дает и следа этого вкуса…”
Опыты Зульцера повторил и расширил Алессандро Вольта
Гальваническая пара, погруженная в кислотный (щелочной) раствор, будет корродировать (разрушаться под действием коррозии). Этот процесс называется гальваническая коррозия. Как правило, соединения разных металлов всегда подвержены коррозии (если не электролитической, так атмосферной). Но некоторые пары металлов корродируют намного сильнее, ниже список металлов, которые не рекомендуется применять в паре.
Недопустимые гальванические пары:
1 пара:
1) Алюминий и все сплавы на его основе
2) Медь и её сплавы, серебро, золото, платина, палладий, родий, олово, никель, хром
2 пара:
1) Магниево-алюминиевые сплавы
2) Сталь легированная и нелегированная, хром, никель, медь, свинец, олово, золото, серебро, платина, палладий, родий
3 пара:
1) Цинк и его сплавы
2) Медь и её сплавы, серебро, золото, платина, палладий, родий
4 пара:
1) Сталь нелегированная, олово, свинец, кадмий
2) Медь, серебро, золото, платина, палладий, родий
5 пара:
1) Никель, хром
2) Серебро, золото, платина, палладий, родий
6 пара:
1) Титан и его сплавы
2) Алюминий и его сплавы
Необходимо избегать механического соединения деталей, изготовленных из металлов с заметно разными электрохимическими потенциалами. Например, недопустимо соединять латунные детали алюминиевой заклепкой. Для выбора материалов в этих случаях можно руководствоваться таблицей электрохимических потенциалов (так называемый электрохимический ряд).
Примечания
Ссылки
dikc.academic.ru