температурный режим огня в зажигалке, влияющие факторы и классификация
 Пламя — это явление, которое вызвано свечением газообразной раскалённой среды. В некоторых случаях оно содержит твёрдые диспергированные вещества и (или) плазму, в которых происходят превращения реагентов физико-химического характера. Именно они и приводят к саморазогреву, тепловыделению и свечению. В газообразной среде пламени содержатся заряженные частицы — радикалы и ионы. Это объясняет существование электропроводности пламени и его взаимодействие с электромагнитными полями. На таком принципе построены приборы, которые могут приглушить огонь, изменить его форму или оторвать его от горючих материалов при помощи электромагнитного излучения.
Пламя — это явление, которое вызвано свечением газообразной раскалённой среды. В некоторых случаях оно содержит твёрдые диспергированные вещества и (или) плазму, в которых происходят превращения реагентов физико-химического характера. Именно они и приводят к саморазогреву, тепловыделению и свечению. В газообразной среде пламени содержатся заряженные частицы — радикалы и ионы. Это объясняет существование электропроводности пламени и его взаимодействие с электромагнитными полями. На таком принципе построены приборы, которые могут приглушить огонь, изменить его форму или оторвать его от горючих материалов при помощи электромагнитного излучения.
Виды пламени
Свечение огня делится на два вида:
- несветящиеся;
- светящиеся.
Свечение пламени обуславливается следующими факторами.
- Температурой.
- Плотностью и давлением газов, которые участвуют в реакции.
- Наличием твёрдого вещества.
Наиболее общая причина свечения — это присутствие в пламени твёрдого вещества.
Многие газы горят слабо светящимся или несветящимся пламенем. Из них наиболее распространены сероводород (пламя голубого цвета как при горении), аммиак (бледно-жёлтое), метан, окись углерода (пламя бледно-голубого цвета), водород. Пары летучих некоторых жидкостей горят едва светящимся пламенем (спирт и сероуглерод), а пламя ацетона и эфира становится немного коптящим из-за небольшого выделения углерода.
Температура пламени

Некоторое количество горючего вещества при сжигании выделяет определённое количество теплоты. Если строение вещества известно, то можно рассчитать объём и состав полученных продуктов горения. А если знать удельную теплоту этих веществ, то можно рассчитать ту максимальную температуру, которую достигнет пламя.
Стоит помнить о том, что если вещество горит в воздухе, то на каждый объём вступающего в реакцию кислорода приходится четыре объёма инертного азота. А так как в пламени присутствует азот, он нагревается теплотой, которая выделяется при реакции. Исходя из этого можно сделать вывод о том, что температура пламени будет состоять из температуры продуктов горения и азота.
Невозможно точно определить температуру, но можно это сделать приблизительно, так как удельная теплота изменяется с температурой.
Вот некоторые показатели по температуре открытого огня в разных материалах.
- Горение магния — 2200 градусов.
- Горение спирта не превышает температуры 900 градусов.
- Горение бензина — 1300−1400 градусов.
- Керосина — 800, а в среде чистого кислорода — 2000 градусов.
- Горение пропан-бутана может достигать температуры от 800 до 1970 градусов.
- При сгорании дерева температурный показатель колеблется от 800 до 1000 градусов, а воспламеняется оно при 300 градусах.
- Температурный параметр горения спички составляет 750−850 градусов.
- В горящей сигарете — от 700 до 800 градусов.
- Большинство твёрдых материалов воспламеняется при температурном показателе в 300 градусов.
Пламя свечи
 Пламя, которое каждый человек может наблюдать при горении свечи, спички или зажигалки, представляет из себя поток раскалённых газов, которые вытягиваются вертикально вверх, благодаря силе Архимеда. Фитиль свечи вначале нагревается и начинает испаряться парафин. Для самой нижней части характерно небольшое свечение синего цвета — там мало кислорода и много топлива. Именно из-за этого топливо не полностью сгорает и образуется оксид углерода, который при окислении на самом крае конуса пламени ему придаёт синий цвет.
Пламя, которое каждый человек может наблюдать при горении свечи, спички или зажигалки, представляет из себя поток раскалённых газов, которые вытягиваются вертикально вверх, благодаря силе Архимеда. Фитиль свечи вначале нагревается и начинает испаряться парафин. Для самой нижней части характерно небольшое свечение синего цвета — там мало кислорода и много топлива. Именно из-за этого топливо не полностью сгорает и образуется оксид углерода, который при окислении на самом крае конуса пламени ему придаёт синий цвет.
За счёт диффузии в центр поступает немного больше кислорода. Там происходит последующее окисление топлива и температурный показатель растёт. Но для полного сгорания топлива этого недостаточно. Внизу и в центре содержатся частицы угля и несгоревшие капельки. Они светятся из-за сильного нагревания. А вот испарившееся топливо, а также продукты сгорания, вода и углекислый газ практически не светятся. В самом верху наибольшая концентрация кислорода. Там не догоревшие частицы, которые в центре светились, догорают. Именно по этой причине эта зона практически не светится, хотя там наиболее высокий температурный показатель.
Классификация пламени
Классифицируют свечение огня следующим образом.
 По восприятию визуальному: цветные, прозрачные, коптящие.
По восприятию визуальному: цветные, прозрачные, коптящие.- По высоте: короткие и длинные.
- По скорости распространения: быстрые и медленные.
- По температурному показателю: высокотемпературные, низкотемпературные, холодные.
- По характеру перемещения среды реакционной: пульсирующие, турбулентные, ламинарные.
- По состоянию горючей среды: предварительно перемешанные и диффузионные.
- По излучению: бесцветные, окрашенные, светящиеся.
- По агрегатному состоянию горючих веществ: пламя аэродисперсных и твёрдых реагентов, жидких и газообразных.
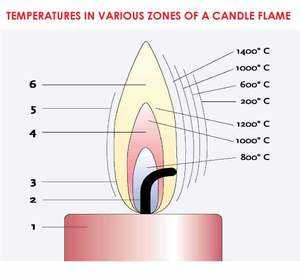
В диффузном ламинарном пламени выделяют три оболочки (зоны). Внутри конуса пламени существует:
- зона тёмная, где нет горения из-за малого количества окислителя — 300−350 градусов;
- зона светящаяся, где осуществляется термическое разложение горючего и оно сгорает частично — 500−800 градусов;
- зона слегка светящаяся, где окончательно сгорают продукты разложения горючего и достигается максимальный температурный показатель в 900−1500 градусов.
 Температурный параметр пламени зависит от интенсивности подвода окислителя и природы горючего вещества. Пламя распространяется по предварительно перемешанной среде. Происходит распространение по нормали от каждой точки фронта к поверхности пламени.
Температурный параметр пламени зависит от интенсивности подвода окислителя и природы горючего вещества. Пламя распространяется по предварительно перемешанной среде. Происходит распространение по нормали от каждой точки фронта к поверхности пламени.
По реально существующим смесям газовоздушным распространение всегда осложнено возмущающими внешними воздействиями, которые обусловлены трением, конвективными потоками, силами тяжести и прочими факторами.
Именно из-за этого реальная скорость распространения от нормальной всегда отличается. В зависимости от того, какой характер носит скорость распространения, различают такие диапазоны:
- При горении детонационном — более 1000 метров в секунду.
- При взрывном — 300−1000.
- При дефлаграционном — до 100.
Пламя окислительное
Оно располагается в самой верхней части огня, которая имеет наибольший температурный показатель. В этой зоне горючие вещества почти полностью превращены в продукты горения. Здесь наблюдается недостаток топлива и избыток кислорода. Именно по этой причине вещества, которые помещены в эту зону, окисляются интенсивно.
Пламя восстановительное
Эта часть наиболее близка к центру или находится чуть ниже его. Здесь мало кислорода для горения и много топлива. Если в эту область внести вещество, в котором имеется кислород, то он отнимется у вещества.
Температура огня в зажигалке
Зажигалка — это устройство портативное, которое предназначено для получения огня. Она может быть бензиново или газовой, в зависимости от применяемого топлива. Ещё существуют зажигалки, в которых собственного топлива нет. Они предназначаются для поджига газовой плиты. Качественная турбозажигалка — это прибор относительно сложный. Температура огня в ней может достигать 1300 градусов.
Химический состав и цвет пламени
У карманных зажигалок небольшой размер, это позволяет их переносить без каких-либо проблем. Довольно редко можно встретить настольную зажигалку. Ведь они из-за своих больших размеров для переноски не предназначены. Их дизайн разнообразен. Есть зажигалки каминные. Они имеют небольшую толщину и ширину, но довольно длинные.
На сегодняшний день становятся популярными рекламные зажигалки. Если в доме нет электроэнергии, то невозможно ей поджечь газовую плиту. Газ поджигает образующаяся электрическая дуга. Достоинствами этих зажигалок являются следующие качества.
- Долговечность и простота конструкции.
- Быстрое и надёжное зажигание газа.
 Первая зажигалка с современным кремнём создана в Австрии в 1903 году после изобретения ферроцериевого сплава бароном Карлом Ауэром фон Вельсбахом.
Первая зажигалка с современным кремнём создана в Австрии в 1903 году после изобретения ферроцериевого сплава бароном Карлом Ауэром фон Вельсбахом.
Ускорилось развитие зажигалок в период Первой мировой войны. Солдаты начали применять спички для того, чтобы видеть в темноте дорогу, но их местоположение выдавала интенсивная вспышка при поджиге. Необходимость в огне без значительной вспышки способствовало развитию зажигалок.
В то время лидерами производства зажигалок «кремнёвых» были Германия и Австрия. Такое портативное устройство, которое предназначено для получения огня, находящиеся в кармане многих курильщиков, при неправильном обращении может таить в себе немало опасностей.
Зажигалка в период работы не должна вокруг себя разбрызгивать искры. Огонь должен быть стабильным и ровным. Температура огня в зажигалках карманных достигает примерно 800−1000 градусов. Свечение красного или оранжевого цвета вызвано частицами углерода, которые раскалились. Для бытовых горелок и турбозажигалок применяется в основном газ бутан, который легко сжигается, не имеет запаха и цвета. Бутан получают путём переработки при высоких температурах нефти, а также её фракций. Бутан — это легковоспламенимые углеводороды, но он абсолютно безопасен в конструкциях современных зажигалок.
Подобные зажигалки в быту очень полезны. Ими можно поджечь любой воспламеняющийся материал. В комплект турбозажигалок входит настольная подставка. Цвет пламени зависит от горючего материала и температуры горения. Пламя костра или камина в основном имеет пёстрый вид. Температура горения дерева ниже температуры горения фитиля свечи. Именно из-за этого цвет костра не жёлтый, а оранжевый.
 Медь, натрий и кальций при высоких температурных показателях светятся различными цветами.
Медь, натрий и кальций при высоких температурных показателях светятся различными цветами.Электрическая зажигалка была изобретена в 1770 году. В ней водородная струя воспламенялась от искры машины электрофорной. Со временем бензиновые зажигалки уступили место газовым, которые более удобные. В них обязательно должна находиться батарейка — источник энергии.
Не очень давно появились зажигалки сенсорные, в которых без механического воздействия происходит зажигание газа воздействием на сенсорный датчик. Сенсорные зажигалки карманного типа. В основном, в них содержится информация рекламного типа, которая нанесена при помощи тампонной или шелкотрафаретной печати.
tokar.guru
Самый горячий цвет огня. Огненная жизнь: ярко и оригинально
Пламя бывает разного цвета. Посмотрите в камин. На поленьях пляшут желтые, оранжевые, красные, белые и синие языки пламени. Его цвет зависит от температуры горения и от горючего материала. Чтобы наглядно себе это представить, вообразите спираль электрической плитки. Если плитка выключена – витки спирали холодные и черные. Допустим, вы решили подогреть суп и включили плитку. Сначала спираль становится темно-красной. Чем выше поднимается температура, тем ярче красный цвет спирали. Когда плитка разогревается до максимальной температуры, спираль становится оранжево-красной.
Естественно, спираль не горит. Вы же не видите пламени. Она просто очень горячая. Если нагревать ее дальше, то будет меняться и цвет. Сначала цвет спирали станет желтым, затем белым, а когда она раскалится еще больше, от нее будет исходить голубое сияние.
Нечто подобное происходит и с пламенем. Возьмем для примера свечу. Различные участки пламени свечи имеют разную температуру. Огню нужен кислород. Если свечу накрыть стеклянной банкой, огонь погаснет. Центральный, прилегающий к фитилю участок пламени свечи, потребляет мало кислорода, и выглядит темным. Верхушке и боковым участкам пламени достается больше кислорода, поэтому эти участки ярче. По мере того как пламя продвигается по фитилю, воск тает и потрескивает, рассыпаясь на мельчайшие частички углерода. (Каменный уголь тоже состоит из углерода.) Эти частички увлекаются пламенем кверху и сгорают. Они очень горячие и светятся, как спираль вашей плитки. Но частички углерода намного горячее, чем спираль самой жаркой плитки (температура сгорания углерода примерно 1 400 градусов Цельсия). Поэтому свечение их имеет желтый цвет. Около горящего фитиля пламя еще горячее и светится синим цветом.
Пламя камина или костра в основном пестрого вида. Дерево горит при более низкой температуре, чем фитиль свечи, поэтому основной цвет костра – оранжевый, а не желтый. Некоторые частички углерода в пламени костра имеют довольно высокую температуру. Их немного, но они добавляют пламени желтоватый оттенок. Остывшие частички раскаленного углерода – это копоть, которая оседает на печных трубах. Температура горения дерева ниже температуры горения свечи. Кальций, натрий и медь, нагретые до высокой температуры, светятся разными цветами. Их добавляют в порох ракет для расцвечивания огней праздничных фейерверков.
Цвет пламени и химический состав
Цвет пламени может меняться в зависимости от химических примесей, содержащихся в поленьях или другом горючем веществе. В пламени может находиться, например, примесь натрия.
Еще в древние времена ученые и алхимики пытались понять, что за вещества сгорают в огне, в зависимости от того, в какой цвет окрашивался огонь.
- Натрий – это составная часть поваренной соли. Если натрий раскалить, он окрашивается в ярко — желтый цвет.
- В огонь может попасть кальций. Мы все знаем, что кальция много в молоке. Это металл. Раскаленный кальций окрашивается в яркий красный цвет.
- Если в огне горит фосфор, то пламя окрасится в зеленоватый цвет. Все эти элементы или содержатся в дереве, или попадают в огонь с другими веществами.
- Практически у всех дома есть газовые плиты или колонки, пламя в которых окрашено в голубой оттенок. Это обусловлено сгораемым углеродом, угарным газом, который и дает этот оттенок.

Смешение цветов пламени, как и смешение цветов радуги, может дать белый цвет, поэтому в пламени костра или камина видны белые участки.
Температура пламени при горении некоторых веществ:
Как получить ровный цвет пламени?
Для исследования минералов и определения их состава используется бунзеновская горелка , дающая ровный бесцветный цвет пламени, не мешающий ходу эксперимента, изобретенная Бунзеном в середине XIX века.
Бунзен был ярым поклонником огненной стихии, часто возился с пламенем. Его увлечением было стеклодувное дело. Выдувая из стекла различные хитрые конструкции и механизмы, Бунзен мог не замечать боли. Бывали, что его заскорузлые пальцы начинали дымиться от горячего еще мягкого стекла, но он не обращал на это внимания. Если боль уже выходила за грань порога чувствительности, то он спасался своим методом – сильно прижимал пальцами мочку уха, перебивая одну боль другой.
Именно он и был родоначальником метода определения состава вещества по цвету пламени. Конечно, и до него ученые пытались ставить такие эксперименты, но у них не было бунзеновской горелки с бесцветным пламенем, не мешающим эксперименту. Он вводил в пламя горелки различные элементы на платиновой проволоке, так как платина не влияет на цвет пламени и не окрашивает его.
Казалось бы, метод хороший, не нужен сложный химический анализ, поднес элемент к пламени – и сразу виден его состав. Но не тут то было. Очень редко вещества встречаются в природе в чистом виде, обычно они содержат большой набор различных примесей, изменяющих окраску.
Бунзен пробовал различные методы вычленения цветов и их оттенков. Например, пытался смотреть через цветные стекла. Скажем, синее стекло гасит желтый цвет, который дают наиболее распространенные соли натрия, и можно было различить малиновый или лиловый оттенок родного элемента. Но и с помощью этих ухищрений определить состав сложного минерала удавалось лишь раз из ста.
Это интересно! Благодаря свойству атомов и молекул испускать свет определенного цвета был разработан метод определения состава веществ, который называется спектральным анализом . Ученые исследуют спектр, который испускает вещество, например, при горении, сравнивают его со спектрами известных элементов, и, таким образом, определяют его состав.
На протяжении многих веков огонь играет очень важную роль в жизни человека. Без него практически невозможно представить наше существование. Он используется во всех сферах промышленности, а также для приготовления пищи, согревания дома и развития технического прогресса.
Впервые огонь появился в эпоху раннего палеолита. Изначально он применялся в борьбе против различных насекомых и нападений диких животных, а также давал свет и тепло. И только потом пламя огня применяли в кулинарии, изготовлении посуды и орудий труда. Так огонь вошел в нашу жизнь и стал «незаменимым помощником» человека.
Многие из нас замечали, что пламя может быть разным по своей цветовой гамме, но не многие знают, почему же огненная стихия обладает пестрой окраской. Как правило, цветовая гамма огня зависит от того, какое химическое вещество в нем сгорает. Благодаря воздействию высокой температуры все атомы химических веществ освобождаются, таким образом, придавая оттенок огню. Также было проведено большое количество экспериментов, о которых в этой статье будет написано чуть ниже, с целью того, чтобы понять, как
us-okna.ru
Газ горит оранжевым, красным или желтым цветом: правильный цвет горения газа
Газовое оборудование является небезопасным устройством. Поэтому необходимо знать признаки различных поломок для быстрого их устранения. Самой распространенной причиной в газовом оборудовании является изменение цвета горения газа. В норме он должен быть синим. Но если вы заметили, что цвет стал красным, оранжевым или желтым, а еще появился неприятный запах и падает черная сажа, то, скорее всего пламя коптит. При нарушении инжекции появляются на язычках пламени оранжевый или желтый цвет. Это говорит о нехватке воздуха.

В нашей статье подробно расскажем о горении газа и о признаках плохой работы газового оборудования.
Содержание:
- Газ горит желтым или оранжевым цветом
- Газ горит красным цветом
- Правильный цвет горения газа – синий
- Что делать в такой ситуации
Газ горит желтым или оранжевым цветом
Дисбаланс в топливовоздушной смеси возникает по различным причинам. Могут быть забиты отверстия для всасывания воздуха частичками пыли. Таким образом, создается препятствие для прохода воздуха. Больше всего газовое оборудование подвергается налету в первый год пользования. Так как после штамповки трубка запальной группы и горелка какое-то время сохраняют масляную пленку. Поэтому пыль налипает и мешает проходить воздуху, но газ пропускает отлично. Происходит большая подача газа в горелку. И нарушается баланс при смешивании подачи топлива к горелке.

Следовательно, газ попадает с пылью и сажей, поэтому возникает желтый и оранжевый цвет горения газа.
Еще главной ошибкой является покупка газового оборудования для другого вида газа. Ведь если вы применяете один газ, а ваше оборудование рассчитано на другой, то появляется желтый цвет горения газа.
Для того чтобы пропан и природный газ правильно сгорали необходимы разные пропорции воздуха. Поэтому перед покупкой газового оборудования нужно узнать, для какого типа газа оно предназначено.
В газовой плите заслонка для регулировки подачи воздуха может упасть, соскочить или может быть закрыта. Таким образом, не поступает необходимое количество воздуха. Если не хватает кислорода, то не все плиты могут гореть от электророзжига и иметь синий цвет пламени. Многие копят и теряют нагрев. В таком случае необходимо проводить ремонт газовой плиты.
Газ горит красным цветом
Угарный газ является побочным продуктом при сгорании абсолютно любого вида топлива. Газовое оборудование выделяет безопасный уровень газа, если при сгорании газа выделяется синий цвет пламени. Если пламя стало красным или оранжевым цветом, то это может говорить о повышенном выделении угарного газа. Если у вас появилась тошнота, головная боль, головокружение, то это могут быть признаки отравления угарным газом.
Угарный газ, как всем известно, не имеет цвета и запаха, поэтому надо контролировать цвет пламени. Если газовая колонка начала тухнуть и газ горит красным цветом, то необходимо провести чистку оборудования. Для этого лучше позвать специалиста.
Раньше, когда не было системы контроля газа, умирало много людей в результате отравления угарным газом. Поэтому при первых подозрениях на утечку угарного газа надо срочно вызвать соответствующих специалистов.
Правильный цвет горения газа – синий

Для того чтобы газ сгорал полностью и выделялось максимальное количество тепла нужно достаточное количества воздуха. Он смешивается с газом в горелке в необходимых пропорциях. Таким образом, будет обеспечиваться высокая интенсивность нагрева и выделения тепла. Если существуют какие-либо препятствия для поступления воздуха, то газ сгорает не полностью и выделяется окись углерода. А пламя становится желтым цветом.
От количества поступаемого воздуха зависит нагрев теплоносителя и цвет пламени. Если поступает нужное количество воздуха, то цвет пламени становится синим.
Если в топливовоздушной смеси больше содержится газа, чем воздуха, то пламя может стать желтым цветом. А через какое-то время и вовсе может стать красным или белым цветом. Связано это с повышенной подачей газа в основную горелку. В таком случае происходит неправильный расход топлива, и горелка начинает коптить. Если горелка коптит, то она не будет нагревать воду, котел будет плохо нагревать теплоноситель, на посуде будет оставляться черный след от газовой плиты, и таким образом еда будет насыщаться серой.
Что делать в такой ситуации
После того как цвет пламени стал оранжевым, красным или желтым следует понимать что это говорит об опасности. Поэтому необходимо найти проблему и устранить ее. После того как вы обнаружили изменение цвета горения пламени, то следует обратить к квалифицированному специалисту для диагностики и проведению ремонта газового устройства.
Возможно, необходимо будет провести чистку газового оборудования, замену форсунок горелки и отрегулировать воздушный затвор в котле. Отрегулировать топливовоздушную смесь можно самостоятельно. Для этого не требуется помощь мастера.
Главным требованием перед установкой газового оборудования является устройство датчиков обнаружения угарного газа.
Для квалифицированных специалистов не составит труда устранить копчение пламени. Для этого не требуется специальных инструментов. При малейших подозрениях на протечку угарного газа срочно обращайтесь к специалистам.
Читайте также:
baltgazservice.ru
От чего зависит цвет пламени
Несложно догадаться, что цвет пламени будет зависеть от того, какие химические вещества в нем сгорают, если под действием высокой температуры отдельные атомы этих веществ высвобождаются – давая окраску. Было проведено множество экспериментов, о которых я напишу чуть ниже, для того, чтобы понять, как вещества влияют на цвет огня.
Еще в древние времена ученые и алхимики пытались понять, что за вещества сгорают в огне, в зависимости от того, в какой цвет окрашивался огонь.
Практически у всех дома есть газовые плиты или колонки, пламя в которых окрашено в голубой оттенок. Это обусловлено сгораемым углеродом, угарным газом, который и дает этот оттенок. Соли натрия, которыми богата природная древесина, дают желто-оранжевое пламя, которым горит обычный лесной костер или бытовые спички. Посыпав конфорку газовой плиты обычной поверенной солью, вы получите тот же самый оттенок. Медь дает зеленый цвет пламени. Думаю, вы не раз замечали, что обычная, не обработанная защитным составом, медь окрашивает кожу в зеленый оттенок, если долго носить кольцо или цепочку. Так и во время процесса горения. При высоком содержании меди пламя имеет очень яркий зеленый цвет, практически идентичный белому. Вы можете это наблюдать, посыпав медной стружкой все ту же газовую конфорку.
Проводились опыты с обычной газовой горелкой и различными минералами для того, чтобы определить их состав. Минерал берется пинцетом и подносится в пламя – по оттенку, в который окрашивается огонь, можно судить о различных примесях, присутствующих в элементе. Зеленый и его оттенки дают такие минералы как барий, медь, молибден, фосфор, сурьма и бор, дающий сине-зеленый цвет. Также в синий окрашивает пламя селен. Красное пламя даст литий, стронций и кальций, фиолетовое – калий, желто-оранжевый оттенок выходит при сгорании натрий.
Для исследования минералов и определения их состава используется бунзеновская горелка, дающая ровный бесцветный цвет пламени, не мешающий ходу эксперимента, изобретенная Бунзеном в середине XIX века.
Бунзен был ярым поклонником огненной стихии, часто возился с пламенем. Его увлечением было стеклодувное дело. Выдувая из стекла различные хитрые конструкции и механизмы, Бунзен мог не замечать боли. Бывали, что его заскорузлые пальцы начинали дымиться от горячего еще мягкого стекла, но он не обращал на это внимания. Если боль уже выходила за грань порога чувствительности, то он спасался своим методом – сильно прижимал пальцами мочку уха, перебивая одну боль другой.

Именно он и был родоначальником метода определения состава вещества по цвету пламени. Конечно, и до него ученые пытались ставить такие эксперименты, но у них не было бунзеновской горелки с бесцветным пламенем, не мешающим эксперименту. Он вводил в пламя горелки различные элементы на платиновой проволоке, так как платина не влияет на цвет пламени и не окрашивает его.
Казалось бы, метод хороший, не нужен сложный химический анализ, поднес элемент к пламени – и сразу виден его состав. Но не тут то было. Очень редко вещества встречаются в природе в чистом виде, обычно они содержат большой набор различных примесей, изменяющих окраску.
Бунзен пробовал различные методы вычленения цветов и их оттенков. Например, пытался смотреть через цветные стекла. Скажем, синее стекло гасит желтый цвет, который дают наиболее распространенные соли натрия, и можно было различить малиновый или лиловый оттенок родного элемента. Но и с помощью этих ухищрений определить состав сложного минерала удавалось лишь раз из ста.
salamand.ru
Какая часть огня самая горячая. Завораживающее пламя свечи: в чем его сила
Костер – это контролируемое горение древесных материалов, например, хвороста, дров, поленьев, сложенных определенным образом. Хотя бывают костры, сделанные всего из одного полена (например, финская свеча) или в которых вовсе не задействована древесина, а используется другое твердое топливо (например, костры из сухой травы, кусков пластмассы или резины).
Костер на туристической стоянке — главный источник тепла, огня для приготовления пищи, света и романтического настроения.
Однако под понятие костра не попадает ни пожар, ни горящая свеча и вот почему.
Пожар – это неконтролируемое горение, поэтому быть костром он не может по определению.
Горение же свечи – это горение доведенного до газообразного состояния парафина или воска, из которого состоит свеча. То есть топливо в данном случае не твердое, а газообразное, а значит свеча не подходит под определение костра. Горение свечи скорее подобно горению горелки на жидком или газообразном топливе.
Кроме того, в свече отсутствует твердое топливо, являющееся непременным атрибутом костра.
Несколько интересных фактов об огне:
- Человек начал использовать огонь задолго до того, как научился его добывать. Источником огня могли служить, например, пожары в результате попадания в дерево молнии или возгорания в результате вулканических извержений. После этот огонь старались поддерживать, постоянно подбрасывая в него топливо.
- В некоторых салонах красоты стрижку клиентам делают с помощью огня. Считается, что огонь оздоравливает волосы, предотвращая их ломкость.
- Пламя способно заметно отклоняться в сторону под действием сильного магнита. Это связано с тем, что в пламени при высокой температуре образуются заряженные частицы, которые и реагируют на магнитные поля.
Компоненты, необходимые для разведения костра
Для того, чтобы началось и поддерживалось горение, необходимы три элемента – топливо, температура и кислород.
Топливо в этой троице служит материалом, который горит, либо который под воздействием высокой температуры разлагается, выделяя горючие вещества. Так, например, при нагревании при недостатке кислорода древесина выделяет пиролизные газы, которые затем загораются. На этом принципе построена работа пиролизных печей.
Для длительного поддержания огня обычно требуется заготовить достаточно большое количество дров.
Топливо не будет гореть, если не будет нагрето до температуры воспламенения. Эта температура у каждого материала своя. Для большинства же твердых материалов она колеблется около 300 °С.
Важно отметить, что при горении эти материалы значительно повышают температуру, что способствует переходу процесса горения в автоматический режим. Так, например, древесина загорается при температуре примерно 300 °С, а температура пламени горящей древесины колеблется в пределах 800–1000 °С.
Не будет гореть топливо и при отсутствии кислорода, поскольку процесс горения является процессом окисления горючего материала. А окисление без кислорода невозможно. Сам же кислород при горении, как правило, поступает из воздуха, в котором его содержание находится в пределах 21%.
Как видим, при отсутствии одного из этих элементов огонь либо не загорится, либо погаснет. Это важно понимать при разжигании костра и его тушении.
Кратко о характеристиках и свойствах: пламя, дым, температура горения
Пламя – форма распространения огня, возникающая в процессе горения топлива и представляющая собой раскаленную газообразную среду.
Считается, что частицы в пламени костра ионизированы и само пламя, по сути, представляет собой плазму.
Пламя в условиях Земли распространяется снизу вверх из-за того, что нагретый пламенем воздух расширяется и плотность его снижается. То есть, становясь более легким по сравнению с окружающими слоями, устремляется вверх, вытягивая за собой пламя.
Именно поэтому растопку поджигают снизу. Если растопку поджечь сверху, то огонь, не имея возможность нагреть нижележащие слои топлива, может погаснуть, а если не погаснет, то процесс разжигания будет медленным и «ленивым».
На этом же принципе основана работа долгогорящего костра «пирамида», о котором мы подробно рассказывали тут.
В условиях отсутствия гравитации, например, на космическом корабле, пламя имеет форму шара. Это происходит из-за того, что разогретый воздух не поднимается вверх, а распространяется равномерно во все стороны, так как на него не действует сила Архимеда. Тем не менее, в условиях невесомости пламя практически сразу гаснет, поскольку продукты горения не отводятся от него и к огню не поступает кислород.
Высота пламени зависит от интенсивности горения. Чем интенсивнее горит топливо, тем выше будут языки пламени, и тем больше тепла оно будет выделять. Например, устроен таким образом, что дрова в нем сгорают очень быстро, выделяя большое количество тепла и света, однако и прогорает такой костер тоже значительно быстрее по сравнению с другими видами костров.
На фото именно такой костер:
Говоря об интенсивности горения, следует отметить две его крайние формы – взрыв и тление. По сути, взрыв – это мгновенное, а тление – медленное сгорание топлива.
Как уже отмечалось ранее, температура пламени зависит от сгораемого материала, поскольку разные горючие вещества выделяют разное количество тепла при сгорании. Например, пламя горящего спирта будет иметь температуру 900 °С, бензина – более 1300 °С, а магния, используемого в виде стружки для разжигания огня от современного огнива, – 2200 °С.
Цвет свечения горящего топлива зависит от температуры горения. Чем выше температура, тем более смещается спектр свечения от красных оттенков к фиолетовым.
Примеси различных веществ в горючем (в том числе образующиеся в результате химической реакции и нагревания) могут менять цвет пламени. Так, например, натрий из поваренной соли, которую кинули в костер, окрашивает пламя в желтый цвет, медный купорос – в синий, а борная кислота – в бирюзовый.
Что касается горения дров, то желто-оранжевый цвет пламя приобретает из-за наличия в составе топлива солей натрия, а синий – из-за образования угарного газа при неполном сгорании дров.
Пламя также может быть бесцветным и невидимым. Это происходит при полном сгорании топлива с образованием водяных паров и углекислого газа, поскольку эффекта окрашивания пламени от этих веществ не наблюдается.
Если поместить способный гореть материал в верхнюю часть пламени, он будет сгорать быстрее, чем помещенный в центральную часть. Это связано с тем, что в верхней части пламени и температура выше, и кислорода больше, поскольку все, что должно было окислиться, уже окислилось и не расходует кислород. Однако этого не скажешь о средней части пламени, где присутствует избыток несгоревшего вещества при недостатке кислорода.
Думаю, с пламенем немного разобрались. Теперь поговорим о дыме.
Дым – мелкодисперсный аэрозоль, образующийся при сгорании топлива. Из-за небольших размеров частицы дыма не оседают, а остаются в толще воздушных масс.
Цвет дыма от костра бывает белым и черным, хотя с помощью различных пиротехнических смесей можно получить дым практически любого цвета. Белый дым может быть связан с большим количеством влаги, содержащейся в сгораемой древесине, а черный – с большим количеством сажи, образующейся при горении. Например, зеленая трава, брошенная в костер, дает густой белый дым, а зажженная автомобильная покрышка – черный.
Например, на фото ниже показан абсолютно натуральный дым от зеленой хвои:
При обеспечении достаточного количества кислорода, поступающего с воздухом, костер может гореть, образуя минимальное количество дыма. И наоборот, если костру не хватает воздуха, он может сильно дымить при слабом горении.
Функции костра и область его применения
Костер издавна используется человеком. Есть сведения, позволяющие утверждать, что даже древние люди применяли его для приготовления еды. На сегодняшний же день в мире не известно ни одного народа, включая самые изолированные и дикие племена, который не использовал бы огонь для приготовления пищи.
Бушмены в пустыне Калахари, Ботсвана.
В некоторых племенах на костре готовят даже бананы и смотрят с большим удивлением на тех, кто ест их в сыром виде.
Современный человек применяет костер для разных целей. Рассмотрим некоторые из них.
Обогрев. Пламя костра и тлеющие угли дают значительное количество тепла, способное согреть человека даже в условиях зимней тайги, где тем
www.kalinark.ru
Тайна пламени – CoolReal | Дневники.Ykt.Ru
Что такое огонь? Просто ответить на этот вопрос на самом деле, достаточно сложно)).
Майкл Фарадей еще в 1860 году попытался это сделать, прочитав ряд лекций для студентов и молодежи на тему «Химическая история свечи». Во вступлении он отмечал: «Явления, наблюдающиеся при горении свечи, таковы, что нет ни одного закона природы, который при этом не был бы так или иначе затронут».
Источники:
1. 100 великих открытий: О теории горения Антуана Лорана Лавуазье
2. Теория горения. Портал о пиротехнике.
2. Инна Купер “Вызов огня” //Троицкий вариант №109 от 31.07.2012, с.16
3. Зельдович Я.Б., Баренблатт Г.И., Либрович В.Б., Махвиладзе Г.М. Математическая теория горения и взрыва. М: Наука, 1975
4. Блинов Е.А. Топливо и теория горения. СПб: Изд-во СЗТУ, 2007
5. Выступления на семинарах ИФТПС СО РАН зав.кафедрой ДВС ТГУ (Хабаровск), д.т.н., проф. Лашко В.А.
Природа горения и пламени
История открытий горения, цвет и температура пламени, природа водорода и кислорода, и происходящих реакций окисления, сходство процессов дыхания с горением свечи… это очень интересно, но в наши интер- и итронетовские времена эти пространные шесть лекций мало кто осилит от начала до конца.

Но если можно было бы кратко прослушать содержание таких лекций, то, по существу, первую химическую теорию горения на рубеже 17 и 18 веков предложил немецкий химик Георг Эрнст Сталь (1659—1734). Процессы окисления и горения различных веществ он объяснил потерей некоего присущего им “начала горючести”, – ‘флогистона’. Восстановление же оксидов сопровождается возвращением флогистона обратно. Но уже в середине 18 века французский юрист и ученый Антуан Лавуазье развенчал концепцию флогистона и сформулировал кислородную теорию горения. Фактически, он методом количественного анализа в замкнутой системе показал увеличение веса остатка при сгорании серы и фосфора за счет воздуха, т.е. доказал, что часть воздуха при горении переходит в сгораемое вещество.
Дальнейшие его исследования были связаны с прокаливанием олова в реторте, – им выделены соотношения количества сгораемого в “землю” (окисел) металла и части воздуха. «Как видно, часть воздуха способна, соединяясь с металлами, образовывать земли, другая же — нет; это обстоятельство заставляет меня предполагать, что воздух — не простое вещество, как думали раньше, а состоит из весьма различных веществ».
В 1775 году Лавуазье представил академии рукопись, в которой был впервые точно выяснен состав воздуха. Оказалось, что воздух состоит из двух газов, «чистого воздуха», способного усиливать горение и дыхание, окислять металлы, и «мефитического воздуха», не обладающего этими свойствами. Названия кислород и азот были даны позднее.
В трактате «О горении вообще» (1777) он подробно развивает свою теорию. Всякое горение есть соединение тела с кислородом; результат его — сложное тело, а именно «металлическая земля» (окисел) или кислота (ангидрид по современной терминологии).
В дальнейшем уже знание водорода и продукта его окисления (воды) дало Лавуазье возможность положить главный камень в основание органической химии. Он определил состав органических тел и создал органический анализ путем сжигания углерода и водорода в определенном количестве кислорода. Как утверждает Н. Меншуткин: «Таким образом, историю органической химии, как и неорганической, приходится начинать с Лавуазье».

Сейчас практически каждый школьник знает, что существование жизни на земле обусловлено наличием реакции горения или в более общем смысле окисления. Основная химическая реакция, тепловая энергия которой является основой современных живых организмов, может быть выражена в первом приближении уравнением:
C + O 2 = CO 2 + 394,7 кДж (выделение тепла!)
Сам же процесс окисления с современной точки зрения можно выразить как потерю электронов окисляющимся веществом и, наоборот, – процесс восстановления, – как присоединение электронов восстанавливающимся веществом.
В связи с этим разделяют четыре основных типа горения. Первое, о котором уже говорилось – это горение твердых или жидких горючих тел за счет кислорода воздуха. Этот тип реакций горения объединяет важнейшие в практическом смысле реакции, например, горение нефти, каменного угля, дерева, бензола, толуола, спирта и т. д. Горение бензола, толуола или спирта может быть выражено основными уравнениями:
C6H6 + 7,5O2 + 28,2N2 = 6CO2 + 3h3O + 28,2N2
C6H5Ch4 + 9O2 + 34N2 = 7CO2 + 4h3O + 34N2
C2H5OH + 3O2 + 11,3N2 = 2CO2 + 3h3O + 11,3N2
Уравнение реакции горения составляется в этих случаях из тех соображений, что воздух состоит только из кислорода и азота, а инертные газы, находящиеся в воздухе, не учитываются, так как участия в горении не принимают. При этих условиях можно считать, что воздух состоит из 21% кислорода и 79% азота по объему, то есть на один объем кислорода в воздухе приходится 3,76 объема азота или на 1 моль кислорода приходится 3,76 моля азота.

Как видно из написанных уравнений горения, для его осуществления теоретически требуется значительное количество воздуха.
Например, на сгорание 1 кг бензола потребуется 10,25 куб.м. воздуха, толуола (динамит)- 9,8 куб.м., этанола 7,0 куб.м., антрацита (каменный уголь) – 9,0 куб.м., тяжелой нефти (мазут) – 10,8 куб.м., сухой древесины – 4,6 куб.м.
Можно заметить, что реакции горения первого типа являются «медленным горением». Но в обычных условиях скорость горения зависит, прежде всего, от величины частиц, а точнее, от величины поверхности горючего тела, и от скорости поступления воздуха к этой поверхности. В практике эти соотношения широко используются для отопления помещений, нагрева паровых котлов и т. л. Температура горения при этом процессе достигает всего 600-800 oС.

Но при усилении притока воздуха к месту горения или при подаче чистого кислорода, а также измельчении горючего и предварительном его смешивании с воздухом в мелкодисперсном состоянии, температура и скорость горения резко возрастает, что используются в кузнечном деле, доменном процессе, различного рода двигателях и турбинах, и т.д.

Но общем случае горение может происходить и без кислорода, например, водорода в атмосфере хлора, что также сопровождается выделением тепла и света. Горение некоторых видов пиротехнических составов происходит также без кислорода, и даже в воде (например, термита).
2Al + Fe 2O 3 = Al 2O 3 + 2Fe + 772 кДж
Это уже 2-й тип реакций – быстрое горение – или горение механических смесей горючих тел с окислителями. В качестве окислителей в практике находят применение преимущественно селитры – соли азотной кислоты, а также хлораты и перхлораты и в некоторых случаях окислы металлов, например железа. К этому типу реакций горения относится горение различного рода пиротехнических составов, зажигательных составов и дымных порохов.
Горение пиротехнического состава зеленого огня происходит по уравнению:
8Ba(NO3)2 + 6Mg + C2Cl6 + C13h22O2 => 7BaO + BaCl2 + 4MgO +
2MgCl2 + 15CO2 + 6h3O + 8N2 + 1,5O2
Также можно сжигать алюмиевую пыль. Горит она очень красиво, как бенгальский огонь
4Al + 3O2 = 2Al2O3,
Вспоминая свое бесшабашное детство, снова можно вспомнить фабрику “Сардаана” на ул.Шавкунова, где мы формировали такие “взрывпакеты” прямо в неработающих цехах. Там на полу почему-то было очень много такой пыли. Новый год нам был обеспечен в любое время года!

Скорость горения смесей даже в виде прессованных шашек при атмосферном давлении не превышает 1-2 см/сек. Повышение скорости горения смесей горючих тел с окислителем по сравнению с горением горючих тел на воздухе влечет за собой резкое повышение температуры горения. Так, например, температура горения термита и пиротехнических составов оценивается величиной 2500 – 3000°С, что имеет существенное значение в практике применения этих смесей.
Горение порохов в незамкнутом объеме также относится ко 2-му типу реакции горения. В замкнутом объеме, каким является, например, зарядная камера орудия, горение пороха протекает со значительной скоростью и сопровождается резким звуком.
Это явление носит наименование «выстрел». Характер действия горения пороха на окружающую среду проявляется в этом случае в более пли менее быстром нарастании давления газов и совершения ими работы перемещения или метания предметов в сторону наименьшего сопротивления.
А вот такой тип реакции горения уже называется взрывом. Этот, третий тип реакций горения протекает с переменной скоростью, достигающей сотен метров в секунду. Характер действия на окружающую среду проявляется в этом случае в форме резкого подъема давления и совершения работы в форме более или менее значительного разрушения среды.
Так, например, дымный порох при надлежащем способе инициирования может разлагаться со скоростью 400 м/сек. Нитроглицериновый порох, сильно охлажденный, например, в зимнее время, горит со скоростью, превышающей скорость горения его в нормальных условиях, что обусловливает раздутие стволов минометов. Наконец, такие ВВ как тротил иногда детонируют неполностью; в этом случае имеет место недостаточное развитие детонационного процесса и переход его последовательно во взрыв, горение и полное прекращение процесса.
4-й тип реакций горения – это детонация. Скорость её достигает тысяч метров в секунду, и характер действия на окружающую cpeду в виде быстрого нарастания давления в месте взрыва выражается в дроблении окружающих предметов. На этом основании вещества, способные к такого рода превращениям, называются бризантными ВВ (от французского слова briser – разрушать, дробить).
Вызов огня
В США проблемой необходимости упрощенного объяснения горения озадачился некто Алан Алда (Alan Alda) — американский актер и популяризатор науки. Вместе с Центром популяризации науки \(Center for Communicating Science) в Университете шт. Нью-Йорк в Стоуни Брук объявил этой весной конкурс под названием «Вызов огня» (The Flame Challenge).
Размышления о том, как объяснять научные понятия публике разного возраста, привели Алана Алду к созданию серии фильмов и передач про науку, к организации интервью с различными учеными, к созданию Центра популяризации науки, упомянутого выше. И весной 2012 года, — к организации конкурса «Вызов огня».
Алан Алда еще школьником очень интересовался окружающим миром и решил спросить свою учительницу, а что же такое огонь? «Это процесс окисления», — ответила учительница. И всё. Правильный по сути ответ показался школьнику недостаточным. Этот ответ, по его словам, не объяснял, почему огонь желто-красный или горячий, что вообще происходит при горении и т.д. [4].

Алан считает, что школьникам необходима простота и ясность изложения [4]. Именно поэтому условия конкурса «Вызов огня» предельно просты. Нужно дать объяснение того, что такое огонь, чтобы оно было понятно 11-летнему школьнику. Конкурс был открыт для участия людей со всего мира. Было подано 822 заявки из 31 страны. Судьями были школьники. Школы со всего мира могли подать коллективную заявку на участие своих школьников в судействе. Для них была разработана простая форма, в которой содержались такие вопросы, как «Понятно ли объяснение?», «Интересно ли оно?» и пр. Всего в судействе принимала участие 131 школа из разных стран.
После первичной обработки заполненных форм был определен круг финалистов, а 9 мая была собрана «Всемирная ассамблея» — живая видеоконференция с Аланом Алдой в качестве ведущего и с участием школ-судей. Десять школ участвовали в видеообсуждении, остальные могли комментировать и голосовать. Как отмечено в блоге одной из школ английского языка в Бельгии, «Всемирная ассамблея — хорошая возможность для школьников с различными судьбами и возможностями собраться вместе для дискуссий и проведения праздника науки» [5].
В атмосфере всеобщей радости и возбуждения был выбран победитель. Церемония объявления победителя прошла 2 июня 2012 года на Всемирном фестивале науки в Нью-Йорке, в США. Победителем стал Бен Эймс (Ben Ames) из Канзас-Сити, штат Миссури. Бену -31 год, он аспирант Инсбрукского университета в Австрии, работает над проблемами квантовой оптики.
Бен, – молодой, “свой” парень, не только знающий физику, но также рисующий, поющий и пишущий музыку, увлекающийся театром. На вопрос Алды: «Как же вам удалось сделать этот ролик, вы же физик, работаете и учитесь?», — Бен ответил просто: «Ну, я сказал на работе, что мне надо взять пару недель отгулов, жене и дочке сказал, что меня не будет какое-то время, заперся у себя в подвале и … сделал ролик» [6].
 Видеоролик Бена Эймса начинается с показа седого старичка, прикованного к скале [7]. Старичок давно горит в адском огне. Голос ученого за кадром обращается к старичку: Какая же это должна быть пытка, быть всё время в огне и не понимать его… Вам не хочется узнать, что же это такое?
Видеоролик Бена Эймса начинается с показа седого старичка, прикованного к скале [7]. Старичок давно горит в адском огне. Голос ученого за кадром обращается к старичку: Какая же это должна быть пытка, быть всё время в огне и не понимать его… Вам не хочется узнать, что же это такое?
Видите вот эту свечку на пирожном? Почему у ее пламени разные цвета? Почему оно такое горячее? И дальше начинается анимированное объяснение. Свеча и пламя состоят из трех типов атомов — углерода, водорода и кислорода. Углерод и водород сцеплены вместе в твердых частях свечи — парафине и фитиле. Кислород — в воздухе вокруг нас. При нагревании кислород «сходит с ума» и начинает «трясти» углерод и водород до тех пор, пока те не «расцепятся» и не начнут уходить из свечки в виде газа и смешиваться с кислородом. Это называется пиролиз.
 Дальше в видео атомы боксируют на ринге, появляются синее пламя и еще один научный термин — хемилюминесценция. Пламя горячее, потому что разные атомы объединяются» и «трясутся как сумасшедшие». И всё это называется окислением — объединение атомов кислорода с другими атомами и появление новых «штук». Желтое пламя, сажа, белое каление — всё это тоже объяснено. Заканчивается ролик лиричной рок-песней с припевом «пиролиз, хемилюминесценция, окисление, белое каление». Чертик раскаляет свой трезубец в огне, а старичок со следами съеденного пирожного на губах довольно улыбается
Дальше в видео атомы боксируют на ринге, появляются синее пламя и еще один научный термин — хемилюминесценция. Пламя горячее, потому что разные атомы объединяются» и «трясутся как сумасшедшие». И всё это называется окислением — объединение атомов кислорода с другими атомами и появление новых «штук». Желтое пламя, сажа, белое каление — всё это тоже объяснено. Заканчивается ролик лиричной рок-песней с припевом «пиролиз, хемилюминесценция, окисление, белое каление». Чертик раскаляет свой трезубец в огне, а старичок со следами съеденного пирожного на губах довольно улыбается
Объяснение другого финалиста, Натана Андерсона (Nathan Anderson), хотя и длинноватое (около 500 слов), но также заслуживает внимание (здесь с сокращениями):
Чтобы получился огонь, нужны три вещи. Топливо (то, что горит), воздух (точнее, кислород в воздухе) и тепло (спички, зажигалка или две сухие палочки, если вам очень повезет). Когда мы зажигаем свечку, огонь спички плавит воск вокруг фитиля. Жидкий воск пропитывает фитиль, закипает и превращается в газ. Этот газ выходит из фитиля как пар. Таким образом воск, превратившийся в газ, кислород в воздухе и тепло от спички создают новое пламя. Цвет испаряющегося воска связан с температурой. Голубоватый — это просто горячий газ. Чем больше он нагревается, тем больше он светится и переходит в красные, а затем желтобелые цвета. А сажа и дым — это то, что не догорело и просто уходит в воздух [8].
Не так образно, может даже с меньшим количеством научной информации, но как-то проще, доступнее и концептуальнее.
Возникает желание еще почитать про огонь? Может, именно в этом, а не в самом лучшем объяснении, главное достижение конкурса. Простой вопрос, интересно организованное событие и множество разных ответов порождает интерес к научному явлению. Школьники узнали об огне и физических явлениях, и, как отметил Алан, школьники признали, что понимание рождалось в результате просмотра и сравнения множества заявок, а не какой-то одной. А ведь это как раз и составляет процесс обучения. Изучить, сопоставить и сравнить, сформировать собственное представление.
Можно ли объяснить научные понятия просто и доходчиво?
Несомненно. Можно и нужно. В Америке проблему доходчивого объяснения часто представляют как умение объяснить то, чем ты занимаешься, своей бабушке (а у нас обычно к ней посылают во всех других случаях). Конкурс «Вызов огня» показал еще раз, что бабушкам или школьникам можно объяснить многое, было бы желание. И будет весело, с выражением, в виде мультика. Можно ли освоить таким образом целые научные предметы, такие, как физика, химия или биология?
К сожалению, нет! На одних играх учебу не построишь, – нужно много и упорно трудиться… Поэтому задача популяризации больше в том, чтобы зажечь интерес, показать, что освоение науки приносит удивительные плоды.
Конкурс «Вызов огня» завершился. Но уже объявлен конкурс на лучший вопрос для популярного объяснения на 2013 год. Дети могут присылать свои вопросы (с разрешения родителей и на английском языке) через форму по ссылке
www.centerforcommunicatingscience.org/?page_id=1385.
Ссылки Инны Купер, канд. социол. наук, Ph.D. Университета штата Индиана:
1. Faradey, M. The Chemical History of a Candle. www.bartleby.com/30/7.html
2. Фарадей М. Лекция I. Свеча. Пламя. Его питание. Его строение. Подвижность. Яркость. http://vivovoco.rsl.ru/VV/Q_PROJECT/FAR/FARADAY1.HTM
3. A Challenge to Make Science Crystal Clear, New York Times, March 5 2012, www.nytimes.com/2012/03/06/science/alan-aldas-challenge-to-make-science-easier-to-understand.html
4. Alda, A. (2012). The Flame Challenge: Editorial. www.centerforcommunicatingscience.org/wp-content/uploads/2012/03/Flame-Challenge1019.full_.pdf
5. St. John’s blog — The flame challenge. http://blog.stjohns.be/2012/05/08/the-flame-challenge/
6. Cool Jobs and The Flame Challenge. http://worldsciencefestival.com/webcasts/cool_jobs_2012
7. The Flame Challenge — Winner Announced. www.flamechallenge.org/
8. The Flame Challenge — The Finalists. www.centerforcommunicatingscience.org/?page_id=1292
Еще о горении
Но на самом деле, в процессе горения топлива, например в автомобильном двигателе участвует около 300 тысяч реакций, из которых в настоящее время изучены только несколько десятков тысяч. Так что моделировать можно, но точно пока не получается…

Интересным явлением при горении, на которое обратил особое внимание в своих лекция еще Фарадей, является пламя. Появление пламени зависит от способности горящего тела или продуктов его разложения переходить при температуре горения в пары или газы, которые при горении нагреваются и светят. Накаленные пары и газы сами по себе светят мало и поэтому горение, например водорода, спирта, сопровождается бледным пламенем. Бледное, пламя можно сделать светящимся, внося в него мелкие частицы твердых тел. Разные вещества, находящиеся в пламени, будут окрашивать его в различные цвета.
Яркое пламя содержит какие-либо твердые частицы или, по крайней мере, очень плотные тяжелые пары. Пламя горящей свечи, дерева, парафина и т. п. веществ ярко светятся именно от частиц продуктов осмоления и угля, получающихся в результате пиролиза вещества при горении.
/Пиролиз – это процесс разложения соединений (органических) при высокой температуре без доступа окислителей (обычно воздуха). Отдельно выделяют пиролиз (“крекинг”) сырой нефти для получения сырья для нефтегазовой промышленности./
Т.е. недостаток воздуха и высокая температура порождает хемилюминесценцию)). А последнее выражает процесс свечения (люминесценции) продуктов реакции и других компонентов пламени в результате возбуждения их атомов (перехода на более высокие орбиты электронов и последующего возвращения с испусканием фотона).

Практически без пламени горят графит, кокс, древесный уголь и ряд других веществ потому, что они при горении не выделяют горючих газообразных продуктов (они сами являются остаточным продуктом пиролиза древесины и нефти). Наблюдаемое при горении этих веществ бледное синее пламя есть результат догорания окиси углерода, получающейся в результате восстановления углекислого газа на раскаленном угле.

Если в печке еще синеет пламя на угольках, – значит есть и окись углерода, и закрывать трубу заслонкой нельзя. Иначе горение прекратится, и помещение наполнится весьма опасным для жизни угарным газом (C=O). Можно “угореть”. Интересно, что причиной такого отравления является связывание угарным газом гемоглобина крови, в результате чего возникает недостаток кислорода, на который первым реагирует мозг человека. Таким образом, по сравнению с диоксидом углерода, окись является химически намного более активной и опасной для живых существ.
Пары и газы, выделяющиеся при горении обычных горючих веществ, как правило, не содержат свободного кислорода и для горения их необходим кислород воздуха, который проникает к месту горения путем диффузии, поэтому пламя имеет определенное строение.

Внутренняя зона (1) заполнена парами и продуктами разложения, выделяющимися из горючего вещества в результате его нагревания. Количество диффундирующего из окружающего воздуха кислорода в этой зоне мало и температура в этой зоне сравнительно невысока. На фотографии хорошо видно что первая зона имеет характерный окрас, усиливающийся к краям зоны, что связано с тем что в этой зоне происходит неполное горение с образованием СO являющимся источником синеватого окраса. По мере приближения к краям зоны количество диффундирующего кислорода увеличивается, и горение идет более интенсивно, что хорошо заметно по усилению окраса. В зоне (2), куда частично, проникает кислород воздуха, происходит окисление паров и продуктов разложения, но вследствие недостаточности кислорода именно в этой зоне происходит осмоление и образование мелких частиц угля и поэтому эта зона ярко светится (напомним что свечение пламени обусловлено наличием в пламени возвещенных частиц твердой фазы). Температура в этой зоне значительно выше, чем в зоне (1). В зоне (3) происходит догорание продуктов, образовавшихся уже в зоне (2), и частично тех паров и продуктов разложения, которые не успели прореагировать в зоне (2). Зона (3) содержит самое большое количество диффундировавшего кислорода т.к она является самой внешней и имеет наибольшую поверхность. При достатке кислорода происходит полное окисление паров до газообразных продуктов, поэтому именно в этой зоне выделяется наибольшее количество тепла. Температура в этой зоне еще выше, чем в зоне (2), но яркости пламени уже нет, т.к в зоне почти отсутствуют частицы недогоревшей твердой фазы.

Цвет пламени при горении органических веществ на воздухе зависит от их химического состава и, главным образом, от содержания в них кислорода и углерода. При содержании кислорода в горючем около 50% и выше пламя горения несветящееся, при меньшем содержании кислорода получается светящееся пламя, при содержании 60% и выше углерода появляется значительное количество копоти. Цвет пламени горючих веществ определяется присутствием в нем твердых частиц углерода. Если вместо углерода ввести в пламя другие твердые частицы, то пламя соответственно окрашивается. Так, например, если в бесцветное пламя метилового спирта ввести соли стронция, то пламя окрашивается в красный цвет, при введении солей бария – в зеленый, меди – в синий, натрия – в желтый. Вводимая в пламя соль при высокой температуре диссоциирует и образующиеся продукты диссоциации излучают характерные для них лучи.
Так, например, хлористый барий при высокой температуре диссоциирует по уравнению:
2BaCl2 => 2BaCl + Cl2
Монохлорид ВаСl излучает в зеленой линии спектра. Это свойство солей некоторых металлов используется при изготовлении самых разнообразных пиротехнических составов. Эти составы представляют собой механические смеси горючего, окислителя, добавки для получения цветного пламени и цементатора.

Одно из неприятных явлений, связанных с переходом горения в детонацию, – повышенный износ автомобильных двигателей.
озникающий при разгоне автомобиля стук является результатом детонации, одной из причин которой может быть раннее зажигание. При этом топливная смесь воспламеняется преждевременно, шатун, не довернувшись до конца, “стучит”, и растет температура в камере, что приводит к повреждению пар трения (задиры на коленвале и вкладышах) и преждевременному износу цилиндров. Возможной причиной детонации может также быть использование низкооктанового топлива (например А-76 вместо А-95) в современных двигателях, что приводит к слишком высокой степени сжатия и детонации (взрыву) топливной смеси. Признак детонации – черный дым выхлопа, падение мощности двигателя.

Горение и детонация взрывчатых веществ (ВВ) так же, как и горение обычных горючих тел, сопровождается появлением пламени.
Яркость и цвет пламени обычного горения ВВ зависит от состава ВВ. ВВ с неполным кислородным балансом, как например тротил, горит с выделением большого количества копоти – свободного углерода. ВВ с большим содержанием кислорода, как например тетрил, тэн, гексоген, горят с образованием белого яркого пламени. При детонации ВВ с неполным кислородным балансом так же, как и при горении, выделяется свободный углерод в виде графита. При детонации тротила образуется пламя, окрашенное в красноватый цвет, и клубы черного дыма.
При детонации нитроглицерина образуется ослепительно яркое пламя без дыма. При выстреле из артиллерийского орудия у среза ствола появляется пламя. Появление этого пламени обусловлено догоранием продуктов разложения пороха – окиси углерода, водорода – при непосредственном соприкосновении и смешении их с кислородом воздуха.

Образование значительного пламени при детонации ВВ, а также яркие вспышки при выстреле, практически представляют серьезные неудобства. Так, например, появление пламени при выстреле демаскирует орудие.
Появление пламени при детонации бризантных ВВ исключает возможность применения их для производства взрывных работ в каменноугольных шахтах, а также и для специальных целей военного дела. Дело в том, что в каменноугольных шахтах из пластов угля выделяется метан, который в смеси с воздухом образует смеси, способные к детонации. Точно так же мелкая угольная пыль в смеси с воздухом способна к детонации. Для приведения в состояние детонации этих смесей может служить пламя взрыва бризантных ВВ. Для предотвращения взрыва метано -воздушной и пылевой смеси при производстве взрывных работ в шахтах применяют так называемые антигризутные ВВ. Эти ВВ обычно представляют собой смеси бризантных ВВ с хлористыми солями калия или натрия.

Природа хемилюминесценции (свечения) огня при ядерном взрыве, и даже при термоядерной реакции на солнце та же, несмотря на более выоские плотности энергии и температуры, другие химические реакции.
Значительный интерес представляет собою явление «беспламенного» горения. Беспламенное горение осуществляется следующим образом. Смесь горючих газов или паров с воздухом направляется па нагретый до определенной температуры катализатор. При соприкосновении смеси с катализатором в тонком слое ее осуществляется химическая реакция окисления, сопровождающаяся выделением тепла, за счет которого катализатор сильно разогревается, однако газовая смесь продолжает гореть без пламени.
Одно время (в 80е-90е годы) в продаже появлялись специальные обогреватели для охотников на основе катализаторного горения, похожие на небольшую фляжку.
В качестве окислительного катализатора вначале применялась платина, в настоящее время исследователями найдены более дешевые катализаторы. Так, например, на основе шамота с примесью окислов никеля и железа получен очень хороший катализатор беспламенного горения. Активность катализатора беспламенного горения зависит от состоянии его поверхности.
Чем больше развита поверхность катализатора, тем выше его активность. Поверхность же катализатора увеличивается с повышением его пористости или степени дробления.




Безбоязненно используя огонь, человек отделяется от животных, становится выше их. Он позволил ему обрабатывать пищу, согревать жилище, осваивать холодные территории. Все современные технологии связаны, так или иначе, с использованием процессов горения, даже если не учитывать электро и тепловую энергии.
Но огонь, кроме добра, приносит также много горя и бед. Это пожары, огнестрельное оружие, бомбы.

Необходимо разумное использование и огня в себе. Чтобы и других обогреть, и себя не сжечь раньше времени и без пользы .
#Статьи
dnevniki.ykt.ru
Температура огня разных источников пламени
Температура огня заставляет в новом свете увидеть привычные вещи – вспыхнувшую белым спичку, голубое свечение горелки газовой печки на кухне, оранжево-красные язычки над пылающим деревом. Человек не обращает внимания на огонь, пока не обожжёт кончики пальцев. Или не спалит картошку на сковороде. Или не прожжёт подошву кроссовок, сохнущих над костром.
Когда первая боль, испуг и разочарование проходят, наступает время философских размышлений. О природе, цветовой гамме, температуре огня.

Горит, как спичка
Кратко о строении спички. Она состоит из палочки и головки. Палочки изготавливают из дерева, картона и хлопчатобумажного жгута, пропитанного парафином. Дерево выбирают мягких пород – тополь, сосну, осину. Сырьё для палочек называют спичечной соломкой. Чтобы избежать тления соломки, палочки пропитывают фосфорной кислотой. Российские заводы мастерят соломку из осины.
Головка спички проста по форме, но сложна по химическому составу. Темно-коричневая голова спички содержит семь компонентов: окислители – бертолетова соль и дихромат калия; стекляннюу пыль, сурик свинцовый, серу, костный клей, цинковые белила.
 Головка спички при трении воспламеняется, нагреваясь до полутора тысяч градусов. Порог воспламенения, в градусах Цельсия:
Головка спички при трении воспламеняется, нагреваясь до полутора тысяч градусов. Порог воспламенения, в градусах Цельсия:- тополь – 468;
- осина – 612;
- сосна – 624.
Температура огня спички равна температуре возгорания древесины. Поэтому белая вспышка серной головки сменяется желто-оранжевым язычком спички.
Если пристально разглядывать горящую спичку, то взгляду предстают три зоны пламени. Нижняя – холодная голубая. Средняя в полтора раза теплее. Верхняя – горячая зона.
Огненный художник
При слове «костёр» вспыхивают не менее ярко ностальгические воспоминания: дым костра, создающий доверительную обстановку; красные и желтые огни, летящие к ультрамариновому небу; переливы язычков с голубого до рубиново–красного цвета; багровые остывающие угли, в которых печётся «пионерская» картошка.
Изменяющийся колер пылающего дерева сообщает о колебаниях температуры огня в костре. Тление дерева (потемнение) начинается со 150°. Возгорание (задымление) происходит в интервале 250-300°. При одинаковом поступлении кислорода породы деревьев горят при несовпадающих температурах. Соответственно, градус костра тоже будет отличаться. Берёза горит при 800 градусах, ольха – при 522°, а ясень и бук – при 1040°.
 Но цвет огня также определяется химическим составом горящего вещества. Желтый и оранжевый цвет огню вносят соли натрия. Химический состав целлюлозы содержит и соли натрия, и соли калия, придающие пылающим углям дерева красный оттенок. Романтические голубые огоньки в древесном костре возникают из-за недостатка кислорода, когда вместо СО2 образуется СО – угарный газ.
Но цвет огня также определяется химическим составом горящего вещества. Желтый и оранжевый цвет огню вносят соли натрия. Химический состав целлюлозы содержит и соли натрия, и соли калия, придающие пылающим углям дерева красный оттенок. Романтические голубые огоньки в древесном костре возникают из-за недостатка кислорода, когда вместо СО2 образуется СО – угарный газ.Энтузиасты научных опытов измеряют температуру огня в костре прибором под названием пирометр. Изготовляют три типа пирометров: оптические, радиационные, спектральные. Это бесконтактные приборы, разрешающие оценивать мощность теплового излучения.
Изучаем огонь на собственной кухне
Кухонные газовые плиты работают на двух видах топлива:
- Магистральный природный газ метан.
- Пропан–бутановая сжиженная смесь из баллонов и газгольдеров.
Химический состав топлива определяет температуру огня газовой плиты. Метан, сгорая, образует огонь мощностью 900 градусов в верхней точке.
Сжигание сжиженной смеси даёт жар до 1950°.
Внимательный наблюдатель отметит неравномерность раскраски язычков горелки газовой плиты. Внутри огненного факела происходит деление на три зоны:
- Тёмный участок, расположенный возле конфорки: здесь нет горения из-за недостатка кислорода, а температура зоны равна 350°.
- Яркий участок, лежащий в центре факела: горящий газ разогревается до 700°, но топливо сгорает не до конца из-за недостатка окислителя.
- Полупрозрачный верхний участок: достигает температуры 900°, и сгорание газа полноценное.
Цифры температурных зон огневого факела приведены для метана.
Правила безопасности при огневых мероприятиях
Разжигая спички, камин, газовую плиту, позаботьтесь о вентиляции помещения. Обеспечьте приток кислорода к топливу.
Не пытайтесь самостоятельно ремонтировать газовое оборудование. Газ не терпит дилетантов.
 Хозяйки отмечают, что горелки светятся голубым цветом, но иногда огонь становится оранжевым. Это не глобальное изменение температуры. Изменение цвета связано с изменением состава топлива. Чистый метан горит без цвета и без запаха. В целях безопасности в бытовой газ добавляют серу, которая при сгорании окрашивает газ в голубые оттенки и сообщает продуктам сгорания характерный запах.
Хозяйки отмечают, что горелки светятся голубым цветом, но иногда огонь становится оранжевым. Это не глобальное изменение температуры. Изменение цвета связано с изменением состава топлива. Чистый метан горит без цвета и без запаха. В целях безопасности в бытовой газ добавляют серу, которая при сгорании окрашивает газ в голубые оттенки и сообщает продуктам сгорания характерный запах.Появление оранжевых и желтых оттенков в огне конфорки сообщает о необходимости профилактических манипуляций с плитой. Мастера прочистят оборудование, удалят пыль и сажу, горение которых и изменяет привычный цвет огня.
Иногда огонь в горелке становится красным. Это сигнал опасного содержания угарного газа в продуктах сгорания. Поступления кислорода к топливу настолько мало, что плита даже тухнет. Угарный газ без вкуса и запаха, и человек рядом с источником выделения вредного вещества заметит слишком поздно, что отравился. Поэтому красный цвет газа требует немедленного вызова мастеров для профилактики и наладки оборудования.
fb.ru