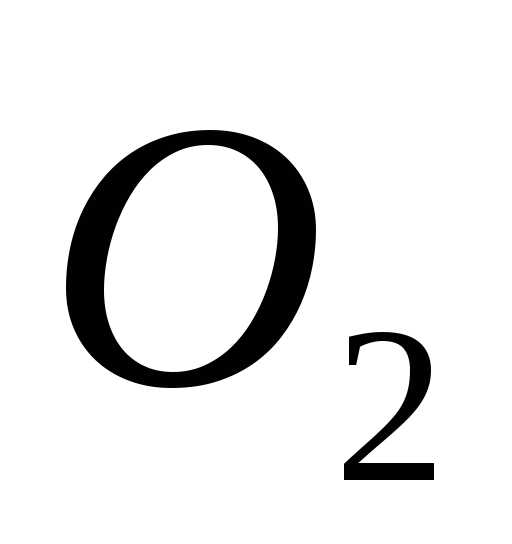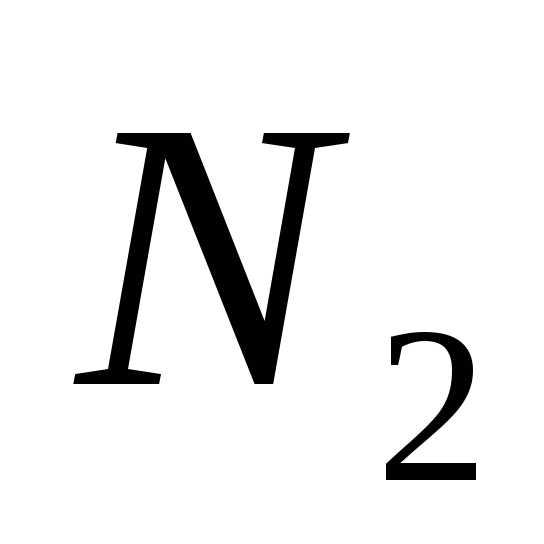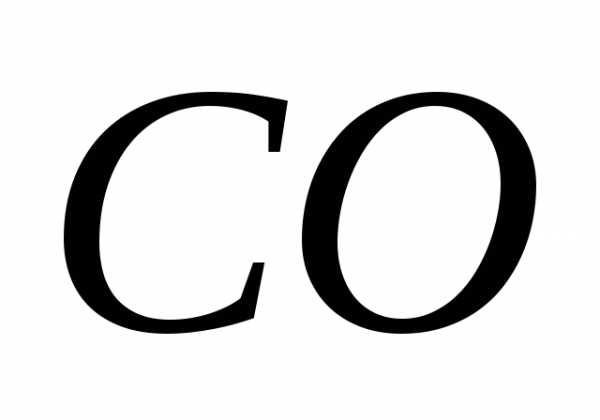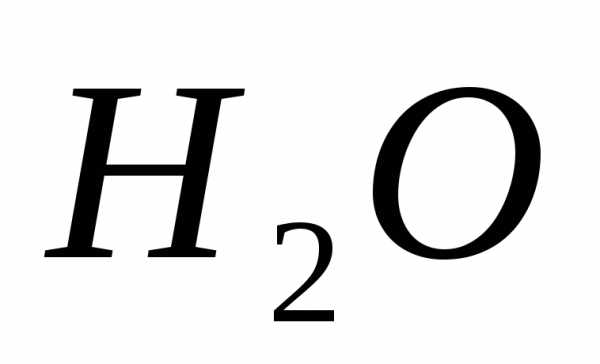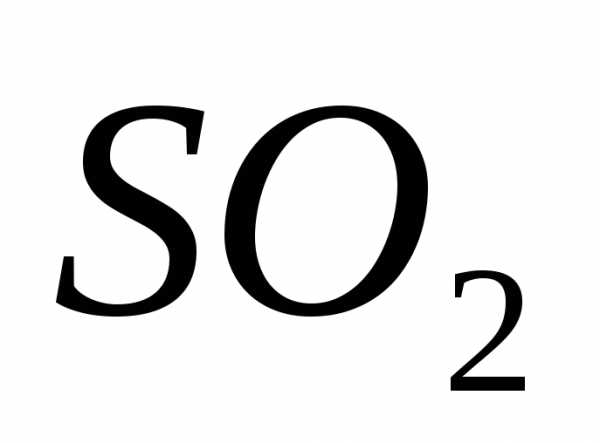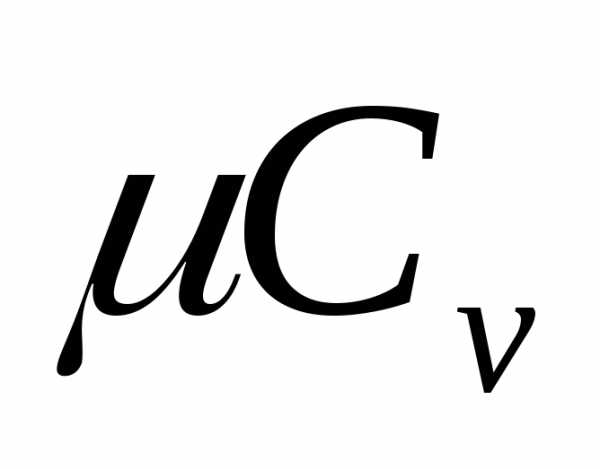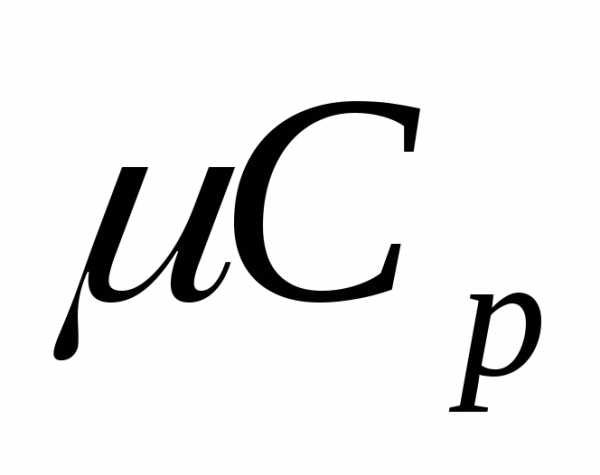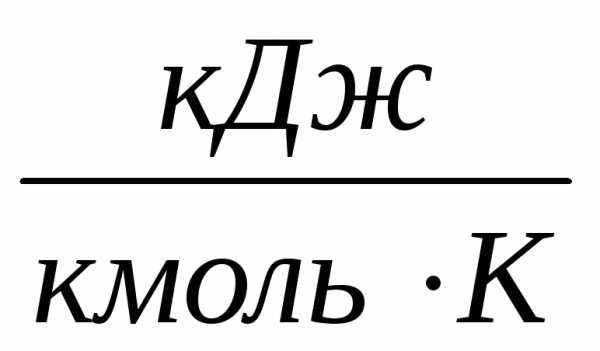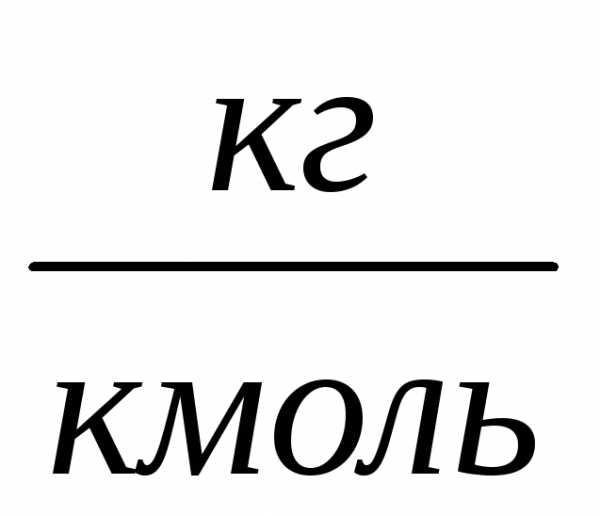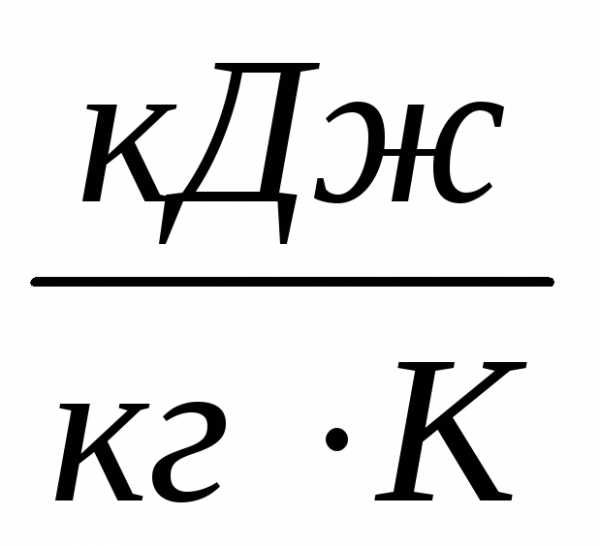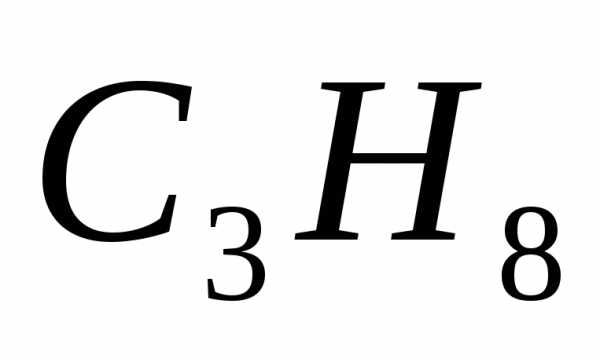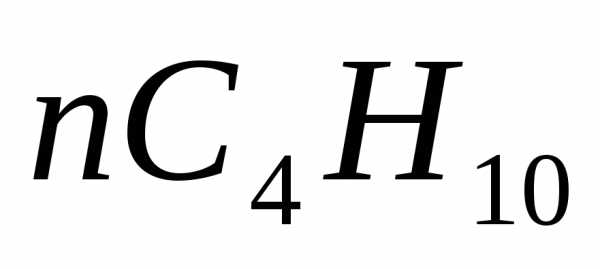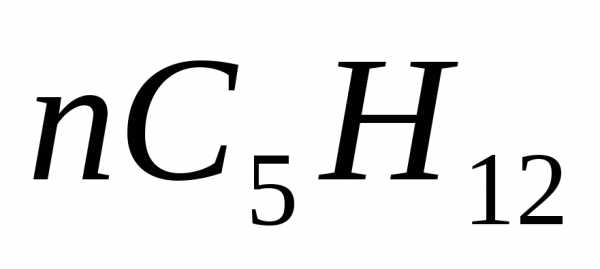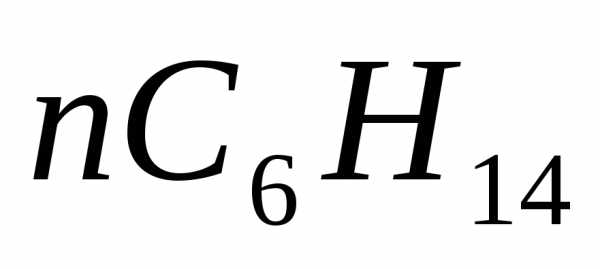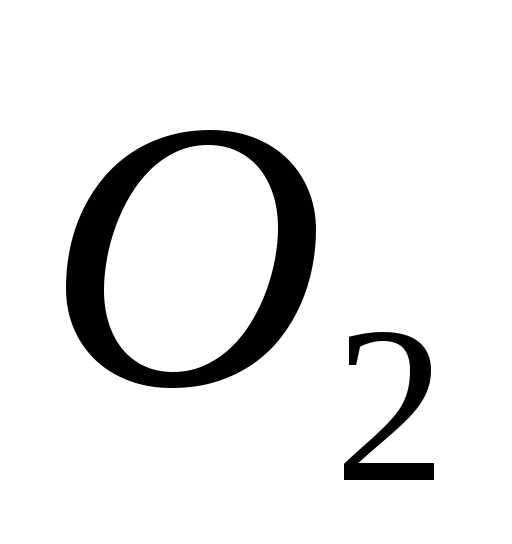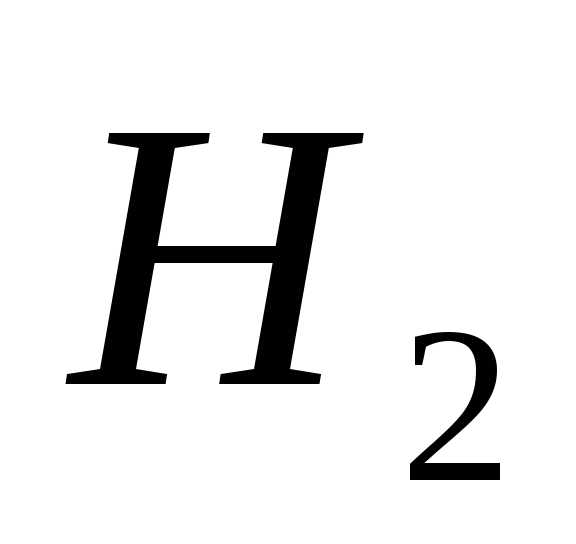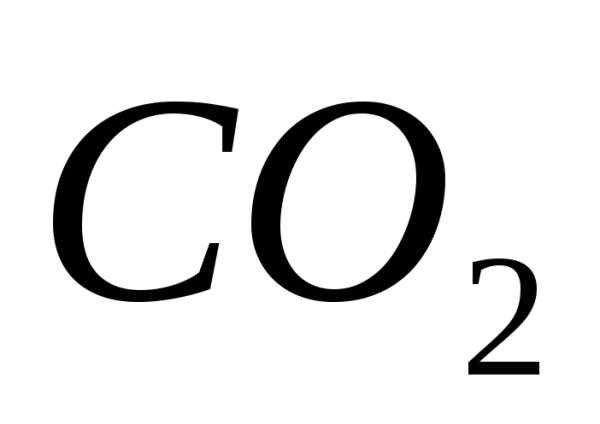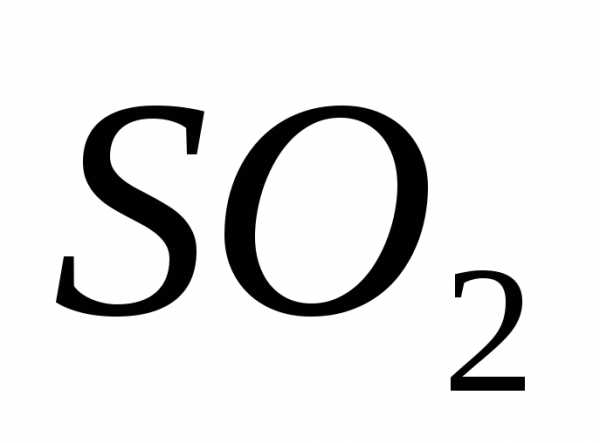Андрианова — Сборник задач по технической термодинамике | ТЕПЛОТА
Андрианова — Сборник задач по технической термодинамике
Задачник составлен в соответствии с программой курса «Техническая термодинамика» для теплотехнических и теплофизических специальностей энергетических вузов и факультетов.
Все задачи снабжены ответами, а наиболее типичные — подробными решениями.
Предлагаемый задачник предназначен в качестве учебного пособия для студентов теплотехнических и теплофизических специальностей энергетических втузов и факультетов и отвечает соответствующей программе курса «Техническая термодинамика». Задачник может быть использован при упражнениях на практических занятиях в аудитории и дома. Этой книгой могут пользоваться и студенты других, неэнергетических втузов.
Работая над задачником, авторы использовали свой опыт педагогической работы в Московском ордена Ленина энергетическом институте и расположили материал в такой последовательности, в какой обычно излагается программа курса в МЭИ.
Ввиду того что в Советском Союзе с 1 января 1963 г введена как предпочтительная международная система единиц (СИ), большая часть задач дана в этой системе Авторы ‘испытывали затруднения применяя ее, в связи с тем, что, составляя задачи, они не сполагали нормативными материалами «(таблицы и диаграммы водяного пара, таблицы термодинамических свойств газов и др.), оставленными по новой системе. Часть задач и ответов к ним даны В старых единицах, что авторы считают необходимым, учитывая сложность «переходного» периода. Сущность системы, ее положи тельные стороны и отличие от технической системы авторы постарались подчеркнуть в решениях некоторых задач раздела «Параметры состояния» и «Первый закон термодинамики»
Содержание некоторых разделов заметно отличается от того материала, который предлагался в ранее изданных задачниках. Так, составляя раздел «Реальные газы», авторы предложили задачи, даю щие некоторые понятия о способах обработки экспериментального материала (‘применение метода конечных разностей, пользование таб лицами и диаграммами обобщенных свойств веществ). Эти задачи могут быть полезными для студентов-теплофизиков. Задачи подобно го типа могут быть предложены для домашних упражнений В разделе «Теплоемкость газов в идеальном состоянии» авторы сочли нужным поместить несколько простейших задач па вычисление теплоемкостей газов по формуле Эйнштейна, для того чтобы дать хотя бы некоторое представление о том, как вычисляются термоди намические функции при помощи квантовой теории теплоемкости
В разделе «Влажный воздух» приведены задачи с применением I-d-диаграммы для повышенных давлений воздуха.
В задачах разделов «Циклы газотурбинных установок и реактивных двигателей» и «Циклы паротурбинных установок» обращено вни мание на влияние необратимости процессов иа к. п. д. установок, а также помещены задачи, рассматривающие новые циклы парогазовых установок
Авторы не сочли необходимым отдельно выделять тему «дифференциальные уравнения термодинамики» и решили применять эти равнения з соответствующих -разделах, там. оде это необходимо. Наиболее характерные задачи приведены с решениями.
Ниже представлено содержание книги Андрианова — Сборник задач по технической термодинамике
1. Параметры состоянии
2. Первый закон термодинамики
3. Законы и уравнение состояния идеальных газов
4. Теплоемкость газов в идеальном состоянии
5. Смеси идеальных газов
6. Процессы изменения состояния идеальных газов
7. Второй закон термодинамики
8. Реальные газы
9. Свойства воды и водяного пара процессы изменения его состояния
10. Влажный воздух
11. Термодинамика газовых потоков
12. Компрессоры циклы двигателей внутреннего сгорания
13. Циклы газотурбинных установок и реактивных двигателей
14. Циклы паротурбинных установок
15. Циклы холодильных машин
16. Элементы термодинамики химических процессов
Скачать — Андрианова — Сборник задач по технической термодинамике>>
www.teplota.org.uaРешение задач по термодинамике | Решатель
Для успешного решения задач по данной теме необходимо знать закон сохранения энергии для термодинамики. Его же называют первым началом. Суть его состоит в том, что, когда термодинамическая система получает извне какое-то количество теплоты, то часть энергии добавляется к внутренней энергии системы, а другая возвращается в процессе совершения системой работы наружу, то есть:
,
где все величины алгебраические.
Для идеального газа изменение внутренней энергии , где i = 3 – степень свободы молекул, для реального газа i зависит от строения молекулы. Так для двухатомной молекулы i = 5, для трехатомной – i = 6 и т.д.
Работу A газ совершает только при изменении объема, т.е. . Надо сказать, что мы получаем три случая, когда один из членов первого начала термодинамики равен
- Q = 0 – это адиабатический процесс, изменение состояния происходит без обмена энергией с внешней средой. A = -ΔU.
- ΔU = 0 – это изотермический процесс, так как внутренняя энергия не изменяется, а, значит не изменяется и температура. Q = A = pΔV, T = const.
- A = 0 – это изохорический процесс, так как газ не совершает работу, а значит и не меняет объема. , V = const.
Наконец, изобарический процесс, в котором энергия расходуется на изменение внутренней энергии и на работу. , p = const.
Также необходимо знать еще 4 формулы, которые помогут нам в решении задач:
- Количество теплоты, которое поглощается при нагревании или выделяется при охлаждении , где с – удельная теплоемкость, т.е. сколько теплоты понадобится передать или отнять у единицы массы вещества для изменения его температуры на 1 o.
Также различают Cv – теплоемкость при постоянном объеме и Cp — теплоемкость при постоянном давлении. Причем и . Соответственно, удельные теплоемкости будут и , где μ – количество вещества в молях. - Количество теплоты, которое поглощается при плавление или выделяется при кристаллизации Q = λm, где λ – удельная теплота плавления.
- Количество теплоты, которое поглощается при парообразовании или выделяется при конденсации Q = rm, где r — удельная теплота парообразования.
- Количество теплоты, которое выделяется при сгорании вещества Q = qm, где q — удельная теплота сгорания.
Все эти удельные величины берутся из справочных таблиц.
В системе, которая не взаимодействует с внешней средой, т.е. в замкнутой, между элементами системы происходит исключительно теплообмен:
где — вся полученная тепловая энергия, — вся отданная тепловая энергия – это закон теплового равновесия.
В итоге все задачи по термодинамике решаются следующим образом:
- Перевести все заданные величины в единицы СИ.
- Определить вид происходящего процесса, т.е., какие параметры остаются неизменными – T, V или P, определить, какие тела входят в замкнутую систему в теплообменных процессах и что с ними происходит.
- Выбрать из справочника необходимые табличные удельные величины или рассчитать, зная степени свободы молекул и молярные массы веществ.
- Применяя формулы, описанные выше, а так же формулы из других разделов физики, решить задачу.
Ниже рассмотрим пару примеров решения задач.
Задача 1. Закрытый сосуд содержит 14 г азота, давление p1 = 0.1 МПа, а температура t = 27oC.
Когда сосуд нагрели, давление увеличилось впятеро. Какая была конечная температура азота? Найти емкость сосуда V и количество теплоты Q, затраченное на нагревание.
Решение.
Состояние азота до нагревания (1), после нагревания (2).
Так как сосуд закрыт, процесс изохорический, т.е. V = const и все тепло уходит на изменение внутренней энергии азота.
Найдем конечную температуру азота:
Решая совместно (1) и (2), получаем:
Количество теплоты, полученное азотом:
где Дж/(моль · K). i = 5, т.к. молекула азота состоит из 2 атомов.
Задача 2. Сколько нужно сжечь керосина, чтобы полностью испарить 100 г воды, температура которой 20oC? К.П.Д. керосинового нагревателя η = 0,2.
Решение.
Тепловая энергия сгорания керосина Qк = qmк
Составляем уравнение теплового баланса Qк — Qн — Qп = 0:
Откуда кг.
В заключение рекомендуемая литература (теоретический материал и примеры решения задач):
- Молекулярная физика и термодинамика. Исаков А.Я. (2007)
- Сивухин Д.В. и др. Сборник задач по общему курсу физики. В 5 томах. Том II. Термодинамика и молекулярная физика. (5-е изд., 2006)
- Основные принципы термодинамики. Белоконь Н.И. (1968)
Решение термодинамики на заказ
Статья написана нашим специалистом по термодинамике, гидравлике и теплотехнике. Он также выполняет заказы по решению задач. Заказать работу можно через нашу форму на сайте.
reshatel.org
Техническая Термодинамика – Стр 4
ЛИТЕРАТУРА
Баскаков А. П. и др. Теплотехника. Учеб. для вузов. – 2-е изд., перераб. – М.: Энергоатомиздат, 1991. – 224 с.
Лариков Н. Н. Теплотехника. Учеб. для вузов. – 3-е изд., перераб. и доп. – М.: Стройиздат, 1985. – 432 с.
Рабинович О. М. Сборник задач по технической термодинамике. – М.: Машиностроение, 1973. -344 с.
Андрианова Т.Н., Дзампов Б.В., Зубарев В.Н., Ремизов С.А. Сборник задач по технической термодинамике для вузов. -М.: Энергоиздат, 1981.- 240с.
Ривкин С.Л., Александров А.А. Термодинамические свойства воды и водяного пара. Справочник.- Энергоатомиздат, 1984.- 45 с.
ПРИЛОЖЕНИЕ 1.1
РАСЧЕТ СРЕДНЕЙ МАССОВОЙ ТЕПЛОЕМКОСТИ КОМПОНЕНТЫ ГАЗОВОЙ СМЕСИ
Для углеводородных газов средняя массовая теплоемкость при постоянном давлении EMBED Equation.3
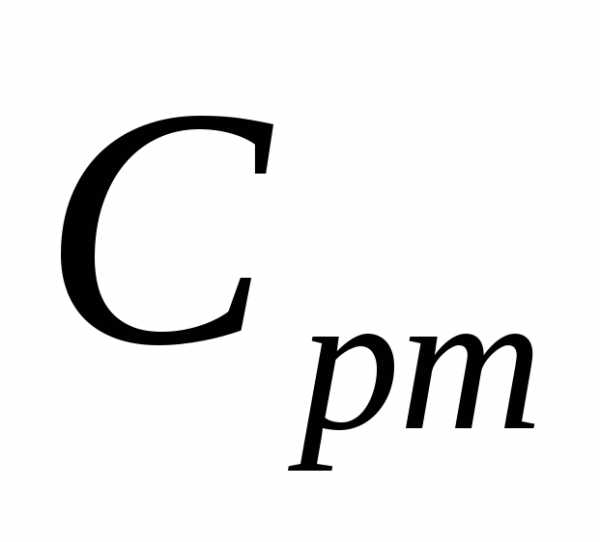 может приниматься приближенно при
EMBED Equation.3
может приниматься приближенно при
EMBED Equation.3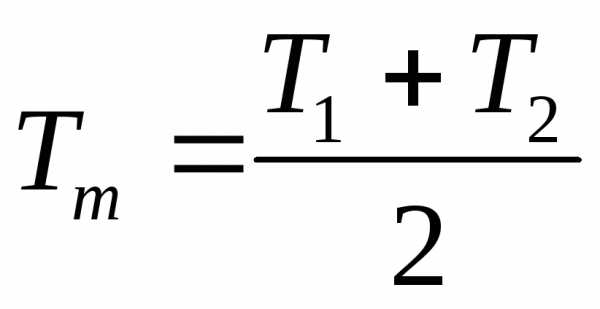 по соответствующим графикам на рис.
2.3…2.8.
по соответствующим графикам на рис.
2.3…2.8.Для неуглеводородных составляющих средняя массовая теплоемкость при постоянном давлении EMBED Equation.3
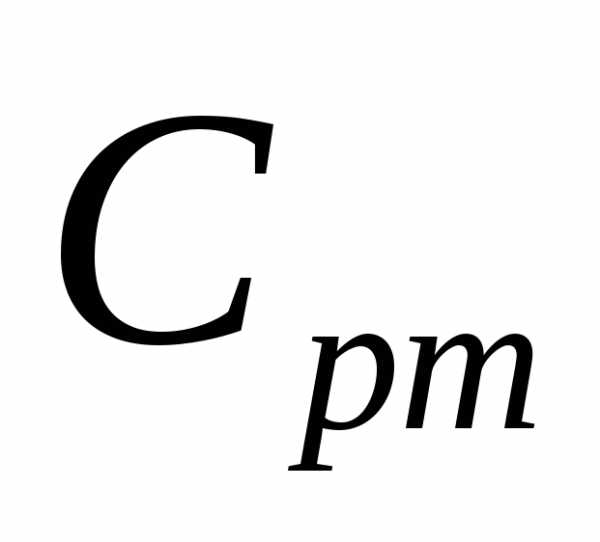 должна рассчитываться через истинную
мольную теплоемкость при постоянном
давлении EMBED Equation.3
должна рассчитываться через истинную
мольную теплоемкость при постоянном
давлении EMBED Equation.3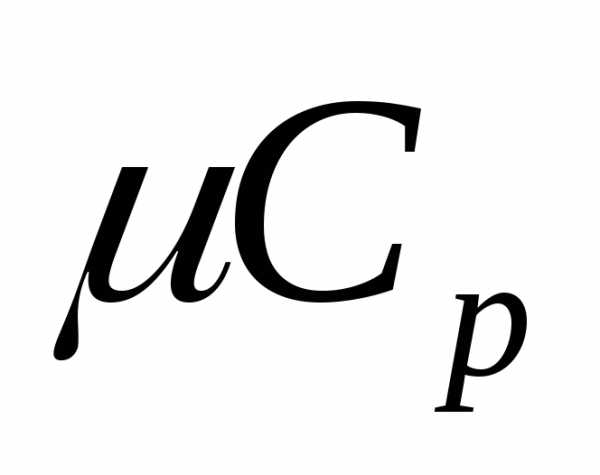 в следующей последовательности:
в следующей последовательности:
EMBED Equation.3 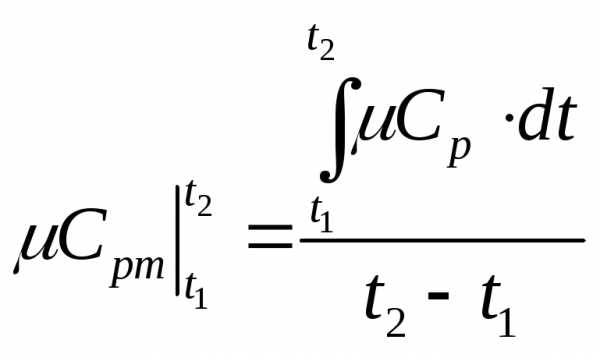 ;
;
EMBED Equation.3 
где EMBED Equation.3 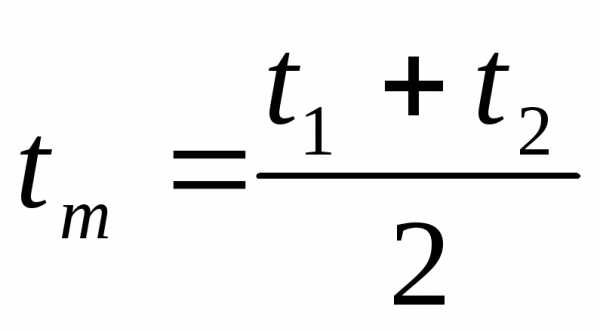 ;
;
EMBED Equation.3 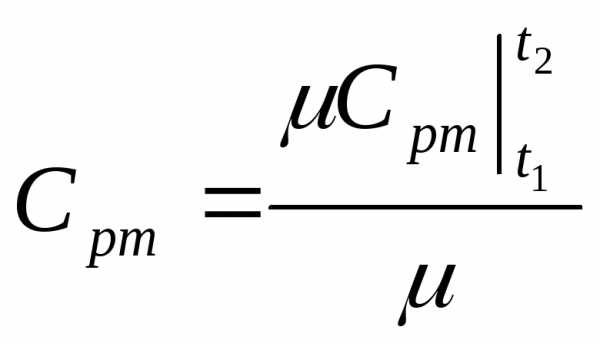 .
.
Для ориентировочных расчетов принимают теплоемкость не зависящей от температуры. Постоянные мольные теплоемкости приведены в табл. 2 приложения 1.
Продолжение приложения 1.1
Таблица 1
Интерполяционные формулы для истинных мольных теплоемкостей неуглеводородных газов
Газ | Мольная теплоемкость при EMBED Equation.3 |
EMBED Equation.3 | EMBED Equation.3 |
EMBED Equation.3 | EMBED Equation.3 |
EMBED Equation.3 | EMBED Equation.3 |
Воздух | EMBED Equation.3 |
EMBED Equation.3 | EMBED Equation.3 |
| EMBED Equation.3 |
EMBED Equation.3 | EMBED Equation.3 |
EMBED Equation.3 | EMBED Equation.3 |
Таблица 2
Приближенные значения мольных теплоемкостей при постоянном объеме и постоянном давлении ( EMBED Equation.3 )
Газ | EMBED Equation.3 | EMBED Equation.3 | k |
EMBED Equation.3 | |||
Одноатомные | 12,56 | 20,93 | 1,67 |
Двухатомные | 20,93 | 29,31 | 1,40 |
Трех- и многоатомные | 29,31 | 37,68 | 1,29 |
Продолжение приложения 1.1
Таблица 3
Молярные массы
EMBED Equation.3 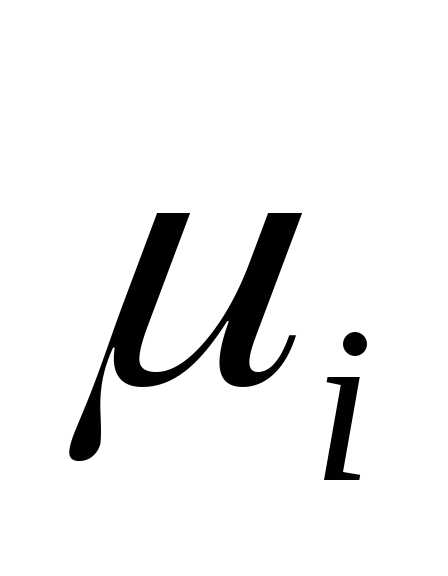 и газовые постоянные EMBED Equation.3
и газовые постоянные EMBED Equation.3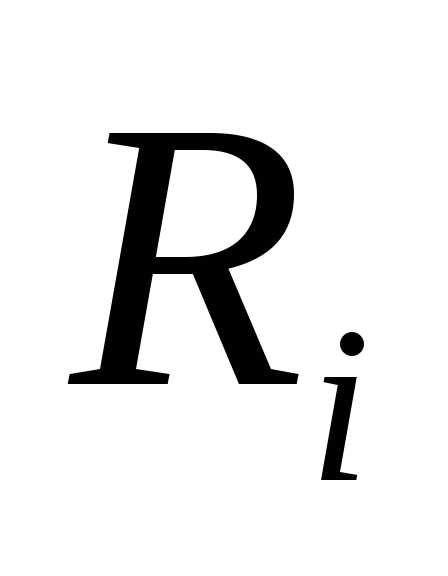 компонентов газовой смеси
компонентов газовой смеси
Газ | Химическая формула | Молярная
масса, EMBED Equation.3 | Газовая
постоянная, EMBED Equation.3 |
Метан | EMBED Equation.3 | 16,04 | 518,67 |
Этан | EMBED Equation.3 | 30,07 | 276,64 |
Пропан | EMBED Equation.3 | 44,09 | 197,70 |
н-Бутан | EMBED Equation.3 | 58,12 | 143,08 |
н-Пентан | EMBED Equation.3 | 72,15 | 115,23 |
н-Гексан | EMBED Equation.3 | 86,17 | 69,48 |
Кислород | EMBED Equation.3 | 32,00 | 259,0 |
Водород | EMBED Equation.3 | 2,02 | 4124,0 |
Азот | EMBED Equation.3 | 28,03 | 296,8 |
Окись углерода | EMBED Equation.3 | 28,01 | 296,8 |
Водяной пар | EMBED Equation.3 | 18,02 | 461 |
Двуокись углерода | EMBED Equation.3 | 44,01 | 188,9 |
Сернистый газ | EMBED Equation.3 | 64,06 | 129,8 |
Воздух | – | 28,96 | 287,0 |
studfiles.net
Сборник задач по технической термодинамике
Задачник составлен в соответствии с программой курса «Техническая термодинамика» для теплотехнических и теплофизических специальностей энергетических вузов и факультетов.
Все задачи снабжены ответами, а наиболее типичные — подробными решениями.
Предлагаемый задачник предназначен в качестве учебного пособия для студентов теплотехнических и теплофизических специальностей энергетических…
Все задачи снабжены ответами, а наиболее типичные — подробными решениями.
Предлагаемый задачник предназначен в качестве учебного пособия для студентов теплотехнических и теплофизических специальностей энергетических втузов и факультетов и отвечает соответствующей программе курса «Техническая термодинамика». Задачник может быть использован при упражнениях на практических занятиях в аудитории и дома.
Этой книгой могут пользоваться и студенты других, не энергетических втузов.
Книга «Сборник задач по технической термодинамике» авторов Борис Васильевич Дзампов, Владимир Николаевич Зубарев, Серафим Александрович Ремизов, Тамара Николаевна Андрианова оценена посетителями КнигоГид, и её читательский рейтинг составил 5.64 из 10.
Для бесплатного просмотра предоставляются: аннотация, публикация, отзывы.
Работа авторов Борис Васильевич Дзампов, Владимир Николаевич Зубарев, Серафим Александрович Ремизов, Тамара Николаевна Андрианова «Сборник задач по технической термодинамике» принадлежит к жанру «Физика».
Онлайн библиотека КнигоГид непременно порадует читателей текстами иностранных и российских писателей, а также гигантским выбором классических и современных произведений. Все, что Вам необходимо — это найти по аннотации, названию или автору отвечающую Вашим предпочтениям книгу и загрузить ее в удобном формате или прочитать онлайн.
…knigogid.ru
| |
aeterna.qip.ru