58. Суть адсорбционных методов очистки газов. Типы адсорбентов.
Адсорбционные методы очистки основаны на поглощении примесей твердыми телами с развитой поверхностью, адсорбентами. Поглощаемые молекулы удерживаются на поверхности твердых тел силами
Ван-дер-Ваальса(физическая адсорбция) или химическими силами( хемосорбция). Стадии адсорбции: – перенос молекул газа к внешней поверхности твердого тела – проникновение молекул газа в поры твердого тела – собственно адсорбция. Адсорбция рекомендуется для очистки газов с невысокой концентрацией вредных компонентов. Адсорбированные вещества удаляют из адсорбентов с помощью десорбции инертным газом или паром. Преимущество: высокая степень очистки. Недостатки: “чистые” (сухие и без пыли) газы, небольшая скорость. Адсорбенты – материалы высокоразвитой внутренней поверхностью(природные и синтетические) : активированные угли, силикагели, алюмогели, цеолиты, иониты.
59. Каталитические методы.
связанны с химическим превращением токсичных компонентов в нетоксичные в присутствии катализаторов. Аппараты – реакторы различной конструкции. Используются для очистки от: оксидов азота, серы, углерода и от органических примесей.
Оксид азота восстанавливается газом – восстановителем(CO,CH(4)…) в присутствии катализаторов. В качестве катализаторов используют различные металлы, которыми покрывают огнеупорные материалы (носители). Часто применяют палладиевый катализатор, нанесенный на оксид алюминия. Температура 400 470 гр. Реакции: — 4NO + CH(4) = CO(2) + 2H(2)O + 2N(2) — 2NO(2) + CH(4) = CO(2) + 2H(2)O + N(2) — 2NO + 2H(2) = N(2) + 2H(2)O — 2NO(2) + 4H(2) = N(2) + 4H(2)O — 2NO + PCO → N(2) + 2CO(2) — 2NO(2) + 4CO → N(2) + 4CO(2)—
Очистка от оксида углерода является наиболее рациональной. Процесс гидрирования оксида углерода на никелевых и железных катализаторах проводят при высоких давлениях и повышенных температурах: — CO + 3H(2) = CH(4) + H(2)O — C)(2) + 4H(2) = CH(4) + 2H(2)O — 1/2O(2) + H(2) = H(2)O—
Очистка от диоксида серы – основана на принципе окисления SO(2) и SO(3) контактным методом. Используют метод очистки с получением сульфата аммония, который можно использовать как удобрение. SO(2) окисляют до SO(3) в присутствии V(2)O(5) при 450 –480 гр. Затем при температуре 220-260 гр. Вводят газообразный аммиак. Полученные кристаллы сульфата аммония отделяют в циклонах и электрофильтрах.
Каталитическая очистка газов от органических веществ. В качестве катализаторов используют Cu, Cr, Co, Mn, Ni … в отдельных случаях бокситы, цеолиты. Катализаторы условно делятся на: – цельнометаллические ( металлы платиновой группы или неблагородные металлы, нанесенные на ленты, сетки, спирали из нержавеющей стали) – смешанные ( металлы платиновой группы или оксиды неблагородных металлов, нанесенные на оксид алюминия, нержавеющую сталь ) – керамические ( -=-, нанесенные на керамическую основу в виде сот или решеток) – насыпные ( гранулы или таблетки из оксида алюминия с нанесенными на него металлами платиновой группы или оксидами неблагородных металлов, зерна оксидов небл. Мет.) Преимуществом обладают катализатор, нанесенные на мет носители. Они более термостабильны, прочны, с легкой регенерацией.
Очистка газов от серо-органических соединений заключается в их окислении при повышенных температурах. Каталитическое окисление производят кислородом, образованием кислородных соединений серы. В качестве катализаторов процессов гидрирования серо-органических соединений водородом используют контактные массы на основе оксидов Fe, Co, Ni, Cu, Zn. При гидрировании водяным паром используют катализаторы, содержащие в качестве компонента оксид железа.
Задача. Концентрация растворимого соединения А в сточной воде составляет СА. Во сколько раз необходимо разбавить эту воду, чтобы можно было сливать ее в канализацию, если известна ПДК соединения А?
Снд=0,0005 моль/л m=νM
ПДКнд=0,0005мг/л mнд=0,0005*200=0,1 г
СNO3-=0.01 моль/л m=νM
ПДКNO3-=45мг/л mNO3-=0,01*62=0,62 г
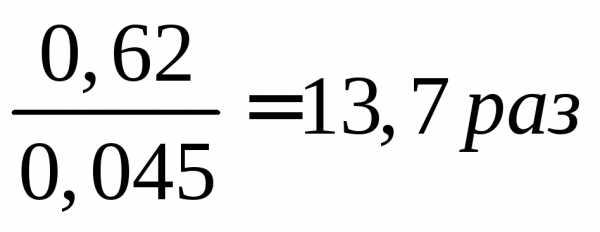
СNO2-=0,5 моль/л m=νM
ПДКNO2-=3,3мг/л mNO3-=0,5*46=23 г
Задача. В воздухе обнаружено присутствие примесей А, В, С в концентрациях С А, СВ, СС. Соотв. ли установленным нормативам качество воздуха, если ПДК этих веществ равны соотв. ПДКА, ПДКВ, ПДКС? При ответе учесть эффект суммации.
находится по формуле:
если ≤1, то соответствует, если неравенство не выполняется, значит концентрация в воздухе вредных примесей превышает нормам.
Задача. Жесткость некоторого образца воды обусловливается только дикарбонатом магния. При кипячении 0,5 л воды в осадок выпало 14 мг Mg(OH)2. Чему равна жесткость воды?
Решение 1.
, или
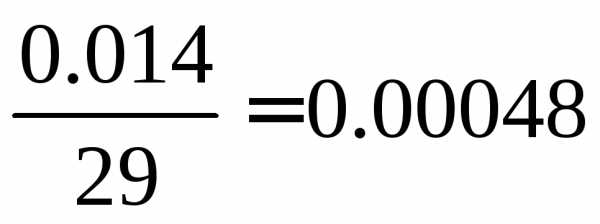 эквивалентной
массы, или
эквивалентной
массы, или
0,48 мэкв Mg(OH)2
В 0,5 л воды содержится 0,48 мэкв Mg(OH)2,
жесткость
воды равна 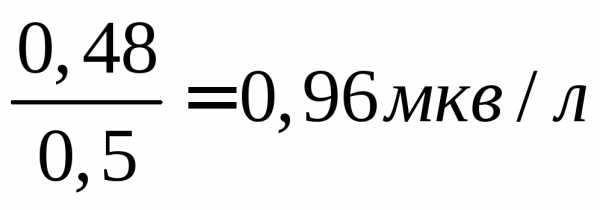
Решение 2.
В 1 л воды содержится 0,014/0,5 = 0,028 г Mg(OH)2,
что составляет 0,028/0,029=0,00096 г-экв или 0,96 мг-экв (29 – эквивалент Mg(OH)2)
Следовательно, жесткость воды 0,96 мг-экв
Задача. Чему равна жесткость (в ммоль/л) 0,003 М раствора MgCl2?
0,003 М MgCl2
0,003 М = 0,003 моль/л = 3ммоль/л
Задача. На титрование 0,5 л образца воды израсходовано 22,8 мл 0,1 н НС1. Чему равна карбонатная жесткость воды?
VH2O=0.5 л 0,1н HCl
VHCl=22,8 мл
Задача. Сколько л 20 % соляной кислоты, плотностью 1,098 г/см3, потребуется для нейтрализации 700л 5 М щелочной сточной воды?
1 л раствора имеет массу 1098 г и содержит 1098*0,20=219,60 г HCl, что составляет
C1V1 = C2V2
700л*5М=Хл*6МЗадача. Рассчитайте минимальный объем (в литрах) 15 % раствора соды (плотность 1,158 г/мл), необходимый для устранения жесткости 100 л природной воды с содержанием гидрокарбонат-ионов, равным 0,61 г/л.
1 л раствора имеет массу 1158 г и содержит 1158*0,15=173,7 г Na2CO3
C1V1 = C2V2
100*0,61=Х*173,7
Задача. Диоксид углерода поглощают раствором гидроксида кальция. Вначале образуется осадок, затем он исчезает. Определите общий объем газа (в литрах, н.у.), израсходованный при образовании 74 г осадка.
Задача. Смесь бромидов натрия и калия применяют в медицине как успокоительное средство. Найдите число бромид-ионов, поступивших в организм после приема 10 мл раствора, содержащего по 30 г бромида натрия и бромида калия в 1 л.
ν=30/103=0,29 моль NaBr
ν=30/119=0,25 моль KBr
[Br]–общ=0,29+0,25=0,54 моль/л
0,54 моль – 1000 мл
Х – 10 мл
число Br–=5.4*10-3=32.5*1020
Задача. Газовая смесь содержит СО2, СО, О2 и N2. При анализе 100 мл смеси методом химического поглощения получены следующие результаты.
Компонент | Количество газа после поглощения, мл |
СО2 | 83,20 |
| О2 | 82.40 |
СО | 75.60 |
N2 | 75,60 |
Определите количественный состав смеси (объемный %), если происходит последовательное поглощение газов из смеси, a N2 не поглощается.
VCO2=83,20 мл
VО2=82,40 мл
VСО=75,60 мл
VN2=75,60 мл
Vобщ=83,20+82,40+75,60+75,60=316,80 мл

81
studfiles.net
58. Суть адсорбционных методов очистки газов. Типы адсорбентов.
Адсорбционные методы очистки основаны на поглощении примесей твердыми телами с развитой поверхностью, адсорбентами. Поглощаемые молекулы удерживаются на поверхности твердых тел силами
Ван-дер-Ваальса(физическая адсорбция) или химическими силами( хемосорбция). Стадии адсорбции: – перенос молекул газа к внешней поверхности твердого тела – проникновение молекул газа в поры твердого тела – собственно адсорбция. Адсорбция рекомендуется для очистки газов с невысокой концентрацией вредных компонентов. Адсорбированные вещества удаляют из адсорбентов с помощью десорбции инертным газом или паром. Преимущество: высокая степень очистки. Недостатки: “чистые” (сухие и без пыли) газы, небольшая скорость. Адсорбенты – материалы высокоразвитой внутренней поверхностью(природные и синтетические) : активированные угли, силикагели, алюмогели, цеолиты, иониты. Активированные угли – гидрофобны. Для адсорбции газов и паров используют микропористые гранулированные активированные угли. Силикагели – гидратированные аморфные кремнеземы (SiO(2)nH(2)O), являющиеся реакционно-способными соединениями переменного состава, превращения которых идет по механизму полконденсации. Зазоры м/у частицами образуют пористую структуру селикагеля. Получают путем осаждения аморфного кремнезема из силикатно-щелочных металлов. Служат для поглощения полярных веществ. Алюмогели ( Al(2)O(3)*nH(2)O где 0< n < 6) – получают прокаливанием различных гидроксидов алюминия. Используют для улавливания полярных органических соединений и осушки газов. Цеолиты – алюмосиликаты, содержащие в своем составе оксиды щелочных и щелочноземельных металлов. Характеризуются регулярной структурой пор, соизмеримых с размерами молекул. Общая химическая формула: Me(2/n)C*Al(2)O(3)*xSi(2)*yH(2)O, где Me катион металла, n – его валентность. Получают синтетически и добывают при разработки месторождений. Обладают наибольшей адсорбцией по парам полярных соединений и веществ с кратными связями в молекулах. Иониты – высокомолекулярные соединения с развитой поверхностью.
59. Каталитические методы.
связанны с химическим превращением токсичных компонентов в нетоксичные в присутствии катализаторов. Аппараты – реакторы различной конструкции. Используются для очистки от: оксидов азота, серы, углерода и от органических примесей.
Оксид азота восстанавливается газом – восстановителем(CO,CH(4)…) в присутствии катализаторов. В качестве катализаторов используют различные металлы, которыми покрывают огнеупорные материалы (носители). Часто применяют палладиевый катализатор, нанесенный на оксид алюминия. Температура 400 470 гр. Реакции: — 4NO + CH(4) = CO(2) + 2H(2)O + 2N(2) — 2NO(2) + CH(4) = CO(2) + 2H(2)O + N(2) — 2NO + 2H(2) = N(2) + 2H(2)O — 2NO(2) + 4H(2) = N(2) + 4H(2)O — 2NO + PCO → N(2) + 2CO(2) — 2NO(2) + 4CO → N(2) + 4CO(2)—
Очистка от оксида углерода является наиболее рациональной. Процесс гидрирования оксида углерода на никелевых и железных катализаторах проводят при высоких давлениях и повышенных температурах: — CO + 3H(2) = CH(4) + H(2)O — C)(2) + 4H(2) = CH(4) + 2H(2)O — 1/2O(2) + H(2) = H(2)O—
Очистка от диоксида серы – основана на принципе окисления SO(2) и SO(3) контактным методом. Используют метод очистки с получением сульфата аммония, который можно использовать как удобрение. SO(2) окисляют до SO(3) в присутствии V(2)O(5) при 450 –480 гр. Затем при температуре 220-260 гр. Вводят газообразный аммиак. Полученные кристаллы сульфата аммония отделяют в циклонах и электрофильтрах.
Каталитическая очистка газов от органических веществ. В качестве катализаторов используют Cu, Cr, Co, Mn, Ni … в отдельных случаях бокситы, цеолиты. Катализаторы условно делятся на: – цельнометаллические ( металлы платиновой группы или неблагородные металлы, нанесенные на ленты, сетки, спирали из нержавеющей стали) – смешанные ( металлы платиновой группы или оксиды неблагородных металлов, нанесенные на оксид алюминия, нержавеющую сталь ) – керамические ( -=-, нанесенные на керамическую основу в виде сот или решеток) – насыпные ( гранулы или таблетки из оксида алюминия с нанесенными на него металлами платиновой группы или оксидами неблагородных металлов, зерна оксидов небл. Мет.) Преимуществом обладают катализатор, нанесенные на мет носители. Они более термостабильны, прочны, с легкой регенерацией.
Очистка газов от серо-органических соединений заключается в их окислении при повышенных температурах. Каталитическое окисление производят кислородом, образованием кислородных соединений серы. В качестве катализаторов процессов гидрирования серо-органических соединений водородом используют контактные массы на основе оксидов Fe, Co, Ni, Cu, Zn. При гидрировании водяным паром используют катализаторы, содержащие в качестве компонента оксид железа.
Задача. Концентрация растворимого соединения А в сточной воде составляет СА. Во сколько раз необходимо разбавить эту воду, чтобы можно было сливать ее в канализацию, если известна ПДК соединения А?
Снд=0,0005 моль/л m=νM
ПДКнд=0,0005мг/л mнд=0,0005*200=0,1 г
СNO3-=0.01 моль/л m=νM
ПДКNO3-=45мг/л mNO3-=0,01*62=0,62 г
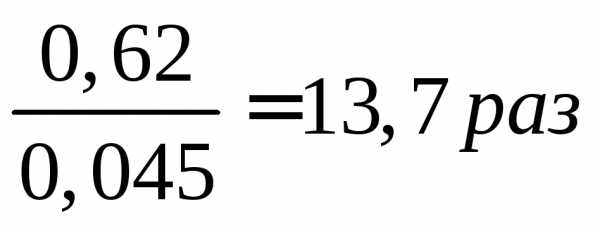
СNO2-=0,5 моль/л m=νM
ПДКNO2-=3,3мг/л mNO3-=0,5*46=23 г
Задача. В воздухе обнаружено присутствие примесей А, В, С в концентрациях СА, СВ, СС. Соотв. ли установленным нормативам качество воздуха, если ПДК этих веществ равны соотв. ПДКА, ПДКВ, ПДКС? При ответе учесть эффект суммации.
находится по формуле:
если ≤1, то соответствует, если неравенство не выполняется, значит концентрация в воздухе вредных примесей превышает нормам.
Задача. Жесткость некоторого образца воды обусловливается только дикарбонатом магния. При кипячении 0,5 л воды в осадок выпало 14 мг Mg(OH)2. Чему равна жесткость воды?
Решение 1.
, или
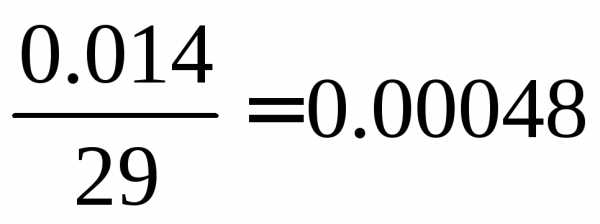 эквивалентной
массы, или
эквивалентной
массы, или
0,48 мэкв Mg(OH)2
В 0,5 л воды содержится 0,48 мэкв Mg(OH)2,
жесткость
воды равна 
Решение 2.
В 1 л воды содержится 0,014/0,5 = 0,028 г Mg(OH)2,
что составляет 0,028/0,029=0,00096 г-экв или 0,96 мг-экв (29 – эквивалент Mg(OH)2)
Следовательно, жесткость воды 0,96 мг-экв
Задача. Чему равна жесткость (в ммоль/л) 0,003 М раствора MgCl2?
0,003 М MgCl2
0,003 М = 0,003 моль/л = 3ммоль/л
Задача. На титрование 0,5 л образца воды израсходовано 22,8 мл 0,1 н НС1. Чему равна карбонатная жесткость воды?
VH2O=0.5 л 0,1н HCl
VHCl=22,8 мл
Задача. Сколько л 20 % соляной кислоты, плотностью 1,098 г/см3, потребуется для нейтрализации 700л 5 М щелочной сточной воды?
1 л раствора имеет массу 1098 г и содержит 1098*0,20=219,60 г HCl, что составляет
C1V1 = C2V2
700л*5М=Хл*6М
Задача. Рассчитайте минимальный объем (в литрах) 15 % раствора соды (плотность 1,158 г/мл), необходимый для устранения жесткости 100 л природной воды с содержанием гидрокарбонат-ионов, равным 0,61 г/л.
1 л раствора имеет массу 1158 г и содержит 1158*0,15=173,7 г Na2CO3
C1V1 = C2V2
100*0,61=Х*173,7
Задача. Диоксид углерода поглощают раствором гидроксида кальция. Вначале образуется осадок, затем он исчезает. Определите общий объем газа (в литрах, н.у.), израсходованный при образовании 74 г осадка.
Задача. Смесь бромидов натрия и калия применяют в медицине как успокоительное средство. Найдите число бромид-ионов, поступивших в организм после приема 10 мл раствора, содержащего по 30 г бромида натрия и бромида калия в 1 л.
ν=30/103=0,29 моль NaBr
ν=30/119=0,25 моль KBr
[Br]–общ=0,29+0,25=0,54 моль/л
0,54 моль – 1000 мл
Х – 10 мл
число Br–=5.4*10-3=32.5*1020
Задача. Газовая смесь содержит СО2, СО, О2 и N2. При анализе 100 мл смеси методом химического поглощения получены следующие результаты.
Компонент | Количество газа после поглощения, мл |
СО2 | 83,20 |
О2 | 82.40 |
СО | 75.60 |
N2 | 75,60 |
Определите количественный состав смеси (объемный %), если происходит последовательное поглощение газов из смеси, a N2 не поглощается.
VCO2=83,20 мл
VО2=82,40 мл
VСО=75,60 мл
VN2=75,60 мл
Vобщ=83,20+82,40+75,60+75,60=316,80 мл

100-(26,3+26+23,9)=23,8% N2
81
studfiles.net
58. Суть адсорбционных методов очистки газов. Типы адсорбентов.
Адсорбционные методы очистки основаны на поглощении примесей твердыми телами с развитой поверхностью, адсорбентами. Поглощаемые молекулы удерживаются на поверхности твердых тел силами
Ван-дер-Ваальса(физическая адсорбция) или химическими силами( хемосорбция). Стадии адсорбции: – перенос молекул газа к внешней поверхности твердого тела – проникновение молекул газа в поры твердого тела – собственно адсорбция. Адсорбция рекомендуется для очистки газов с невысокой концентрацией вредных компонентов. Адсорбированные вещества удаляют из адсорбентов с помощью десорбции инертным газом или паром. Преимущество: высокая степень очистки. Недостатки: “чистые” (сухие и без пыли) газы, небольшая скорость. Адсорбенты – материалы высокоразвитой внутренней поверхностью(природные и синтетические) : активированные угли, силикагели, алюмогели, цеолиты, иониты. Активированные угли – гидрофобны. Для адсорбции газов и паров используют микропористые гранулированные активированные угли. Силикагели – гидратированные аморфные кремнеземы (SiO(2)nH(2)O), являющиеся реакционно-способными соединениями переменного состава, превращения которых идет по механизму полконденсации. Зазоры м/у частицами образуют пористую структуру селикагеля. Получают путем осаждения аморфного кремнезема из силикатно-щелочных металлов. Служат для поглощения полярных веществ. Алюмогели ( Al(2)O(3)*nH(2)O где 0< n < 6) – получают прокаливанием различных гидроксидов алюминия. Используют для улавливания полярных органических соединений и осушки газов. Цеолиты – алюмосиликаты, содержащие в своем составе оксиды щелочных и щелочноземельных металлов. Характеризуются регулярной структурой пор, соизмеримых с размерами молекул. Общая химическая формула: Me(2/n)C*Al(2)O(3)*xSi(2)*yH(2)O, где Me катион металла, n – его валентность. Получают синтетически и добывают при разработки месторождений. Обладают наибольшей адсорбцией по парам полярных соединений и веществ с кратными связями в молекулах. Иониты – высокомолекулярные соединения с развитой поверхностью.
59. Каталитические методы.
связанны с химическим превращением токсичных компонентов в нетоксичные в присутствии катализаторов. Аппараты – реакторы различной конструкции. Используются для очистки от: оксидов азота, серы, углерода и от органических примесей.
Оксид азота восстанавливается газом – восстановителем(CO,CH(4)…) в присутствии катализаторов. В качестве катализаторов используют различные металлы, которыми покрывают огнеупорные материалы (носители). Часто применяют палладиевый катализатор, нанесенный на оксид алюминия. Температура 400 470 гр. Реакции: — 4NO + CH(4) = CO(2) + 2H(2)O + 2N(2) — 2NO(2) + CH(4) = CO(2) + 2H(2)O + N(2) — 2NO + 2H(2) = N(2) + 2H(2)O — 2NO(2) + 4H(2) = N(2) + 4H(2)O — 2NO + PCO → N(2) + 2CO(2) — 2NO(2) + 4CO → N(2) + 4CO(2)—
Очистка от оксида углерода является наиболее рациональной. Процесс гидрирования оксида углерода на никелевых и железных катализаторах проводят при высоких давлениях и повышенных температурах: — CO + 3H(2) = CH(4) + H(2)O — C)(2) + 4H(2) = CH(4) + 2H(2)O — 1/2O(2) + H(2) = H(2)O—
Очистка от диоксида серы – основана на принципе окисления SO(2) и SO(3) контактным методом. Используют метод очистки с получением сульфата аммония, который можно использовать как удобрение. SO(2) окисляют до SO(3) в присутствии V(2)O(5) при 450 –480 гр. Затем при температуре 220-260 гр. Вводят газообразный аммиак. Полученные кристаллы сульфата аммония отделяют в циклонах и электрофильтрах.
Каталитическая очистка газов от органических веществ. В качестве катализаторов используют Cu, Cr, Co, Mn, Ni … в отдельных случаях бокситы, цеолиты. Катализаторы условно делятся на: – цельнометаллические ( металлы платиновой группы или неблагородные металлы, нанесенные на ленты, сетки, спирали из нержавеющей стали) – смешанные ( металлы платиновой группы или оксиды неблагородных металлов, нанесенные на оксид алюминия, нержавеющую сталь ) – керамические ( -=-, нанесенные на керамическую основу в виде сот или решеток) – насыпные ( гранулы или таблетки из оксида алюминия с нанесенными на него металлами платиновой группы или оксидами неблагородных металлов, зерна оксидов небл. Мет.) Преимуществом обладают катализатор, нанесенные на мет носители. Они более термостабильны, прочны, с легкой регенерацией.
Очистка газов от серо-органических соединений заключается в их окислении при повышенных температурах. Каталитическое окисление производят кислородом, образованием кислородных соединений серы. В качестве катализаторов процессов гидрирования серо-органических соединений водородом используют контактные массы на основе оксидов Fe, Co, Ni, Cu, Zn. При гидрировании водяным паром используют катализаторы, содержащие в качестве компонента оксид железа.
Задача. Концентрация растворимого соединения А в сточной воде составляет СА. Во сколько раз необходимо разбавить эту воду, чтобы можно было сливать ее в канализацию, если известна ПДК соединения А?
Снд=0,0005 моль/л m=νM
ПДКнд=0,0005мг/л mнд=0,0005*200=0,1 г
СNO3-=0.01 моль/л m=νM
ПДКNO3-=45мг/л mNO3-=0,01*62=0,62 г
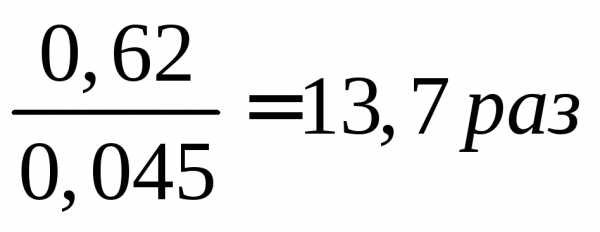
СNO2-=0,5 моль/л m=νM
ПДКNO2-=3,3мг/л mNO3-=0,5*46=23 г
Задача. В воздухе обнаружено присутствие примесей А, В, С в концентрациях СА, СВ, СС. Соотв. ли установленным нормативам качество воздуха, если ПДК этих веществ равны соотв. ПДКА, ПДКВ, ПДКС? При ответе учесть эффект суммации.
находится по формуле:
если ≤1, то соответствует, если неравенство не выполняется, значит концентрация в воздухе вредных примесей превышает нормам.
Задача. Жесткость некоторого образца воды обусловливается только дикарбонатом магния. При кипячении 0,5 л воды в осадок выпало 14 мг Mg(OH)2. Чему равна жесткость воды?
Решение 1.
, или
 эквивалентной
массы, или
эквивалентной
массы, или
0,48 мэкв Mg(OH)2
В 0,5 л воды содержится 0,48 мэкв Mg(OH)2,
жесткость воды равна
Решение 2.
В 1 л воды содержится 0,014/0,5 = 0,028 г Mg(OH)2,
что составляет 0,028/0,029=0,00096 г-экв или 0,96 мг-экв (29 – эквивалент Mg(OH)2)
Следовательно, жесткость воды 0,96 мг-экв
Задача. Чему равна жесткость (в ммоль/л) 0,003 М раствора MgCl2?
0,003 М MgCl2
0,003 М = 0,003 моль/л = 3ммоль/л
Задача. На титрование 0,5 л образца воды израсходовано 22,8 мл 0,1 н НС1. Чему равна карбонатная жесткость воды?
VH2O=0.5 л 0,1н HCl
VHCl=22,8 мл
Задача. Сколько л 20 % соляной кислоты, плотностью 1,098 г/см3, потребуется для нейтрализации 700л 5 М щелочной сточной воды?
1 л раствора имеет массу 1098 г и содержит 1098*0,20=219,60 г HCl, что составляет
C1V1 = C2V2
700л*5М=Хл*6М
Задача. Рассчитайте минимальный объем (в литрах) 15 % раствора соды (плотность 1,158 г/мл), необходимый для устранения жесткости 100 л природной воды с содержанием гидрокарбонат-ионов, равным 0,61 г/л.
1 л раствора имеет массу 1158 г и содержит 1158*0,15=173,7 г Na2CO3
C1V1 = C2V2
100*0,61=Х*173,7
Задача. Диоксид углерода поглощают раствором гидроксида кальция. Вначале образуется осадок, затем он исчезает. Определите общий объем газа (в литрах, н.у.), израсходованный при образовании 74 г осадка.
Задача. Смесь бромидов натрия и калия применяют в медицине как успокоительное средство. Найдите число бромид-ионов, поступивших в организм после приема 10 мл раствора, содержащего по 30 г бромида натрия и бромида калия в 1 л.
ν=30/103=0,29 моль NaBr
ν=30/119=0,25 моль KBr
[Br]–общ=0,29+0,25=0,54 моль/л
0,54 моль – 1000 мл
Х – 10 мл
число Br–=5.4*10-3=32.5*1020
Задача. Газовая смесь содержит СО2, СО, О2 и N2. При анализе 100 мл смеси методом химического поглощения получены следующие результаты.
Компонент | Количество газа после поглощения, мл |
СО2 | 83,20 |
О2 | 82.40 |
СО | 75.60 |
N2 | 75,60 |
Определите количественный состав смеси (объемный %), если происходит последовательное поглощение газов из смеси, a N2 не поглощается.
VCO2=83,20 мл
VО2=82,40 мл
VСО=75,60 мл
VN2=75,60 мл
Vобщ=83,20+82,40+75,60+75,60=316,80 мл
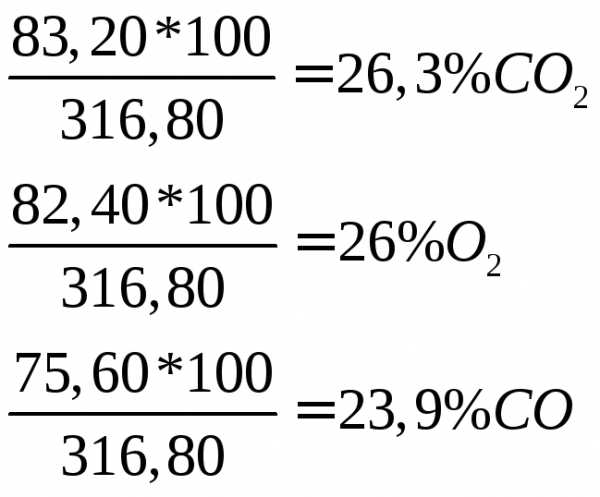
100-(26,3+26+23,9)=23,8% N2
81
studfiles.net
Задача № 1. «Определение суммарного уровня загрязнения воздушной среды»
Для того чтобы снизить отрицательное воздействие загрязняющих веществ на биосферу, в целом, и на атмосферу в частности, применяют принципы нормирования. Принцип раздельного нормирования заключается в том, что для каждого вредного вещества устанавливается несколько максимально разовых концентраций ПДК в воздушной среде. Это ПДК в воздухе рабочей зоны (ПДК р.з.) и ПДК атмосферного воздуха (ПДК а.в.).
Суммация действия вредных веществ в расчетах рассеивания.
Чаще всего в воздухе присутствует ни одно вещество, а сразу несколько. При одновременном присутствии в атмосфере нескольких n вредных веществ, обладающих суммацией действия, безразмерная суммарная концентрация (для каждой группы вредных веществ однонаправленного действия) не должна превышать единицы при расчете по формуле:
(1)
где С1, С2, Сn – концентрации вредных веществ, однонаправленного действия в атмосферном воздухе, мг/ м3.
ПДК1, ПДК2, ПДКn, – это соответствующие ПДК этих веществ в атмосферном воздухе, мг/ м3.
К вредным веществам однонаправленного действия относятся вещества близкие по химическому строения и характеру биологического воздействия на организм человека, например:
– Ацетон – фенол;
– ацетон – фурфурол – формальдегид – фенол;
– озон – диоксид азота – формальдегид;
– оксид углерода – диоксид азота – формальдегид – гексан;
– диоксид серы – оксид углерода – диоксид азота – фенол;
– диоксид серы – аэрозоль серной кислоты
– диоксид серы – триоксид серы – аммиак – окислы азота;
– сильные минеральные кислоты (серная, соляная, азотная).
А так же
– ацетон, акролеин, фталевый ангидрид;
– ацетон и фенол;
– ацетон и ацетофенол;
– ацетон, фурфурол, формальдегид, фенол;
– ацетальдегид и винилацетат;
– аэрозоли пентоксид ванадия и окисей марганца;
– аэрозоли пентоксид ванадия и сернистый ангидрид;
– аэрозоли пентоксид ванадия и триокиси хрома;
– бензол и ацетофенон;
– вольфрамовый и серистый ангидрид;
– гексахлоран и фазолон;
– изобутенилкарбинол, диметилвинилкаринол;
– метилгидропиран и метилентетрагидропирен;
– озон, двуокись азота и формальдегид;
– окись углерода, двуокись азота, формальдегид, гексан;
– сернистый ангидрид и аэрозоль серной кислоты;
– сернистый ангидрид и никель металлический;
– сернистый ангидрид и сероводород;
– сернистый ангидрид и двуокись азота;
– сернистый ангидрид, окись углерода, этил конверторного производства;
– сернистый ангидрид и фенол;
– сернистый ангидрид и фтористый водород;
– серный и сернистый ангидрид, аммиак и окиси азота;
– фенол и ацетофенон;
– фурфурол, метиловый и этиловый спирты;
– циклогексан и бензол;
– этилен, пропилен, бутилен, амилен.
Степень загрязнения окружающей среды принято оценивать по кратности превышения ПДК и лимита на выбросы, назначаемые определенному объекту, классу опасности веществ, количеству химических элементов и соединений. В случае одновременного присутствия нескольких загрязняющих веществ используются суммарные показатели.
Сs – суммарный показатель загрязнения воздуха может быть определен по следующей формуле:
(2)
где: – Сi – концентрация вредных веществ, обладающих однонаправленным действием, мг/ м3;
– ПДКi – соответствующий ПДК этих веществ, мг/ м3 .
Уровень загрязнения воздуха по определенному веществу Сnрассчитывается по формуле:
(3)
Пример № 1. В воздухе промышленной площадки химического завода одновременно присутствую фенол, ацетон, сероводород, формальдегид в следующих концентрациях: 0,08, 50, 5, 0,14 мг/ м3. Рассчитать уровень загрязнения воздуха промышленной площадки учитывая эффект суммации и сделать вывод о состоянии атмосферного воздуха.
РЕШЕНИЕ.
Находим ПДК р.з. указанных веществ по справочнику (таблица 1), затем рассчитываем ПДКп.п. исходя из того, что ПДК п.п. = 0,3 ПДК р.з.
ПДК р.з. (фенол) = 0,3 ПДК п.п. = 0,3 0,3 = 0,09 мг/м3 .
ПДК р.з. (ацетон) = 200 ПДК п.п. = 200 0,3 = 60 мг/м3 м3 .
ПДК р.з. (сероводород) = 10 ПДК п.п. = 10 0,3 = 3 мг/ м3 .
ПДК р.з. (формальдегид) = 0,5 ПДК п.п. = 0,5 0,3 = 0,15 мг/ м3 .
Из указанных веществ выбираем только вещества однонаправленного действия по утвержденным спискам. В нашей задаче вещества из группы – фенол – ацетон – формальдегид;
Далее рассчитываем суммарный уровень загрязнения воздушной среды
Исходя из расчетов, получаем, что суммарный уровень загрязнения воздуха превышает единицу, т.е. воздух не соответствует санитарно-гигиеническим требованиям.
Проверяем уровень загрязнения воздуха по сероводороду, не вошедшему в список веществ однонаправленного действия:
ПДКр.з.(сероводород)=10 ПДКп.п.= 100,3= 3 мг/ м3 .
Уровень загрязнения воздуха по сероводороду превышает единицу, воздух не соответствует санитарно-гигиеническим требованиям.
Исходя из этих расчетов, можно сделать однозначный вывод, что атмосферный воздух данной промышленной площадки не соответствует санитарно-гигиеническим требованиям.
studfiles.net
Задача № 1. «Определение суммарного уровня загрязнения воздушной среды»
Для того чтобы снизить отрицательное воздействие загязняющих веществ на биосферу в общем, и на атмосферу в частности, применяют принципы нормирования. Принцип раздельного нормирования заключается в том, что для каждого вредного вещества устанавливается несколько максимально разовых концентраций ПДК в воздушной среде. Это ПДК в воздухе рабочей зоны (ПДК р.з.) и ПДК атмосферного воздуха (ПДК а.в.).
Суммация действия вредных веществ в расчетах рассеивания.
Чаще всего в воздухе присутствует ни одно вещество, а сразу несколько. При одновременном присутствии в атмосфере нескольких n вредных веществ, обладающих суммацией действия, безразмерная суммарная концентрация (для каждой группы вредных веществ однонаправленного действия) не должна превышать единицы при расчете по формуле:
где С1, С2, Сn – концентрации вредных веществ, однонаправленного действия в атмосферном воздухе, мг/ м3.
ПДК1, ПДК2, ПДКn, – это соответствующие ПДК этих веществ в атмосферном воздухе, мг/ м3.
К вредным веществам однонаправленного действия относятся вещества близкие по химическому строения и характеру биологического воздействия на организм человека, например:
– Ацетон – фенол;
– ацетон – фурфурол – формальдегид – фенол;
– озон – диоксид азота – формальдегид;
– оксид углерода – диоксид азота – формальдегид – гексан;
– диоксид серы – оксид углерода – диоксид азота – фенол;
– диоксид серы – аэрозоль серной кислоты
– диоксид серы – триоксид серы – аммиак – окислы азота;
– сильные минеральные кислоты (серная, соляная, азотная).
А так же
– ацетон, акролеин, фталевый ангидрид;
– ацетон и фенол;
– ацетон и ацетофенол;
– ацетон, фурфурол, формальдегид, фенол;
– ацетальдегид и винилацетат;
– аэрозоли пентоксид ванадия и окисей марганца;
– аэрозоли пентоксид ванадия и сернистый ангидрид;
– аэрозоли пентоксид ванадия и триокиси хрома;
– бензол и ацетофенон;
– вольфрамовый и серистый ангидрид;
– гексахлоран и фазолон;
– изобутенилкарбинол, диметилвинилкаринол;
– метилгидропиран и метилентетрагидропирен;
– озон, двуокись азота и формальдегид;
– окись углерода, двуокись азота, формальдегид, гексан;
– сернистый ангидрид и аэрозоль серной кислоты;
– сернистый ангидрид и никель металлический;
– сернистый ангидрид и сероводород;
– сернистый ангидрид и двуокись азота;
– сернистый ангидрид, окись углерода, этил конверторного производства;
– сернистый ангидрид и фенол;
– сернистый ангидрид и фтористый водород;
– серный и сернистый ангидрид, аммиак и окиси азота;
– фенол и ацетофенон;
– фурфурол, метиловый и этиловый спирты;
– циклогексан и бензол;
– этилен, пропилен, бутилен, амилен.
Степень загрязнения окружающей среды принято оценивать по кратности превышения ПДК и лимита на выбросы, назначаемые определенному объекту, классу опасности веществ, количеству химических элементов и соединений. В случае одновременного присутствия нескольких загрязняющих веществ используются суммарные показатели.
Сs – суммарный показатель загрязнения воздуха может быть определен по следующей формуле:
где: – Сi – концентрация вредных веществ, обладающих однонаправленным действием, мг/ м3;
– ПДКi – соответствующий ПДК этих веществ, мг/ м3 .
Уровень загрязнения воздуха по определенному веществу Сn рассчитывается по формуле:
Пример № 1. В воздухе промышленной площадки химического завода одновременно присутствую фенол, ацетон, сероводород, формальдегид в следующих концентрациях: 0,08, 50, 5, 0,14 мг/ м3. Рассчитать уровень загрязнения воздуха промышленной площадки учитывая эффект суммации и сделать вывод о состоянии атмосферного воздуха.
РЕШЕНИЕ.
Находим ПДК р.з. указанных веществ по справочнику (таблица 1), затем рассчитываем ПДКп.п. исходя из того, что ПДК п.п. = 0,3 ПДК р.з.
ПДК р.з. (фенол) = 0,3 ПДК п.п. = 0,3 ×0,3 = 0,09 мг/м3 .
ПДК р.з. (ацетон) = 200 ПДК п.п. = 200 ×0,3 = 60 мг/м3 м3 .
ПДК р.з. (сероводород) = 10 ПДК п.п. = 10 ×0,3 = 3 мг/ м3 .
ПДК р.з. (формальдегид) = 0,5 ПДК п.п. = 0,5 ×0,3 = 0,15 мг/ м3 .
Из указанных веществ выбираем только вещества однонаправленного действия по утвержденным спискам. В нашей задаче вещества из группы – фенол – ацетон – формальдегид;
Далее рассчитываем суммарный уровень загрязнения воздушной среды
Исходя из расчетов, получаем, что суммарный уровень загрязнения воздуха превышает единицу, т.е. воздух не соответствует санитарно-гигиеническим требованиям.
Проверяем уровень загрязнения воздуха по сероводороду, не вошедшему в список веществ однонаправленного действия:
ПДКр.з.(сероводород)=10 ПДКп.п.= 10×0,3= 3 мг/ м3 .
Уровень загрязнения воздуха по сероводороду превышает единицу, воздух не соответствует санитарно-гигиеническим требованиям.
Исходя из этих расчетов, можно сделать однозначный вывод, что атмосферный воздух данной промышленной площадки не соответствует санитарно-гигиеническим требованиям.
Варианты заданий №1.
1. В атмосферном воздухе г. Донецк одновременно обнаружены следующие загрязняющие примеси:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,006 мг/ м3.
Фенол – 0,007 мг/ м3.
Формальдегид – 0,018 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха и сделать вывод о состоянии атмосферного воздуха.
2. В воздухе промышленной площадки химического завода одновременно присутствуют следующие вещества:
Оксид углерода – 3,2 мг/ м3.
Сероводород – 4 мг/ м3.
Фенол – 0,008 мг/ м3.
Диоксид серы – 1,2 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух промышленной площадки санитарно-гигиеническим требованиям?
3. В атмосферном воздухе Г. Донецк одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,018 мг/ м3.
Диоксид серы 0,014 мг/м3.
Аммиак – 0,10 мг/м3.
Оксид азота – 0,30 мг/ м3.
Рассчитать суммарный уровень загрязнения г. Донецк. Соответствует ли воздух г. Донецк санитарно-гигиеническим требованиям?
4. В воздухе рабочей зоны химического цеха по производству азотной кислоты обнаружены следующие примеси:
Диоксид серы – 5 мг/ м3
Диоксид азота – 1 мг/ м3.
Ацетон – 100 мг/ м3.
Диоксид углерода – 20 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха рабочей зоны и сделать вывод о состоянии атмосферного воздуха.
5. В воздухе промышленной площадки химического завода одновременно присутствуют следующие вещества в концентрациях:
Оксид углерода – 4,6 мг/ м3.
Сероводород – 3 мг/ м3.
Фенол – 0,005 мг/ м3
Диоксид серы 1,5 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
6. В атмосферном воздухе г. Ялта обнаружены следующие загрязняющие вещества в концентрациях:
Оксид углерода – 2 мг/ м3.
Озон – 0,12 мг/ м3.
Диоксид азота – 0,05 мг/ м3.
Аммиак – 0,1 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух г. Ялта санитарно-гигиеническим требованиям?
7. В атмосферном воздухе г. Донецк одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,005 мг/ м3
Фенол – 0,003 мг/ м3.
Формальдегид – 0,02 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха, соответствует ли воздух г. Донецк санитарно-гигиеническим требованиям?
8. В воздухе рабочей зоны химического цеха обнаружены загрязняющие вещества аммиак, ацетон, формальдегид, фенол в следующих концентрациях: 25; 100; 0,8; 0,2 мг/м3. Рассчитать уровень загрязнения воздуха химического цеха и сделать вывод о состоянии атмосферного воздуха данного цеха.
9. В воздухе промышленной площадки химического цеха обнаружены пары следующих кислот – серной; соляной и азотной в концентрациях 0,5; 1,2; 0,8 мг/ м3. Рассчитать уровень загрязнения воздуха промышленной площадки и сделать вывод о состоянии атмосферного воздуха.
10. В атмосферном воздухе небольшого промышленного города обнаружены следующие загрязняющие вещества диоксид азота, диоксид серы, оксид углерода и гидроксид кальция в концентрациях 0,05; 0,4; 3,0; 0,5 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
11. В атмосферном воздухе г. Ялта обнаружены следующие загрязняющие вещества: диоксид серы, триоксид серы, окислы азота, ацетон в следующих концентрациях: 0,014; 0,3; 0,43; 0,14 мг/ м3.Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
12. В атмосферном воздухе небольшого города постоянно в течение года были обнаружены следующие вещества диоксид азота, оксид углерода, анилин, диоксид серы в следующих концентрациях: 0,03; 0,5; 0,02; 0,04 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
13. В атмосферном воздухе небольшого города постоянно в течение года были обнаружены следующие вещества диоксид азота, озон, сероводород в концентрациях: 0,03; 0,02; 0,08 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
14. В атмосферном воздухе г. Энергодар одновременно обнаружены следующие загрязняющие примеси:
Ацетон – 0,64 мг/ м3.
Формальдегид – 0,018 мг/ м3.
Сероводород – 0,056 мг/ м3.
Фенол – 0,037 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха и сделать вывод о состоянии атмосферного воздуха.
15. В воздухе промышленной площадки химического завода одновременно присутствуют следующие вещества:
Оксид углерода – 3,8 мг/ м3.
Сероводород – 4,8 мг/ м3.
Фенол – 0,0054мг/ м3.
Диоксид серы – 1,56 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух промышленной площадки санитарно-гигиеническим требованиям?
16. В воздухе рабочей зоны химического цеха литейного завода обнаружены загрязняющие вещества аммиак, ацетон, формальдегид, фенол в следующих концентрациях: 55; 140; 0,83; 0,12 мг/м3. Рассчитать уровень загрязнения воздуха химического цеха и сделать вывод о состоянии атмосферного воздуха данного цеха.
17. В воздухе промышленной площадки химического цеха обнаружены пары следующих кислот – серной; соляной и азотной в концентрациях 0,5; 1,2; 0,8 мг/ м3. Рассчитать уровень загрязнения воздуха промышленной площадки и сделать вывод о состоянии атмосферного воздуха.
18. В атмосферном воздухе небольшого промышленного города обнаружены следующие загрязняющие вещества диоксид азота, диоксид серы, оксид углерода и гидроксид кальция в концентрациях 0,95; 0,44; 3,6; 4,5 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
19. В атмосферном воздухе г. Ялта обнаружены следующие загрязняющие вещества: диоксид серы, триоксид серы, окислы азота, ацетон в следующих концентрациях: 0,014; 0,3; 0,43; 0,14 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздух.
20. В атмосферном воздухе г. Нетешин одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,018 мг/ м3.
Диоксид серы 0,014 мг/м3.
Аммиак – 0,10 мг/м3.
Оксид азота – 0,30 мг/ м3.
Рассчитать суммарный уровень загрязнения г. Нетешин. Соответствует ли воздух г. Нетешин санитарно-гигиеническим требованиям?
21. В воздухе промышленной площадки химического цеха по производству азотной кислоты обнаружены следующие примеси:
Диоксид серы – 5,6 мг/ м3
Диоксид азота – 4,8 мг/ м3.
Ацетон – 158 мг/ м3.
Диоксид углерода – 20 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха промышленной площадки и сделать вывод о состоянии атмосферного воздуха.
- В воздухе промышленной площадки химического завода по производству удобрений одновременно присутствуют следующие вещества в концентрациях:
Оксид углерода – 5,6 мг/ м3.
Сероводород – 7мг/ м3.
Фенол – 0,001 мг/ м3
Диоксид серы 1,8 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
- В атмосферном воздухе г. Ровно обнаружены следующие загрязняющие вещества в концентрациях:
Оксид углерода – 2,9 мг/ м3.
Озон – 4,12 мг/ м3.
Диоксид азота – 1,05 мг/ м3.
Аммиак – 0,08 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух г. Ровно санитарно-гигиеническим требованиям?
- В атмосферном воздухе г. Кузнецовск одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,005 мг/ м3
Фенол – 0,003 мг/ м3.
Формальдегид – 0,02 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха, соответствует ли воздух г. Кузнецовск санитарно-гигиеническим требованиям?
25. В атмосферном воздухе небольшого курортного города постоянно в течение года были обнаружены следующие вещества диоксид азота, оксид углерода, анилин, диоксид серы в следующих концентрациях: 0,03; 0,5; 0,02; 0,04 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
26. В атмосферном воздухе небольшого города постоянно в течение года были обнаружены следующие вещества диоксид азота, озон, сероводород в концентрациях: 0,03; 0,02; 0,08 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
- В атмосферном воздухе г. Нетешин одновременно обнаружены следующие загрязняющие примеси:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,006 мг/ м3.
Фенол – 0,007 мг/ м3.
Формальдегид – 0,018 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха и сделать вывод о состоянии атмосферного воздуха.
- В воздухе промышленной площадки гальванического цеха химического завода одновременно присутствуют следующие вещества:
Оксид углерода – 8,2 мг/ м3.
Сероводород – 5,9 мг/ м3.
Фенол – 0,47 мг/ м3.
Диоксид серы – 8,2 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух промышленной площадки санитарно-гигиеническим требованиям?
- В атмосферном воздухе Г. Киев одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,018 мг/ м3.
Диоксид серы 0,014 мг/м3.
Аммиак – 0,10 мг/м3.
Оксид азота – 0,30 мг/ м3.
Рассчитать суммарный уровень загрязнения г. Киева. Соответствует ли воздух санитарно-гигиеническим требованиям?
30. В воздухе промышленной площадки химического цеха обнаружены пары следующих кислот – серной; соляной и азотной в концентрациях 0,5; 1,2; 0,8 мг/ м3. Рассчитать суммарный уровень. Соответствует ли воздух санитарно-гигиеническим требованиям?
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
zdamsam.ru
Задача1
Задача1Задача1. Газовая смесь содержит СО2, СО, О2 и N2. При анализе 100 мл смеси методом химического поглощения получены следующие результаты.
Определите количественный состав смеси (объемный %), если происходит последовательное поглощение газов из смеси, a N2 не поглощается.
Задача 2. Смесь бромидов натрия и калия применяют в медицине как успокоительное средство. Найдите число бромид-ионов, поступивших в организм после приема 10 мл раствора, содержащего по 30 г бромида натрия и бромида калия в 1 л.
Задача3. Диоксид углерода поглощают раствором гидроксида кальция. Вначале образуется осадок, затем он исчезает. Определите общий объем газа (в литрах, н.у.), израсходованный при образовании 74 г осадка.
Задача4 . Рассчитайте минимальный объем (в литрах) 15 % раствора соды (плотность 1,158 г/мл), необходимый для устранения жесткости 100 л природной воды с содержанием гидрокарбонат-ионов, равным 0,61 г/л.
Задача5 . Сколько л 20 % соляной кислоты, плотностью 1,098 г/см3, потребуется для нейтрализации 700л 5 М щелочной сточной воды?
Задача6. На титрование 0,5 л образца воды израсходовано 22,8 мл 0,1 н НС1. Чему равна карбонатная жесткость воды?
Задача7 . Чему равна жесткость (в ммоль/л) 0,003 М раствора MgCl2?
Задача8. Жесткость некоторого образца воды обусловливается только дикарбонатом магния. При кипячении 0,5 л воды в осадок выпало 14 мг Mg(OH)2. Чему равна жесткость воды?
Задача9. В воздухе обнаружено присутствие примесей А, В, С в концентрациях СА, СВ, СС. Соотв. ли установленным нормативам качество воздуха, если ПДК этих веществ равны соотв. ПДКА, ПДКВ, ПДКС? При ответе учесть эффект суммации.
Задача10. Концентрация растворимого соединения А в сточной воде составляет СА. Во сколько раз необходимо разбавить эту воду, чтобы можно было сливать ее в канализацию, если известна ПДК соединения А? (несколько вариантов данных)
filepo27.narod.ru
Варианты заданий №1.
В атмосферном воздухе г. Донецк одновременно обнаружены следующие загрязняющие примеси:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,006 мг/ м3.
Фенол – 0,007 мг/ м3.
Формальдегид – 0,018 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха и сделать вывод о состоянии атмосферного воздуха.
В воздухе промышленной площадки химического завода одновременно присутствуют следующие вещества:
Оксид углерода – 3,2 мг/ м3.
Сероводород – 4 мг/ м3.
Фенол – 0,008 мг/ м3.
Диоксид серы – 1,2 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух промышленной площадки санитарно-гигиеническим требованиям?
В атмосферном воздухе Г. Донецк одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,018 мг/ м3.
Диоксид серы 0,014 мг/м3.
Аммиак – 0,10 мг/м3.
Оксид азота – 0,30 мг/ м3.
Рассчитать суммарный уровень загрязнения г. Донецк. Соответствует ли воздух г. Донецк санитарно-гигиеническим требованиям?
В воздухе рабочей зоны химического цеха по производству азотной кислоты обнаружены следующие примеси:
Диоксид серы – 5 мг/ м3
Диоксид азота – 1 мг/ м3.
Ацетон – 100 мг/ м3.
Диоксид углерода – 20 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха рабочей зоны и сделать вывод о состоянии атмосферного воздуха.
В воздухе промышленной площадки химического завода одновременно присутствуют следующие вещества в концентрациях:
Оксид углерода – 4,6 мг/ м3.
Сероводород – 3 мг/ м3.
Фенол – 0,005 мг/ м3
Диоксид серы 1,5 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе г. Ялта обнаружены следующие загрязняющие вещества в концентрациях:
Оксид углерода – 2 мг/ м3.
Озон – 0,12 мг/ м3.
Диоксид азота – 0,05 мг/ м3.
Аммиак – 0,1 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух г. Ялта санитарно-гигиеническим требованиям?
В атмосферном воздухе г. Донецк одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,005 мг/ м3
Фенол – 0,003 мг/ м3.
Формальдегид – 0,02 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха, соответствует ли воздух г. Донецк санитарно-гигиеническим требованиям?
В воздухе рабочей зоны химического цеха обнаружены загрязняющие вещества аммиак, ацетон, формальдегид, фенол в следующих концентрациях: 25; 100; 0,8; 0,2 мг/м3. Рассчитать уровень загрязнения воздуха химического цеха и сделать вывод о состоянии атмосферного воздуха данного цеха.
В воздухе промышленной площадки химического цеха обнаружены пары следующих кислот – серной; соляной и азотной в концентрациях 0,5; 1,2; 0,8 мг/ м3. Рассчитать уровень загрязнения воздуха промышленной площадки и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе небольшого промышленного города обнаружены следующие загрязняющие вещества диоксид азота, диоксид серы, оксид углерода и гидроксид кальция в концентрациях 0,05; 0,4; 3,0; 0,5 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе г. Ялта обнаружены следующие загрязняющие вещества: диоксид серы, триоксид серы, окислы азота, ацетон в следующих концентрациях: 0,014; 0,3; 0,43; 0,14 мг/ м3.Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе небольшого города постоянно в течение года были обнаружены следующие вещества диоксид азота, оксид углерода, анилин, диоксид серы в следующих концентрациях: 0,03; 0,5; 0,02; 0,04 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе небольшого города постоянно в течение года были обнаружены следующие вещества диоксид азота, озон, сероводород в концентрациях: 0,03; 0,02; 0,08 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе г. Энергодар одновременно обнаружены следующие загрязняющие примеси:
Ацетон – 0,64 мг/ м3.
Формальдегид – 0,018 мг/ м3.
Сероводород – 0,056 мг/ м3.
Фенол – 0,037 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха и сделать вывод о состоянии атмосферного воздуха.
В воздухе промышленной площадки химического завода одновременно присутствуют следующие вещества:
Оксид углерода – 3,8 мг/ м3.
Сероводород – 4,8 мг/ м3.
Фенол – 0,0054мг/ м3.
Диоксид серы – 1,56 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух промышленной площадки санитарно-гигиеническим требованиям?
В воздухе рабочей зоны химического цеха литейного завода обнаружены загрязняющие вещества аммиак, ацетон, формальдегид, фенол в следующих концентрациях: 55; 140; 0,83; 0,12 мг/м3. Рассчитать уровень загрязнения воздуха химического цеха и сделать вывод о состоянии атмосферного воздуха данного цеха.
В воздухе промышленной площадки химического цеха обнаружены пары следующих кислот – серной; соляной и азотной в концентрациях 0,5; 1,2; 0,8 мг/ м3. Рассчитать уровень загрязнения воздуха промышленной площадки и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе небольшого промышленного города обнаружены следующие загрязняющие вещества диоксид азота, диоксид серы, оксид углерода и гидроксид кальция в концентрациях 0,95; 0,44; 3,6; 4,5 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе г. Ялта обнаружены следующие загрязняющие вещества: диоксид серы, триоксид серы, окислы азота, ацетон в следующих концентрациях: 0,014; 0,3; 0,43; 0,14 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздух.
В атмосферном воздухе г. Нетешин одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,018 мг/ м3.
Диоксид серы 0,014 мг/м3.
Аммиак – 0,10 мг/м3.
Оксид азота – 0,30 мг/ м3.
Рассчитать суммарный уровень загрязнения г. Нетешин. Соответствует ли воздух г. Нетешин санитарно-гигиеническим требованиям?
В воздухе промышленной площадки химического цеха по производству азотной кислоты обнаружены следующие примеси:
Диоксид серы – 5,6 мг/ м3
Диоксид азота – 4,8 мг/ м3.
Ацетон – 158 мг/ м3.
Диоксид углерода – 20 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха промышленной площадки и сделать вывод о состоянии атмосферного воздуха.
В воздухе промышленной площадки химического завода по производству удобрений одновременно присутствуют следующие вещества в концентрациях:
Оксид углерода – 5,6 мг/ м3.
Сероводород – 7мг/ м3.
Фенол – 0,001 мг/ м3
Диоксид серы 1,8 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе г. Ровно обнаружены следующие загрязняющие вещества в концентрациях:
Оксид углерода – 2,9 мг/ м3.
Озон – 4,12 мг/ м3.
Диоксид азота – 1,05 мг/ м3.
Аммиак – 0,08 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух г. Ровно санитарно-гигиеническим требованиям?
В атмосферном воздухе г. Кузнецовск одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,005 мг/ м3
Фенол – 0,003 мг/ м3.
Формальдегид – 0,02 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха, соответствует ли воздух г. Кузнецовск санитарно-гигиеническим требованиям?
В атмосферном воздухе небольшого курортного города постоянно в течение года были обнаружены следующие вещества диоксид азота, оксид углерода, анилин, диоксид серы в следующих концентрациях: 0,03; 0,5; 0,02; 0,04 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе небольшого города постоянно в течение года были обнаружены следующие вещества диоксид азота, озон, сероводород в концентрациях: 0,03; 0,02; 0,08 мг/ м3. Рассчитать уровень загрязнения воздуха и сделать вывод о состоянии атмосферного воздуха.
В атмосферном воздухе г. Нетешин одновременно обнаружены следующие загрязняющие примеси:
Ацетон – 0,20 мг/ м3.
Сероводород – 0,006 мг/ м3.
Фенол – 0,007 мг/ м3.
Формальдегид – 0,018 мг/ м3.
Рассчитать суммарный уровень загрязнения атмосферного воздуха и сделать вывод о состоянии атмосферного воздуха.
В воздухе промышленной площадки гальванического цеха химического завода одновременно присутствуют следующие вещества:
Оксид углерода – 8,2 мг/ м3.
Сероводород – 5,9 мг/ м3.
Фенол – 0,47 мг/ м3.
Диоксид серы – 8,2 мг/ м3.
Рассчитать суммарный уровень загрязнения воздуха. Соответствует ли воздух промышленной площадки санитарно-гигиеническим требованиям?
В атмосферном воздухе Г. Киев одновременно обнаружены загрязняющие вещества в концентрациях:
Ацетон – 0,018 мг/ м3.
Диоксид серы 0,014 мг/м3.
Аммиак – 0,10 мг/м3.
Оксид азота – 0,30 мг/ м3.
Рассчитать суммарный уровень загрязнения г. Киева. Соответствует ли воздух санитарно-гигиеническим требованиям?
В воздухе промышленной площадки химического цеха обнаружены пары следующих кислот – серной; соляной и азотной в концентрациях 0,5; 1,2; 0,8 мг/ м3. Рассчитать суммарный уровень. Соответствует ли воздух санитарно-гигиеническим требованиям?
studfiles.net