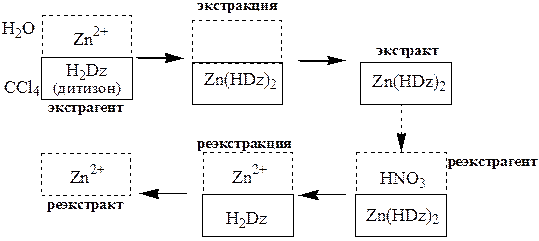9.2. Жидкость – жидкостная экстракция
Жидкость-жидкостная экстракция –метод разделения и концентрирования веществ, основанный на их различном распределении между двумя несмешивающимися жидкими фазами, обычно между водой и несмешивающимся с ней органическим растворителем.
Жидкая
фаза (органический растворитель или
их смесь), в которую переходит
вещество, например, из водной фазы
называется экст- рагентом.Если экстракция обусловлена образованием
новых химических соединений, то
экстрагентом обычно называют реагент,
при взаимодействии с которым образуется
экстрагируемое соединение. Отделённая
органическая фаза, содержащая вещество,
экстрагированное из водной фазы,
называется экстрактом.Процесс обратного извлечения вещества
из экстракта в водную фазу называется реэкс- тракцией.
экстракция
H2O | Zn2+ | |
CCl4 | H2Dz (дитизон) | |
экстрагент | ||
2+ Zn |
Реэкстракт
экстракт
Zn(HDz)2
Zn(HDz)2
Реэкстракция
9.2.1. Количественные характеристики экстракционного равновесия
Экстракционное равновесие описывается с помощью закона распределения Нернста.
При постоянной температуре третий компонент, добавленный к системе, состоящей из двух несмешивающихся или ограниченно смешивающихся жидкостей, распределяется между ними в определённом постоянном для данной температуры соотношении.
I
аз
—— = K – термодинамическая константа экстракции аз
На практике для описания экстракционного равновесия используют:
константа распределения (P0),
коэффициент распределения
степень однократной экстракции (R),
константа экстракции (Kex).
Константа распределения –это отношение равновесной концентрации строго определённой формы вещества в органической фазе к равновесной концентрации этой же формы в водной фазе.
Коэффициент распределения –это отношение общей концентрации всех форм существования экстрагируемого вещества в органической фазе к общей концентрации всех его форм, находящихся в водной фазе.
Например, при экстракции слабой кислоты из водной фазы неполярным органическим растворителем
+
водная фаза
4
HA(B) + h3O ^ A(B) + h4Of
A
HA
(O)
(O)
органическая фаза[HA] [HA]
[A – ]( [A –]
P0 (HA)
P0(A –)
D
[HA]о + [A – ]( [HA] в +[HA]Степень однократной экстракции –доля вещества от его начального количества, экстрагируемая в фазу органического растворителя за одну экстракцию при данных условиях.
n,
n
• 100%
R
•100%N
no +n вЕсли в процессе экстракции протекает химическая реакция, то для характеристики экстракционного равновесия используют константу экстракции. Например
[Zn(HDz)2]o[H+]2 [Zn2+ ]в[h3Dz]2
Kex =
Zn2+ +2H2Dzo ^ Zn(HDz)2o +2H,9.2.2. Экстракционные системы и экстрагенты
Все экстракционные системы можно разделить на 2 группы
В первом типе экстракционных систем разделение происходит в результате разности энергий сольватации и гидратации экстрагирующегося вещества. В органическую фазу переходят вещества, которые плохо гидратируются в водных растворах. Обычно это незаряженные соединения с крупными неполярными молекулами. Наличие гидрофильных групп в молекуле вещества уменьшает его способность экстрагироваться неполярным органическим растворителем, в то время как крупные углеводородные остатки увеличивают эту способность.
В гомологическом ряду с увеличением числа атомов углерода (n) способность вещества экстрагироваться неполярным растворителем повышается, причёмlgP0 линейно зависит отn (рис. 9.1).
гидрофильная группа
гидрофобные углеводородные -—. остатки ^^ ‘fOH
H
OH
Рис. 9.1.Изменение экстрагируемости в гомологическом ряду н-алканолов в системе хлороформ-вода
4 n
увеличение экстрагируемости
В основе реакционной экстракции лежит взаимодействие вещества с экстрагентом с образованием соединения, которое экстрагируется лучше, чем исходное вещество. В зависимости от кислотно- основных свойств экстракционные реагенты обычно разделяют на
studfiles.net
2.5. Жидкостная экстракция
Контрольные вопросы:
1.Что называется абсорбцией? Когда применяется процесс абсорбции?
2.В чем состоит сущность переноса вещества между фазами?
3.Что понимается под движущей силой массообмена абсорбцией?
4.От каких факторов зависит скорость массопередачи?
5.Какими способами осуществляется контакт жидкости и газа?
6.Сущность модели Хигби для определения скорости массопередачи
7.Что называется равновесным соотношением в системе газ – жидкость?
8.Какими параметрами определяется равновесное распределение между двумя фазами (газ-жидкость)?
9.Что называется идеальными системами?
10.Сформулируйте закон Рауля.
11.Сформулируйте закон Дальтона.
12.Дайте характеристику неидеальным системам.
13.Что такое коэффициент активности, и в каких процессах он применяется?
2.5.1.Сущность и основные понятия и определения
Процессы разделения, в которых две взаимно нерастворимые или частично растворимые друг в друге фазы приводятся в контакт для перехода одного или более компонентов из одной фазы в другую, представляют собой экстракцию в системе жидкость-жидкостьили, в более широком смысле слова, – экстракцию избирательными растворителями.
Процессы экстракции являются преимущественно физическими, так как подлежащие переносу из фазы в фазу вещества извлекаются обычно без химических превращений.
Вместе с тем физические равновесные соотношения в значительной мере зависят от химических характеристик растворенных веществ и избирательных растворителей (экстрагентов).
Применение экстрагента, который ближе по своей химической природе к одному из компонентов смеси, приводит к повышению концентрации этого компонента в фазе экстракта.
Экстракция избирательными растворителями проводится различными способами. В простейшем случае к жидкой смеси (исходному раствору) добавляют один экстрагент, что приводит к образованию второй жидкой фазы.
Иногда добавляют два взаимно нерастворимых экстрагента, чтобы компоненты исходного раствора распределялись между двумя жидкими фазами. В водную фазу желательно добавлять соль для повышения активности распределяемого компонента. Это способствует его переходу в неводную фазу,
в которой данная соль не растворяется. Можно изменять рН водной среды, содержащей кислые или щелочные растворенные вещества, чтобы уменьшить ионизацию некоторых из них и обеспечить их концентрирование в неводной фазе экстрагента.
Для получения наиболее благоприятного равновесного соотношения на каждой ступени экстракции изменяют температуру контролируемых фаз.
Простое выщелачивание растворимого компонента из инертного твердого вещества можно рассматривать как специальный случай жидкостной экстракции. Многие расчетные методы для систем жидкость-жидкостьприменимы и для системжидкость-твердоетело.
Для увеличения интенсивности процесса массопередачи, в любом случае необходимо проводить фазы экстрагента и исходного раствора в тесный контакт.
Когда система приближается к равновесию, производится механическое разделение фаз.
После этого, желательно подвергнуть каждую из фаз дальнейшей обработке, например, в противоточном процессе. Экстрагент регенерируют для повторного использования, после выделения конечных продуктов в чистом виде.
Этот процесс связан с проведением дистилляции.
На рис. 2.6 показана простейшая схема экстракции, где экстрактор работает совместно с двумя дистилляционными установками.

Очищенный рафинат R (обогащенный
компонентом А)
Рафинат R
Экстратор
Исходная смесь
F(A+B) Очищенный экстракт Е (обогащенный компонентом В)
| Дистилляционная |
Экстракт Е | установка |
Регенерированный экстракт S
Рис. 2.6. Упрощенная схема процесса экстракции в системе жидкость–жидкостьс регенерацией экстрагента
Схема позволяет проводить процесс непрерывно, получая в достаточно чистом виде легколетучие компоненты А иВ.
Из экстрактора удалятся два потока.
Фаза, состоящая в основном из экстрагента (избирательного растворителя) называется фазой экстракта, а очищенный конечный продукт – очищенным экстрактом. Фаза, подвергшаяся обработке избирательным растворителем, называется фазой рафината. Рафинатом или экстрактом может быть любая из фаз.
Коэффициентом распределения в процессах экстракции называется отношение весовой или молярной доли распределенного компонента С в фазе, богатойА (хСа), т.е.
К = | х(СВ) | =const, | (2.68) |
| |||
| х |
| |
| (Са) |
| |
где К – коэффициент распределения, величина большая единицы. Соотношение (2.68) обычно хорошо оправдывается для малых
концентраций распределяемого вещества и когда отсутствует диссоциация или ассоциация молекул распределяемого вещества в фазах.
В общем случае хорошо применимым является соотношение:
хm
К = CB , (2.69))xCa
где m>1 в общем случае величина переменная.
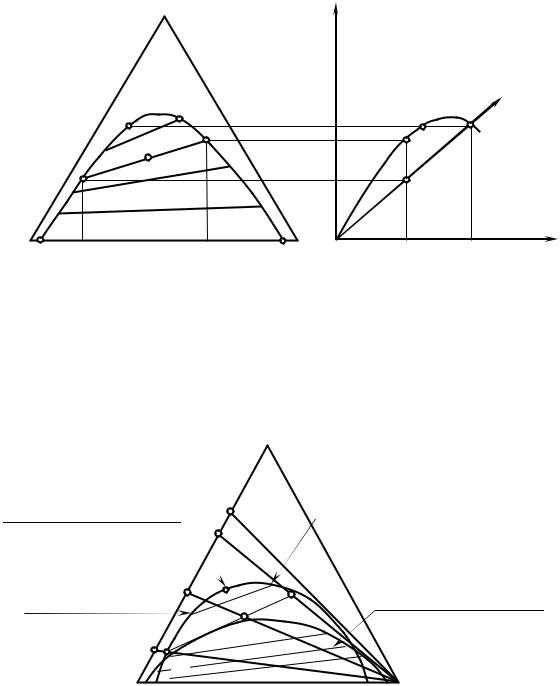
Графики, характеризующие величину коэффициента распределения, представлены на рис 2.7.
Так как С больше растворим вВ, чем вА, то точки левой ветви пограничной кривой треугольной диаграммы дают значениехСА, а точки правой части ветви – значениехСВ, точка перегибаQ лежит на диагонали прямоугольной диаграммы и ей соответствует равенствохСВ=хСА.
При малых концентрациях, близко к началу координат, кривая распределения приближается к прямой (линейный закон распределения), что находится в соответствии с равенством (2.68).
| С | xCB |
|
|
|
|
|
|
| ||
|
|
|
| xCB= xCD | |
Q |
| xQ |
|
| Q |
M | E | xCB | E, R |
| |
|
| ||||
R |
|
|
|
| |
|
|
|
|
| |
xD |
|
|
|
|
|
A D | N | B | xR | xQ | xCA |
Рис. 2.7. Построение прямоугольной диаграммы из треугольной | |||||
Типичная треугольная фазовая диаграмма с изображением процесса представлена на рис. 2.8. Диаграмма (рис. 2.7) для жидкой смеси типа I, для которой область взаимной нерастворимости компонентов примыкает только к одной стороне треугольника.
|
|
|
| B |
|
критическая точка | E* |
| экстракт | ||
E′ |
|
| |||
рафинат |
| F | M | E | хорды равновесия |
|
| ||||
|
|
|
| ||
|
| R′ |
|
|
|
| A | R |
|
| S |
|
|
|
| ||
Рис. 2.8. Треугольная фазовая диаграмма
Экстрагент S настолько близок химически компонентуВ, что смесиВ иS полностью взаимно растворимы. Химическая природа экстрагентаS и компонентаА различна, в результате чего бинарные смесиА иS разделяются на две жидкие фазы.
Добавление компонента В к подобным смесям способствует повышению растворимостиА вS и наоборот. В критической точке обе фазы превращаются в одну. Состав слоев экстракта лежат справа от критической точки. Составы слоев рафината – слева от критической точки. ЛинияRE представляет собой хорду равновесия, которая соединяет составы рафината и экстракта, находящиеся в термодинамическом равновесии друг с другом.
Физическая смесь М исходного раствора и экстрагента расслаивается на фазыR иE.
После удаления экстрагента из последних получают фазы R′ иE′. Рассмотренный процесс чаще включает многократное проточное
смещение и разделение фаз, чем единичные контакты и сепарацию, показанные на диаграмме.
На рис 2.8 видно, что концентрация компонента В в очищенном экстракте ограничена вследствие замыкания области существования двух фаз в критической точке. Наиболее концентрированный экстракт, который может быть получен в данном случае, соответствует точкеЕ .
Избирательный растворитель сообщает противоположные термодинамические свойства молекулам растворенного вещества в фазах экстракта и рафината.
Для облегчения сепарации желательно наличие существенной разности плотности фаз и большое межфазовое натяжение.
В экстракторе любая из фаз может диспергироваться в другую, как показано на рис 2.9.
Легкая жидкость |
| б) | Легкая жидкость | |
| Токи равного | |||
|
| давления |
| Токи равного |
|
|
| давления | |
Поверхность |
|
| ||
|
|
| ||
раздела фаз |
| Тяжелая |
| |
|
| Тяжелая |
| |
Тяжелая |
| жидкость | жидкость |
|
жидкость |
|
|
|
|
|
|
|
| Тяжелая |
|
|
|
| жидкость |
Легкая |
|
| Легкая |
|
жидкость |
|
| жидкость |
|
Поверхность раздела фаз
Рис. 2.9. Расположение поверхности раздела фаз в распылительных экстракторах
а – легкая | жидкость диспергируется | в тяжелой; |
б – тяжелая | жидкость диспергируется в | легкой |
Экстрактор представляет собой, по существу, одно из колен двухжидкостного манометра, работающего так, чтобы поверхность раздела между фазами поддерживалась в верхней или нижней части рабочего объема аппарата.
Если точка перелива (гидравлический затвор) расположена высоко, то столбы жидкости в аппарате и переливе балансируются, когда поверхность раздела фаз находится у верха аппарата (рис. 2.9а). При более низком расположении точки перелива поверхность раздела фаз поддерживается вблизи днища аппарата (рис. 2.9б).
В первом случае, при высокой точке перелива, более легкая фаза диспергируется в более тяжелой, причем последняя является сплошной.
Во втором случае, показано диспергирование более тяжелой фазы в легкой (сплошной).
Коэффициент массопередачи и скорость захлебывания в противоточном экстракторе зависит от того, какая из фаз (легкая или тяжелая) является сплошной.
При прочих равных условиях обычно лучше диспергировать фазу с большей объемной скоростью, чтобы обеспечить большую величину поверхности контакта фаз.
Проектирование аппаратуры для процессов жидкостной экстракции основывается на законах равновесия фаз, уравнениях скоростей массопередачи
studfiles.net
1.6. Жидкостная экстракция
Жидкостная экстракция– процесс разделения смесей взаимнорастворимых жидкостей путём перехода одного или нескольких компонентов смеси из одной жидкой фазы в другую, практически не растворимую или плохо растворимую в первой фазе. Процесс протекает при непосредственном контакте двух жидких фаз и основан на различии растворимости извлекаемого компонента в этих фазах.
Процессы жидкостной экстракции применяют в химической, нефтехимической, фармацевтической, гидрометаллургической и других отраслях промышленности при получении редких элементов, извлечении ценных или токсичных веществ из растворов, в том числе из сточных вод.
Жидкостная экстракция, наряду с перегонкой и ректификацией, является одним из основных методов разделения однородных жидких смесей. При малой концентрации извлекаемого компонента процесс экстракции обычно экономически более выгоден, чем перегонка и ректификация, поскольку при экстракции нет необходимости испарять значительную часть жидкой смеси. Кроме того, экстракцию целесообразно применять в случае, если смесь невозможно или трудно разделить ректификацией, или разделяемые компоненты разлагаются при нагревании.
Экстрагирующую жидкость, в которую переходит извлекаемый компонент, называют экстрагентомили растворителем. Раствор извлечённых веществ в экстрагенте называютэкстрактом, а раствор, из которого удалены экстрагируемые компоненты –рафинатом.
По принципу взаимодействия и способу контакта фаз экстракторы подразделяют на две группы: ступенчатые (смесительно-отстойные)идиффренциально-контактные. Ступенчатый экстрактор представляет собой несколько последовательно соединённых ступеней, каждая из которых состоит из аппарата смешения и отстойника эмульсий. Такие аппараты громоздки, и обычно не используются, если для эффективного разделения требуется более трёх ступеней.
Из дифференциально-контактных экстракторов наибольшее распространение получили: полые колонные экстракторы, насадочные, тарельчатые, роторно-дисковые и центробежные экстракторы.
Полые (распылительные) колонные экстракторы
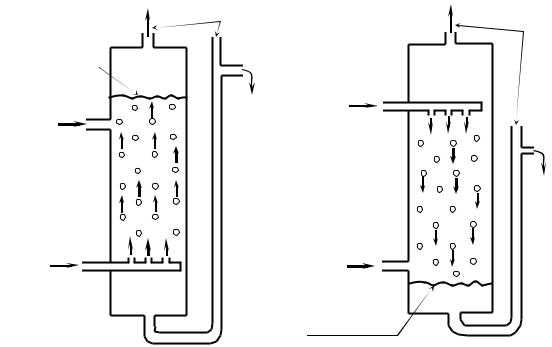
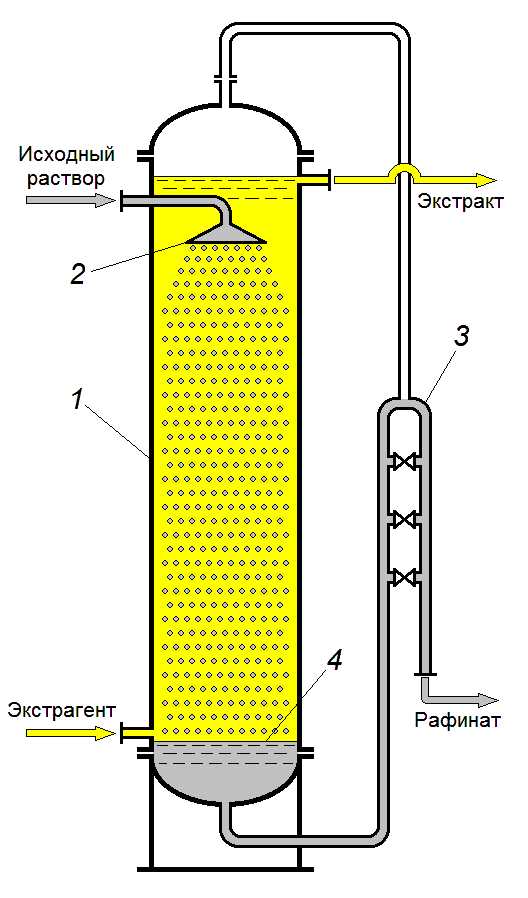
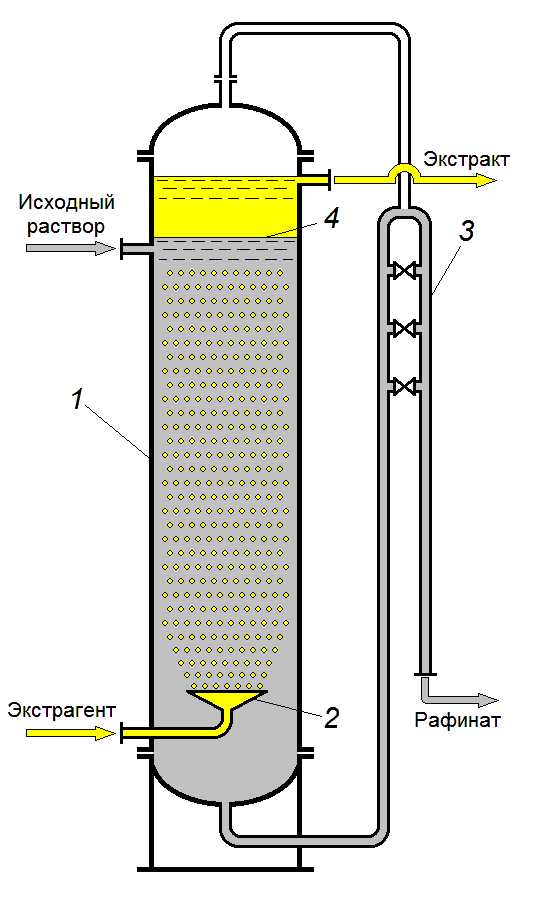
Наиболее простыми по устройству дифференциально-контактными экстракторами являются распылительные колонны. Они относятся к гравитационным экстракторам – аппаратам, где движение диспергированной фазы через сплошную происходит вследствие разности их плотностей. В зависимости от того, какую фазу диспергируют, конструкция экстрактора несколько различается (см. рис. 42). Эти экстракторы представляют собой полые колонны с устройствами для диспергирования тяжёлой (рис. 46 а) или лёгкой (рис. 46 б) фазы (исходного раствора или экстрагента). Сплошная и дисперсная фазы перемещаются противотоком. Капли диспергированной фазы, пройдя через столб сплошной фазы, коалесцируют в сплошной слой, после чего выводятся из колонны. Тяжёлая фаза уходит через гидрозатвор, с помощью которого регулируют уровень раздела фаз в колонне.
Полые колонные экстракторы просты в устройстве и дёшевы в изготовлении. Важным достоинством этих аппаратов является возможность обработки в них загрязнённых твёрдыми частицами жидкостей. Иногда эти аппараты используют для экстрагирования из пульп и суспензий.
 а
б
Рис. 42. Полые
колонные экстракторы с распылением
тяжёлой фазы (а) и лёгкой фазы (б):
а
б
Рис. 42. Полые
колонные экстракторы с распылением
тяжёлой фазы (а) и лёгкой фазы (б):
1 – корпус, 2 – распределительное устройство, 3 – гидрозатвор, 4 – поверхность раздела фаз
Полые колонные экстракторы отличаются невысокой эффективностью, что является следствием возникающего в них продольного перемешивания, снижающего движущую силу массопередачи. При большой доле дисперсной фазы снижается сечение для движения сплошной фазы и увеличивается унос капель, что может привести к захлёбыванию экстрактора.
studfiles.net
2.5. Жидкостная экстракция
Контрольные вопросы:
1.Что называется абсорбцией? Когда применяется процесс абсорбции?
2.В чем состоит сущность переноса вещества между фазами?
3.Что понимается под движущей силой массообмена абсорбцией?
4.От каких факторов зависит скорость массопередачи?
5.Какими способами осуществляется контакт жидкости и газа?
6.Сущность модели Хигби для определения скорости массопередачи
7.Что называется равновесным соотношением в системе газ – жидкость?
8.Какими параметрами определяется равновесное распределение между двумя фазами (газ-жидкость)?
9.Что называется идеальными системами?
10.Сформулируйте закон Рауля.
11.Сформулируйте закон Дальтона.
12.Дайте характеристику неидеальным системам.
13.Что такое коэффициент активности, и в каких процессах он применяется?
2.5.1.Сущность и основные понятия и определения
Процессы разделения, в которых две взаимно нерастворимые или частично растворимые друг в друге фазы приводятся в контакт для перехода одного или более компонентов из одной фазы в другую, представляют собой экстракцию в системе жидкость-жидкостьили, в более широком смысле слова, – экстракцию избирательными растворителями.
Процессы экстракции являются преимущественно физическими, так как подлежащие переносу из фазы в фазу вещества извлекаются обычно без химических превращений.
Вместе с тем физические равновесные соотношения в значительной мере зависят от химических характеристик растворенных веществ и избирательных растворителей (экстрагентов).
Применение экстрагента, который ближе по своей химической природе к одному из компонентов смеси, приводит к повышению концентрации этого компонента в фазе экстракта.
Экстракция избирательными растворителями проводится различными способами. В простейшем случае к жидкой смеси (исходному раствору) добавляют один экстрагент, что приводит к образованию второй жидкой фазы.
Иногда добавляют два взаимно нерастворимых экстрагента, чтобы компоненты исходного раствора распределялись между двумя жидкими фазами. В водную фазу желательно добавлять соль для повышения активности распределяемого компонента. Это способствует его переходу в неводную фазу,
в которой данная соль не растворяется. Можно изменять рН водной среды, содержащей кислые или щелочные растворенные вещества, чтобы уменьшить ионизацию некоторых из них и обеспечить их концентрирование в неводной фазе экстрагента.
Для получения наиболее благоприятного равновесного соотношения на каждой ступени экстракции изменяют температуру контролируемых фаз.
Простое выщелачивание растворимого компонента из инертного твердого вещества можно рассматривать как специальный случай жидкостной экстракции. Многие расчетные методы для систем жидкость-жидкостьприменимы и для системжидкость-твердоетело.
Для увеличения интенсивности процесса массопередачи, в любом случае необходимо проводить фазы экстрагента и исходного раствора в тесный контакт.
Когда система приближается к равновесию, производится механическое разделение фаз.
После этого, желательно подвергнуть каждую из фаз дальнейшей обработке, например, в противоточном процессе. Экстрагент регенерируют для повторного использования, после выделения конечных продуктов в чистом виде.
Этот процесс связан с проведением дистилляции.
На рис. 2.6 показана простейшая схема экстракции, где экстрактор работает совместно с двумя дистилляционными установками.

Очищенный рафинат R (обогащенный
компонентом А)
Рафинат R
Экстратор
Исходная смесь
F(A+B) Очищенный экстракт Е (обогащенный компонентом В)
| Дистилляционная |
Экстракт Е | установка |
Регенерированный экстракт S
Рис. 2.6. Упрощенная схема процесса экстракции в системе жидкость–жидкостьс регенерацией экстрагента
Схема позволяет проводить процесс непрерывно, получая в достаточно чистом виде легколетучие компоненты А иВ.
Из экстрактора удалятся два потока.
Фаза, состоящая в основном из экстрагента (избирательного растворителя) называется фазой экстракта, а очищенный конечный продукт – очищенным экстрактом. Фаза, подвергшаяся обработке избирательным растворителем, называется фазой рафината. Рафинатом или экстрактом может быть любая из фаз.
Коэффициентом распределения в процессах экстракции называется отношение весовой или молярной доли распределенного компонента С в фазе, богатойА (хСа), т.е.
К = | х(СВ) | =const, | (2.68) |
| |||
| х |
| |
| (Са) |
| |
где К – коэффициент распределения, величина большая единицы. Соотношение (2.68) обычно хорошо оправдывается для малых
концентраций распределяемого вещества и когда отсутствует диссоциация или ассоциация молекул распределяемого вещества в фазах.
В общем случае хорошо применимым является соотношение:
хm
К = CB , (2.69))xCa
где m>1 в общем случае величина переменная.
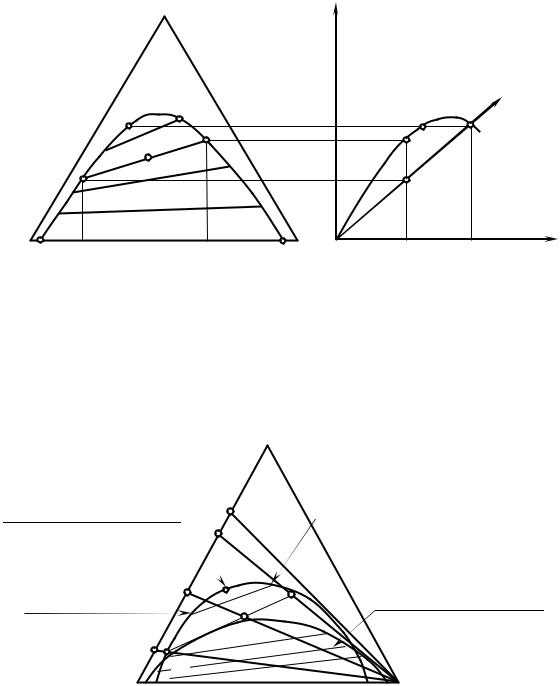
Графики, характеризующие величину коэффициента распределения, представлены на рис 2.7.
Так как С больше растворим вВ, чем вА, то точки левой ветви пограничной кривой треугольной диаграммы дают значениехСА, а точки правой части ветви – значениехСВ, точка перегибаQ лежит на диагонали прямоугольной диаграммы и ей соответствует равенствохСВ=хСА.
При малых концентрациях, близко к началу координат, кривая распределения приближается к прямой (линейный закон распределения), что находится в соответствии с равенством (2.68).
| С | xCB |
|
|
|
|
|
|
|
| |
|
|
|
| xCB= xCD | |
Q |
| xQ |
|
| Q |
M | E | xCB | E, R |
| |
|
| ||||
R |
|
|
|
| |
|
|
|
|
| |
xD |
|
|
|
|
|
A D | N | B | xR | xQ | xCA |
Рис. 2.7. Построение прямоугольной диаграммы из треугольной | |||||
Типичная треугольная фазовая диаграмма с изображением процесса представлена на рис. 2.8. Диаграмма (рис. 2.7) для жидкой смеси типа I, для которой область взаимной нерастворимости компонентов примыкает только к одной стороне треугольника.
|
|
|
| B |
|
критическая точка | E* |
| экстракт | ||
E′ |
|
| |||
рафинат |
| F | M | E | хорды равновесия |
|
| ||||
|
|
|
| ||
|
| R′ |
|
|
|
| A | R |
|
| S |
|
|
|
| ||
Рис. 2.8. Треугольная фазовая диаграмма
Экстрагент S настолько близок химически компонентуВ, что смесиВ иS полностью взаимно растворимы. Химическая природа экстрагентаS и компонентаА различна, в результате чего бинарные смесиА иS разделяются на две жидкие фазы.
Добавление компонента В к подобным смесям способствует повышению растворимостиА вS и наоборот. В критической точке обе фазы превращаются в одну. Состав слоев экстракта лежат справа от критической точки. Составы слоев рафината – слева от критической точки. ЛинияRE представляет собой хорду равновесия, которая соединяет составы рафината и экстракта, находящиеся в термодинамическом равновесии друг с другом.
Физическая смесь М исходного раствора и экстрагента расслаивается на фазыR иE.
После удаления экстрагента из последних получают фазы R′ иE′. Рассмотренный процесс чаще включает многократное проточное
смещение и разделение фаз, чем единичные контакты и сепарацию, показанные на диаграмме.
На рис 2.8 видно, что концентрация компонента В в очищенном экстракте ограничена вследствие замыкания области существования двух фаз в критической точке. Наиболее концентрированный экстракт, который может быть получен в данном случае, соответствует точкеЕ .
Избирательный растворитель сообщает противоположные термодинамические свойства молекулам растворенного вещества в фазах экстракта и рафината.
Для облегчения сепарации желательно наличие существенной разности плотности фаз и большое межфазовое натяжение.
В экстракторе любая из фаз может диспергироваться в другую, как показано на рис 2.9.
а) | Легкая жидкость |
| б) | Легкая жидкость |
| Токи равного | |||
|
| давления |
| Токи равного |
|
|
| давления | |
Поверхность |
|
| ||
|
|
| ||
раздела фаз |
| Тяжелая |
| |
|
| Тяжелая |
| |
Тяжелая |
| жидкость | жидкость |
|
жидкость |
|
|
|
|
|
|
|
| Тяжелая |
|
|
|
| жидкость |
Легкая |
|
| Легкая |
|
жидкость |
|
| жидкость |
|
Поверхность раздела фаз
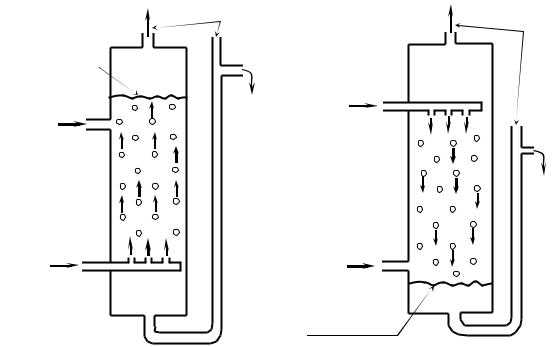
Рис. 2.9. Расположение поверхности раздела фаз в распылительных экстракторах
а – легкая | жидкость диспергируется | в тяжелой; |
б – тяжелая | жидкость диспергируется в | легкой |
Экстрактор представляет собой, по существу, одно из колен двухжидкостного манометра, работающего так, чтобы поверхность раздела между фазами поддерживалась в верхней или нижней части рабочего объема аппарата.
Если точка перелива (гидравлический затвор) расположена высоко, то столбы жидкости в аппарате и переливе балансируются, когда поверхность раздела фаз находится у верха аппарата (рис. 2.9а). При более низком расположении точки перелива поверхность раздела фаз поддерживается вблизи днища аппарата (рис. 2.9б).
В первом случае, при высокой точке перелива, более легкая фаза диспергируется в более тяжелой, причем последняя является сплошной.
Во втором случае, показано диспергирование более тяжелой фазы в легкой (сплошной).
Коэффициент массопередачи и скорость захлебывания в противоточном экстракторе зависит от того, какая из фаз (легкая или тяжелая) является сплошной.
При прочих равных условиях обычно лучше диспергировать фазу с большей объемной скоростью, чтобы обеспечить большую величину поверхности контакта фаз.
Проектирование аппаратуры для процессов жидкостной экстракции основывается на законах равновесия фаз, уравнениях скоростей массопередачи
studfiles.net
Экстракция
Экстракцией в широком смысле называют процессы извлечения одного или нескольких компонентов из растворов или твердых тел с помощью избирательных растворителей (экстрагентов). При взаимодействии с экстрагентом в нем хорошо растворяются только извлекаемые компоненты и значительно слабее или практически вовсе не растворяются остальные компоненты исходной смеси.
В химической технологии экстракция из растворов экстрагентами более распространена, чем экстракция из твердых тел. Экстракция из твердых веществ или квазитвердых материалов (например, из тканей растительного сырья) применяется главным образом в лесохимической, пищевой и фармацевтической промышленности. В химической технологии используют в основном экстракцию из твердых пористых веществ водой или водными растворами кислот и щелочей (процессы выщелачивания).
Как следует из главы X, процесс массоотдачи в твердой фазе существенно отличается от массоотдачи в жидкостях, поэтому процессы экстракции в системах жидкость — жидкость и в системах жидкость — твердое тело должны рассматриваться раздельно.
Процессы экстракции в системах жидкость — жидкость Общие сведения
Процессы экстракции в системах жидкость — жидкость находят широкое применение в химической, нефтеперерабатывающей и нефтехимической и других отраслях промышленности. Они эффективно используются для выделения в чистом виде различных продуктов органического и нефтехимического синтеза, извлечения и разделения редких и рассеянных элементов, очистки сточных вод и т. д.
Экстракция в системах жидкость — жидкость представляет собой диффузионный процесс, протекающий; с участием двух взаимно нерастворимых или ограниченно растворимых жидких фаз, между которыми распределяется экстрагируемое вещество (или несколько веществ). Так, например, очистку сточных вод производят экстракцией бутил ацетатом, в который предпочтительно переходят одноатомные и многоатомные фенолы.
Для повышения скорости процесса исходный раствор и экстрагент приводят в тесный контакт, осуществляемый обычно многократно. В результате взаимодействия фаз получают экстракт — раствор извлеченных веществ в экстрагенте и рафинат — остаточный исходный раствор, из которого с той или иной степенью полноты удалены экстрагируемые компоненты. Полученные жидкие фазы (экстракт и рафинат) отделяются друг от друга отстаиванием, иногда центрифугированием или другими механическими способами. После этого производят извлечение целевых продуктов из экстракта и регенерацию экстрагента из рафината.
Соответствующие компоненты выделяются из экстракта либо ректификацией, либо путем реэкстракции, например перевода их в водный раствор. Во избежание потерь экстрагента, растворенного или унесенного рафинатом, экстрагент выделяют ректификацией или экстракцией другим растворителем и возвращают для последующего использования.
Принципиальная схема процесса непрерывной экстракции приведена на рис. ХIII-1, а. Процесс собственно экстракции происходит в колонном экстракторе 1, после чего производится выделение извлеченных веществ из экстракта (в ректификационной колонне 2 и экстрагента из рафината (в ректификационной колонне 3).
На рис. ХIII-1, б показана типичная схема экстракции солей металлов, отличающаяся тем, что после колонного экстрактора 4 соли извлекаются из экстракта путем перевода их в водный раствор (реэкстракции) в колонне 5. Экстрактор 4 может иметь, как видно из рисунка, промывную секцию для дополнительной отмывки экстракта от нежелательных примесей.
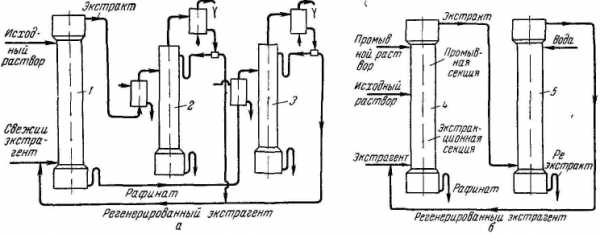
Рис ХIII-1 Принципиальнее схемы процесса экстракции в системах жидкость — жидкость:
а — непрерывная экстракция; б — экстракция солей металлов; 1 — колонный экстрактор; 2 — ректификационная колонна для выделения извлеченных веществ из экстракта, 3 — ректификационная колонна для регенерации экстрагента из рафината; 4 — колонный экстрактор; 5 — колонна для реэкстракции.
В ряде случаев процесс экстракции усложняется, в частности, вследствие химической реакции, протекающей в объеме или на поверхности раздела фаз. При определенных условиях для лучшего разделения исходного раствора применяют специфические способы экстракции. Так, например, исходный раствор, представляющий собой смесь органических веществ, оказывается целесообразным обрабатывать двумя взаимно нерастворимыми экстрагентами, между которыми распределяются извлекаемые компоненты. Для облегчения перехода экстрагируемых компонентов, например солей металлов, в органическую фазу иногда применяют высаливание, осуществляемое путем добавки соли с одноименными ионами в исходный водный раствор, а также регулируют кислотность или рН раствора, концентрацию экстрагента в инертном разбавителе, служащим для уменьшения его вязкости, и т. д.
Основным достоинством процесса экстракции по сравнению с другими процессами разделения жидких смесей (ректификацией, выпариванием и др.) является низкая рабочая температура процесса, который проводится наиболее часто при нормальной (комнатной) температуре. При этом отпадает необходимость в затратах тепла на испарение раствора. Кроме того, при экстракции обычно возможно из многочисленных растворителей подбирать высокоизбирательный экстрагент, отличающийся по химическим свойствам от компонентов исходной смеси и часто позволяющий достичь более полного разделения, чем это осуществимо с помощью других массообменных процессов. Вместе с тем применение дополнительного компонента — экстрагента и необходимость его регенерации приводит к некоторому усложнению аппаратурного оформления и удорожанию процесса экстракции.
При извлечении летучих веществ экстракция может успешно конкурировать с ректификацией в тех случаях, когда разделение ректификацией либо затруднено, а иногда и практически невозможно (разделение смесей, состоящих из близкокипящих компонентов и азеотропных смесей), либо сопряжено с чрезмерно высокими затратами (извлечение вредных примесей или ценных веществ из сильно разбавленных растворов). Так, например, извлечение уксусной кислоты из ее малоконцентрированных водных растворов экстракцией этилацетатом (или смесью этилацетата и бензола) является значительно более экономичным, чем выделение ректификацией, так как, несмотря на довольно большую разность температур кипения воды и кислоты, относительная летучесть их невелика. Кроме того, необходимость испарения очень больших количеств воды весьма удорожает ректификацию.
Экстракция незаменима для разделения смесей веществ, чувствительных к повышенным температурам, например антибиотиков, которые могут разлагаться при разделении их ректификацией или выпариванием. Применение экстракции часто позволяет эффективно заменять такие процессы, как разделение высококипящих веществ с использованием глубокого вакуума, например молекулярной дистилляцией, или разделение смесей методом фракционированной кристаллизации.
Экстракция может служить также экономичным и эффективным методом разделения сложных смесей на классы соединений одинакового химического состава, температуры кипения которых перекрывают друг друга (разделение ароматических и предельных углеводородов, кипящих в том же интервале температур).
Весьма перспективно применение экстракции для разделения смесей неорганических веществ, когда другие способы разделения неприменимы. Процессы жидкостной экстракции в настоящее время успешно используются для переработки ядерного горючего, получения циркония и гафния и многих других редких металлов. С помощью экстракции можно получать высокочистые цветные и благородные металлы.
В ряде случаев значительный эффект достигается при сочетании экстракции с другими процессами разделения. Примерами подобных комбинированных процессов являются: разделение близкокипящих и азеотропных смесей с помощью экстрактивной ректификации, предварительное концентрирование разбавленных растворов посредством экстракции перед выпариванием и ректификацией, которые проводятся при этом с меньшим расходом тепла.
studfiles.net
Процессы диффузии и экстракции основные понятия и определения
Экстрагированием называется процесс извлечения одного или нескольких компонентов из смеси веществ путем обработки ее жидким растворителем, обладающим способностью избирательно растворять только извлекаемые компоненты. Физическая сущность экстрагирования заключается в переходе извлекаемого (экстрагируемого) компонента из одной фазы (жидкой или твердой) в фазу экстрагента при их взаимном соприкосновении.
В пищевой промышленности наиболее распространен процесс экстрагирования в системах жидкость-твердое тело: извлечение сахара из свеклы в свеклосахарном производстве, извлечение масел из масличных семян в производстве растительных масел, получение эфирных масел в эфиромасличном производстве, экстрагирование ферментов из культур плесневых грибов в производстве ферментных препаратов, производство вина, пива, крахмала, ликероводочных изделий, растворимых кофе и чая и др.
Жидкостная экстракция (экстрагирование в системах жидкость-жидкость) применяется в производствах, связанных с получением спирта, вина, растительных масел и других пищевых продуктов.
Движущей силой диффузии компонентов из исходных технологических сред в экстрагенты является разность концентраций в обеих средах, т. е. процесс экстракции базируется на законах диффузии и равновесного распределения переходящих компонентов между двумя фазами (жидкость-жидкость, твердое тело-жидкость).
Экстракция в системе жидкость-жидкость
Жидкие фазы, участвующие в процессе экстракции, носят названия экстрагент (растворитель) и исходный раствор. Извлекаемыми компонентами могут быть органические и неорганические вещества.
В начальный момент процесса исходные фазы (первичный раствор и экстрагент) приводят в тесное соприкосновение, обеспечивающее большие поверхности контакта между ними. При этом получают две фазы, которые называются экстрактом и рафинатом. Экстракт представляет собой раствор извлеченного компонента в экстрагенте, рафинат – остаточный исходный раствор. Обычно одна фаза является сплошной, а вторая – дисперсной, распределяемой в первой в виде капель.
Экстрагирование включает следующие основные операции:
смешение исходной смеси веществ и экстрагента с целью более тесного контакта между ними;
механическое разделение двух несмешивающихся фаз на экстракт и рафинат;
удаление и регенерацию экстрагента и рафината.
Для успешного проведения экстракции исходный раствор и экстрагент должны быть взаимно нерастворимы друг в друге. Выбор экстрагента в каждом конкретном случае представляет собой сложную задачу, поскольку при этом необходимо уметь определять или оценивать характер сил взаимодействия молекул экстрагента и растворяемого вещества.
Для промышленного использования экстрагента необходимо, чтобы он обладал: малой растворимостью в первичном растворителе; хорошей избирательностью (селективностью), т. е. способностью извлекать из исходной смеси или материала только один (целевой) компонент или группу компонентов; высоким коэффициентом распределения kP, что дает возможность снизить расход растворителя на единицу исходной смеси; высоким коэффициентом диффузии D, что позволяет увеличить скорость процесса и, следовательно, уменьшить размеры экстрактора; невоспламеняемостью или узким пределом температур вспышки; некоррозионными свойствами по отношению к материалу аппаратуры; низкой температурой замерзания или застывания; безвредностью для здоровья обслуживающего персонала; низкой теплоемкостью, высокой летучестью, низкой теплотой испарения для снижения затрат на регенерацию.
Равновесие в системах жидкость-жидкость. Расчет статики процесса. В системах жидкость-жидкость обычно существует две фазы (две несмешивающиеся жидкости) и три компонента, т. е. такие системы называются тройными. Поэтому согласно правилу фаз число параметров, определяющих состояние системы, будет
3 + 2 = 2 + N, N = 3.
Равновесное распределение третьего компонента между двумя жидкими фазами фиксируется значениями концентраций в каждой фазе и температурой и наглядно выражается при помощи треугольной диаграммы (рис. 1).
В этой диаграмме процентное содержание компонентов А, В и С отложено на сторонах треугольника, состав смеси определяется точками (М), расположенными внутри него, а точки S, лежащие на его сторонах определяют составы бинарных смесей. Компонент В растворим в А и С во всех соотношениях, компоненты А и С ограниченно растворимы друг в друге.
С
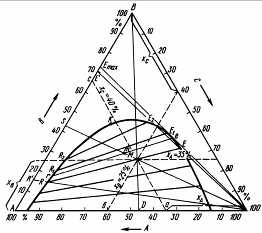
Рис. 1. Треугольная диаграмма
остав тройной смеси определяют на сторонах треугольника длиной отрезков, отсекаемых параллельными сторонам линиями, проведенными через точкуМ (на рис. 1: 35 % А; 25 % В; 40 % С). Кривая RE ограничивает область взаимной растворимости компонентов и выражает равновесное распределение компонента В в А и С. Точки, лежащие под пограничной кривой RE, соответствуют области расслоения жидкостей А и С; точки, расположенные выше пограничной кривой, находятся в области полной взаимной растворимости компонентов, где существует лишь одна фаза.Состав расслаивающихся жидкостей при равновесном насыщении под пограничной кривой для точки М характеризуется точками R и E. Все смеси вдоль линии RE образуют два слоя состава R и E.
Так как полученная после экстракции смесь расслаивается на две фазы: экстракт Е, обогащенный компонентом В, и обедненный рафинат R, которые находятся в равновесии, то построенная по экспериментальным данным линия ЕR, соединяющая точки равновесных концентраций для рафината и экстракта и называемая линией равновесных концентраций (конодой), будет находиться внутри треугольной диаграммы. Угол наклона этой линии зависит от коэффициента распределения, определяемого как
kр= y*/х, (1)
где y* и x – равновесные доли распределяемого компонента в экстракте и рафинате соответственно.
По величине коэффициента распределения судят об экстракционной способности растворителя: чем больше kр, тем выше способность данного растворителя извлекать целевой компонент.
Для оценки разделяющей способности растворителя используют соотношение
. (2)
Величину  называюткоэффициентом,
или фактором разделения в экстракции, который показывает, во
сколько раз отношение равновесных
концентраций разделяемых компонентов
в экстракте больше по сравнению с
рафинатом. Концентрации чаще выражают
в абсолютных или относительных массовых
долях (или процентах).
называюткоэффициентом,
или фактором разделения в экстракции, который показывает, во
сколько раз отношение равновесных
концентраций разделяемых компонентов
в экстракте больше по сравнению с
рафинатом. Концентрации чаще выражают
в абсолютных или относительных массовых
долях (или процентах).
По данным треугольной диаграммы можно построить диаграмму равновесия типа х–у (х – содержание экстрагируемого компонента В в рафинате, а у – в экстракте), удобную для дальнейшего расчета процесса (рис. 2).
Случаю, представленному на рис. 1, соответствует kp > 1; при kp < 1 коноды будут наклонены в обратном направлении, а при kp = 1 они будут параллельны стороне АС. Число таких конод в пределах пограничной кривой равно бесконечности. При пересечении конод в одной точке можно определить положение фокуса О по двум известным конодам, что позволяет наносить любые другие точки при отсутствии для них экспериментальных данных и построить график равновесного распределения.
К
Рис. 2. Преобразование диаграммы равновесия экстракции
оноды в пределах пограничной кривой с увеличением компонентаВ становятся все меньше и меньше, превращаясь в точку перегиба К (в критическую точку). Здесь два жидкостных слоя становятся идентичными по составу и плотности. Равновесное распределение третьего компонента (например, В) между фазами (А и С) при расчетах процесса экстракции можно представить в виде коэффициента распределения kp.При изменении содержания компонента В в смеси равновесные составы будут располагаться на других хордах равновесия. Перемещения от стороны треугольника АС до критической точки К соответствует исчезновению поверхности раздела между фазами при их расслаивании, т. е. когда система становится гомогенной.
При расслаивании смеси М на фазы R и Е составы последних находятся на одной прямой с составом исходной смеси. Количество фаз R и Е относятся как длины отрезков МЕ и МR. Это правило пропорциональности является общим, и поэтому оно справедливо для случаев, когда к смеси двух компонентов добавляется третий. Если к смеси А и В, состав которой выражается точкой S, добавлен компонент С, то состав полученной тройной смеси выразится точкой М на прямой CS, причем
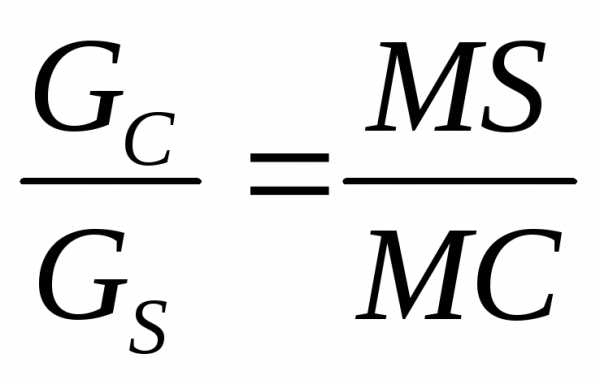 ,
(3)
,
(3)
что вытекает из правила пропорциональности. При этом отрезок АS соответствует содержанию в исходной смеси компонента В, а отрезок SВ – содержанию компонента А. На прямой линии, соединяющей точки S и С, будет находиться точка М, отвечающая составу новой смеси, положение которой определяют по правилу рычага из уравнения
. (4)
Это уравнение выводится из подобия треугольников СМб и MSc (на рис. 1).
Разделение смеси возможно, если точка М располагается в области диаграммы, ограниченной бинодальной кривой. Проводя через точку М прямую RE (коноду) под углом
, (5)
можно определить на ее концах, лежащих на бинодальной кривой, составы фаз после их расслоения: состав рафината – в точке R, экстракта – в точке Е.
Количество экстракта
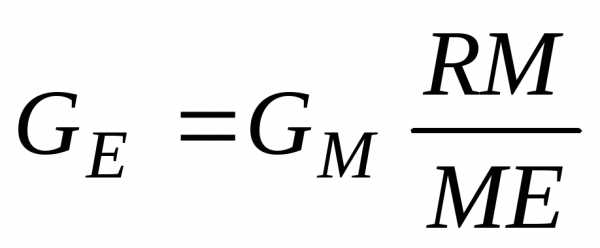 ,
(6)
,
(6)
где общее количество смеси
; (7)
причем количество растворителя
. (8)
Количество рафината
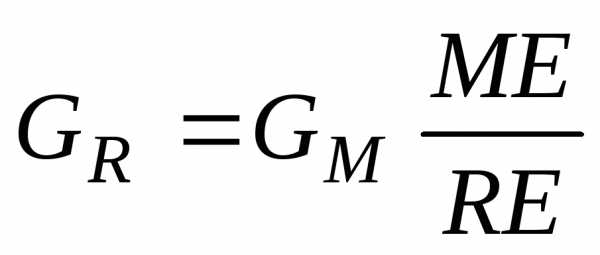 .
(9)
.
(9)
Количество экстракта после испарения растворителя С, если пренебречь растворением компонента В в рафинате, можно определить по формуле
. (10)
Содержание в экстракте компонента В определяется отрезком АЕ` на пересечении линии, проведенной из точки С через точку Е, со стороной АВ треугольника. Содержание в рафинате компонента В определяется отрезком AR`. Если провести касательную из точки С к бинодальной кривой и продолжить ее до пересечения со стороной АВ, то получим отрезок АЕmax, который характеризует максимально возможное содержание компонента В в экстракте. При этом можно определить положение точек m и r, если провести через точку касания e коноду er.
studfiles.net
Системы жидкость жидкость жидкостная экстракция
Извлечение целевых компонентов как из жидкостей, так и из твердых пористых тел нередко называют экстракцией (иногда экстрагированием) без уточнений или с добавлением жидкостная , жидкофазная , в системе жидкость—жидкость , из твердого тела , в системе твердое тело—жидкость . Возможно, это связано с формальным сходством уравнений материального баланса и методов расчета процессов в статических условиях с использованием прямоугольных и треугольных диаграмм. Между тем кинетика процессов в системах жидкость—жидкость и твердое тело— жидкость существенно отличается. Например, в системе -жидкость— жидкость межфазная поверхность зависит от гидродинамических условий в аппарате, а в системе твердое тело—жидкость она формируется на предшествующей операции измельчения и от гидродинамики не зависит. [c.50]Экстракция представляет собой процесс разделения, основанный на различной растворимости компонентов смеси в каком-либо растворителе (экстрагенте) или в смеси нескольких растворителей если исходная смесь находится в жидком состоянии и экстракция происходит в системе жидкость — жидкость, то такой процесс называют обычно жидкостной экстракцией. [c.388]
В системах твердое тело — газ (пар) протекают процессы адсорбции (избирательного поглощения твердым веществом — адсорбентом одного или нескольких компонентов газовой, паровой или парогазовой смеси) и десорбции (выделения адсорбированных веществ из твердых тел), а также процессы сушки твердых материалов. В системах твердое тело — жидкость осуществляются процессы получения растворов твердых веществ, кристаллизации из растворов и расплавов, избирательного поглощения твердыми телами (адсорбентами или ионитами) отдельных компонентов из растворов (адсорбция, ионный обмен), выщелачивания или экстрагирования растворимых веществ из твердых тел и промывки осадков, получаемых в процессах разделения суспензий. Для систем жидкость — жидкость характерны процессы разделения жидких смесей путем избирательного растворения отдельных компонентов селективными растворителями, ограниченно смешивающимися с исходным раствором (жидкостная экстракция), а для систем жидкость — газ — процессы разделения газовых смесей путем избирательного поглощения из них одного или нескольких компонентов селективными растворителями (абсорбция) и противоположные процессы выделения растворенных в жидкости газов (десорбция). Наконец, в системах жидкость —пар проводятся процессы разделения жидких смесей (дистилляция и ректификация). [c.402]
Процессы в системах жидкость-жидкость. Условия в насадочной колонне для жидкостной экстракции в основном те же, что в насадочной колонне для контактирования газа и жидкости. Так как плотности двух фаз различаются ненамного, то предельные [c.550]
Таким образом, любой смеситель, разработанный для экстракции в системе жидкость — жидкость, может быть использован для процесса с химической реакцией, если решен вопрос об удовлетвори-те.льном температурном контроле. И наоборот, такой аппарат как смеситель Морриса [21], первоначально спроектированный для проведения реакции в системе жидкость — жидкость и с успехом применяемый в крупномасштабном производстве тринитротолуола, теперь используется для обычной жидкостной экстракции. [c.365]
Массоперенос при больших значениях Ре (метод диффузионного пограничного слоя). При Ре>10 процесс переноса с достаточной для практических целей точностью можно считать установившимся и рассматривать в приближении диффузионного пограничного слоя. Большие значения Ре наиболее характерны для процессов жидкостной экстракции и абсорбции. Это обусловлено весьма малыми значениями коэффициентов диффузии в жидкости для систем жидкость – жидкость или жидкость — газ. Коэффициенты диффузии О в таких системах имеют порядок 10 см /с, и для капель диаметром 2-3 мм значения Ре лежат обычно в интервале 10″ -10. В приближении стационарного диффузионного пограничного слоя уравнение (4.42) принимает вид [c.196]
Ковалев Ю. П., Каган С. 3., Межфазная поверхность в системах жидкость— жидкость при механическом перемешивании, сб. Процессы жидкостной экстракции и хемосорбции , Труды П Всесоюзного совещания по жидкостной экстракции и хемосорбции, изд, Химия , 1965, стр. 43. [c.687]
Классификация. Хим.-технол. процесс в целом – это сложная система, состоящая из единичных, связанных между собой элементов и взаимодействующая с окружающей средой. Элементами этой системы являются 5 групп процессов 1) механические – измельчение, грохочение, таблетирование, транспортирование твердых материалов, упаковка конечного продукта и др. 2) гидромеханические – перемещение жидкостей и газов по трубопроводам и аппаратам, пневматич. транспорт, гидравлич. классификация, туманоулавливание, фильтрование, флотация, центрифугирование, осаждение, перемешивание, псевдоожижение идр. скорость этих процессов определяется законами механики и гидродинамики 3) тепловые – испарение, конденсация, нафевание, охлаждение, выпаривание (см. также Теплообмен), скорость к-рых определяется законами теплопередачи 4) диффузионные или массообменные, связанные с переносом в-ва в разл. агрегатных состояниях из одной фазы в другую,- абсорбция газов, увлажнение газов и паров, адсорбция, дистилляция, ректификация, сушка, кристаллизация (см. также Кристаллизационные методы разделения смесей), сублимация, экстрагирование, жидкостная экстракция, ионный обмен, обратный осмос (см. также Мембранные процессы разделения), электродиализ и др. 5) химические. Все эти процессы рассматриваются как единичные или основные. [c.238]
Барботажные аппараты предназначены для осуществления химических реакций и межфазных взаимодействий в системах газ— жидкость, газ— жидкость— твердое, газ—несмешивающиеся жидкости. Они широко применяются как газо-жидкостные химические реакторы и ферментаторы, флотаторы, а также в процессах физической абсорбции, жидкостной экстракции, смешения жидкостей, аэрации и озонирования воды. [c.512]
Сопоставим определенный
www.chem21.info